Το Πακιστάν διεξάγει έρευνα για δύο διανομείς του ελβετικού φαρμάκου για τον καρκίνο Avastin της Roche, μετά την τύφλωση 12 διαβητικών ασθενών μετά από ενέσεις του φαρμάκου. Το Avastin διαθέτει επίσης άδεια στο Βιετνάμ.
Στο Βιετνάμ, έως τις 27 Σεπτεμβρίου, η Υπηρεσία Φαρμάκων του Βιετνάμ ( Υπουργείο Υγείας ) δεν είχε λάβει καμία αναφορά που να αντικατοπτρίζει ανεπιθύμητες παρενέργειες του Avastin που σχετίζονται με την απώλεια όρασης σε ασθενείς μετά τη χρήση του Avastin.
Η Υπηρεσία Φαρμάκων του Βιετνάμ έλαβε αναφορά από το Γραφείο Αντιπροσωπείας της F. Hoffmann La Roche Ltd. σχετικά με το περιστατικό.
Συγκεκριμένα, στο Πακιστάν, περίπου 12 ασθενείς έχασαν την όρασή τους μετά από χρήση ενέσεων που προμήθευσε ο παράνομος προμηθευτής Genius Pharmaceutical Service. Το φάρμακο έφερε την ετικέτα "Inj. Avastin 1.25mg/0.05ml", δημιουργώντας την εσφαλμένη εντύπωση ότι επρόκειτο για προϊόν της Roche.
Το Avastin της Roche δεν έχει εγκριθεί για οφθαλμική χρήση. Η Genius Pharmaceutical Service προμήθευσε/αραίωσε/επανασυσκεύασε τη δόση των 1,25 mg/0,5 ml υπό ανθυγιεινές και μη εγκεκριμένες συνθήκες.
Οι πακιστανικές αρχές διερευνούν την αιτία της μόλυνσης. Πιθανές αιτίες περιλαμβάνουν ανεπαρκή αποστείρωση, μολυσμένα φιαλίδια, μη αποστειρωμένες σύριγγες και αποκλίσεις από τις τυπικές διαδικασίες λειτουργίας κατά τη χορήγηση.
Ταυτόχρονα, η πακιστανική κυβέρνηση ζήτησε την ανάκληση 3 παρτίδων Avastin 100mg/ml (H352B11, B7266B07, B7266B20) της Roche και όλων των φαρμάκων που προμηθεύτηκε η Genius Pharmaceutical Service.
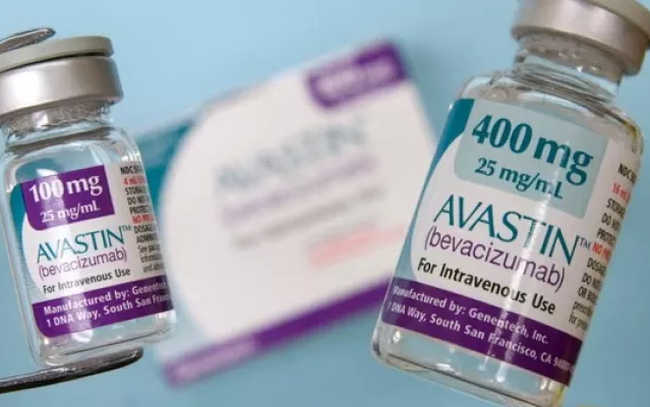
(Εικονογράφηση: 24 News HD).
Στο Βιετνάμ, στο φάρμακο Avastin (δραστικό συστατικό Bevacizumab) έχουν χορηγηθεί 4 πιστοποιητικά κυκλοφορίας, τα οποία εξακολουθούν να ισχύουν. Συμπεριλαμβανομένων:
Μπεβασιζουμάμπη 100mg/4ml (κουτί με 1 φιαλίδιο x 4ml· αριθμός καταχώρισης: 400410250123 (QLSP-1118-18)· κατασκευαστής: Roche Diagnostics GmbH, Γερμανία).
Μπεβασιζουμάμπη 400mg/16ml (κουτί με 1 φιαλίδιο x 16ml: αριθμός καταχώρισης: 400410250223 (QLSP-1119-18)· κατασκευαστής: Roche Diagnostics GmbH, Γερμανία).
Μπεβασιζουμάμπη 100mg/4ml (κουτί με 1 φιαλίδιο x 16ml· αριθμός καταχώρισης: QLSP-1010-17· κατασκευαστής: F. Hoffmann-La Roche Ltd., Ελβετία).
Μπεβασιζουμάμπη 400mg/16ml (Κουτί με 1 φιαλίδιο x 16ml· αριθμός καταχώρισης: QLSP-1011-17· κατασκευαστής: F. Hoffmann-La Roche Ltd., Ελβετία).
Το Avastin έχει άδεια κυκλοφορίας στο Βιετνάμ για τη θεραπεία ορισμένων μορφών καρκίνου, συμπεριλαμβανομένου του μεταστατικού καρκίνου του παχέος εντέρου, του προχωρημένου, μεταστατικού ή υποτροπιάζοντος μη μικροκυτταρικού καρκίνου του πνεύμονα, του προχωρημένου ή/και μεταστατικού νεφρικού καρκινώματος, του γλοιοβλαστώματος/κακοήθους γλοιώματος (στάδιο IV κατά ΠΟΥ), του επιθηλιακού καρκίνου των ωοθηκών, του καρκίνου των σαλπίγγων και του πρωτοπαθούς περιτοναίου.
Εκτός από τις γενικές προειδοποιήσεις, το εγκεκριμένο από τον FDA ένθετο συσκευασίας περιλαμβάνει μια προειδοποίηση σχετικά με το «όχι για ενδοϋαλώδη χρήση».
Συγκεκριμένα, το φάρμακο μπορεί να προκαλέσει οπτικές διαταραχές και έχουν αναφερθεί μεμονωμένες περιπτώσεις και ομάδες σοβαρών οφθαλμικών ανεπιθύμητων ενεργειών μετά από ενδοϋαλώδη ένεση, μια μη εγκεκριμένη οδό χορήγησης με μείγματα Avastin από φιαλίδια που προορίζονται για ενδοφλέβια έγχυση σε ασθενείς με καρκίνο.
Αυτές οι αντιδράσεις περιλαμβάνουν ενδοφθάλμια λοίμωξη, ενδοφθαλμίτιδα, ραγοειδίτιδα, αποκόλληση αμφιβληστροειδούς, ρήξη μελάγχρουν επιθηλίου του αμφιβληστροειδούς, γλαύκωμα, ενδοφθάλμια αιμορραγία… Ορισμένα από αυτά τα συμβάντα έχουν οδηγήσει σε ποικίλους βαθμούς απώλειας οπτικού πεδίου, συμπεριλαμβανομένης της μόνιμης τύφλωσης .
[διαφήμιση_2]
Πηγή



![[Φωτογραφία] Ο Πρόεδρος Λουόνγκ Κουόνγκ δέχεται τον Υπουργό Πολέμου των ΗΠΑ Πιτ Χέγκεθ](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/02/1762089839868_ndo_br_1-jpg.webp)



![[Φωτογραφία] Λαμ Ντονγκ: Εικόνες ζημιών μετά από ύποπτη έκρηξη λίμνης στο Τούι Φονγκ](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/02/1762078736805_8e7f5424f473782d2162-5118-jpg.webp)






































































































Σχόλιο (0)