最近、ベトナム保健省がペンブロリアと呼ばれる抗がん剤の流通登録証明書をベトナムで発行したというダン・トリ新聞のニュースが世間から特に注目を集めている。
具体的には、ベトナム保健省医薬品管理局が10月31日に発行した決定第628/QD-QLD号に基づき、ペンブロリア医薬品にはベトナム国内で3年間有効な流通登録証明書が付与されます。
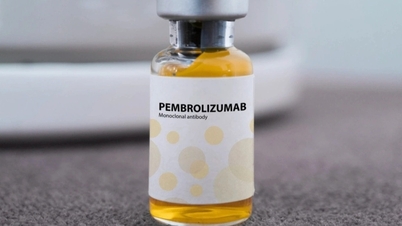
ペンブロリア医薬品の主な有効成分はペンブロリズマブで、含有量は 100 mg/4 ml です。PK-137 有限責任会社 (ロシア) によって製造され、点滴用の濃縮溶液の形で製造され、製造日から 24 か月の有効期限があります。

ペンブロリア薬の主な有効成分はペンブロリズマブです(写真:incentra)。
上記の形態に加えて、流通登録施設からの情報によると、ペンブロリアは透明からわずかに不透明、無色から薄茶色の溶液の形態でも調製されます。
ペンブロリアはどのような種類の癌に適応しますか?
登録機関の使用説明書によると、ペンブロリアは多くの種類の癌に適応があるとされています。
これらは、黒色腫、非小細胞肺がん、頭頸部の扁平上皮がん、古典的ホジキンリンパ腫、尿路上皮がん、食道がん、大腸がん、大腸以外のがん、子宮頸がんおよび子宮内膜がん、腎細胞がん、トリプルネガティブ乳がん、胃または胃食道接合部の腺がん、および胆管がんである。
がんの種類と病気の進行段階(初期または転移)に応じて、ペンブロリアはさまざまな年齢で処方され、単独療法として、または化学療法や他の薬剤と組み合わせて使用されます。
この薬は外来および入院の両方で使用されます。治療は経験豊富な腫瘍専門医によって開始および監督される必要があります。
上記の薬剤を処方されるためには、患者はPD-L1検査(がん細胞の表面にあるPD-L1タンパク質の量を測定する免疫組織化学検査)を実施し、マイクロサテライト不安定性(MSI)またはミスマッチ修復(MMR)欠損の腫瘍状態を判断する検査を実施する必要があります。
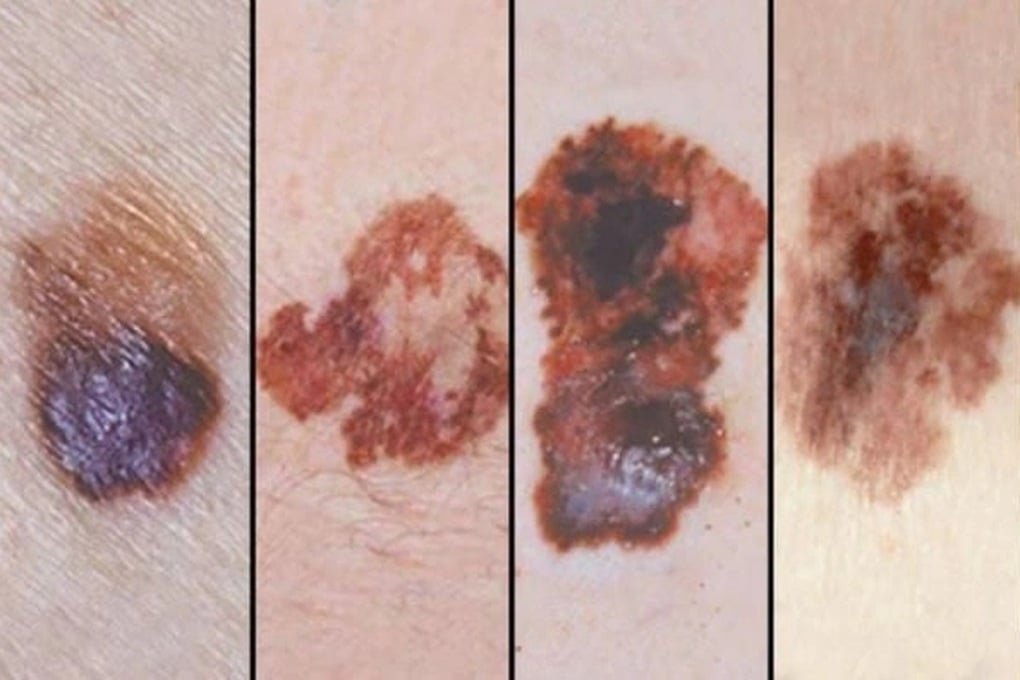
悪性黒色腫はペンブロリズマブで治療できる疾患の一つです(写真:BV)。
使用上の注意
投与量に関しては、成人に対するペンブロリズマブの推奨投与量は、静脈内注入として投与される場合、3週間ごとに200mg、または6週間ごとに400mgです。
3 歳以上の小児患者 (古典的ホジキンリンパ腫) または 12 歳以上の患者 (黒色腫) における単剤療法としてのペンブロリズマブの推奨用量は、体重 1 kg あたり 2 mg (最大 200 mg) を 3 週間ごとに静脈内注入で投与することです。
併用に関しては、製品の特性と併用療法によって異なります。
がんの種類に応じて、病気の進行または許容できない毒性の証拠が現れるまで、患者はペンブロリズマブ治療を受けることが推奨されます。

チョーライ病院で治療を受ける癌患者たち(写真:ホアン・レ)。
特定の癌(メラノーマ、非小細胞肺癌、腎細胞癌など)の補助療法では、ペムブロリズマブは、疾患の再発、許容できない毒性が現れるまで、または最長 1 年間まで、製造元によって推奨されています。
治療の適応症に加えて、患者はペンブロリアを使用する際に免疫関連の副作用にも注意し、適切な調整を行ったり、一時的に使用を中止したり、無期限に中止したりする必要があります。
具体的には、患者は肺炎(グレード 2 ~ 3)、大腸炎(グレード 2 ~ 3)、腎炎、内分泌疾患、肝炎、重度の皮下反応などの症状を経験する可能性があります...
患者が心筋炎、脳炎、ギランバレー症候群(急性多発神経障害)、または重度の注射後反応(グレード 3 ~ 4)を発症した場合、この薬剤による治療は永久に中止する必要があります。
さらに、18歳未満の患者におけるペムブロリズマブの安全性と有効性は確立されていません(メラノーマおよび古典的ホジキンリンパ腫の小児患者を除く)。また、本剤は急速静脈内注射や静脈内ボーラス注射ではなく、30分かけて静脈内投与することが推奨されます。
臨床研究を実施するための循環登録の付与
ベトナム保健省医薬品管理局は、10月31日に発行された決定第628/QD-QLD号の第2条第5項(製造施設および医薬品登録施設の責任について)において、本決定の付録1の医薬品(ペンブロリア)については、流通登録証明書の交付を受けた後、企業は定期的に臨床研究の実施状況を更新し、第3相免疫原性をモニタリングし、研究期間の終了時に第3相免疫原性モニタリングデータを変更、補足、更新するための書類を提出しなければならないと規定した。
医薬品管理局の情報によると、ペンブロリアは、製薬会社MSD(米国)のオリジナルの生物学的製剤に基づいて製造されたモノクローナル抗体です。2017年以降、ペンブロリズマブを主成分とする別の薬剤であるキイトルーダがベトナムで流通許可されています。
出典: https://dantri.com.vn/suc-khoe/thuoc-pembroria-cua-nga-duoc-chi-dinh-cho-cac-loai-ung-thu-gi-20251111231728560.htm


































































































![ドンナイ省一村一品制への移行:[第3条] 観光と一村一品制製品の消費の連携](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/11/10/1762739199309_1324-2740-7_n-162543_981.jpeg)








コメント (0)