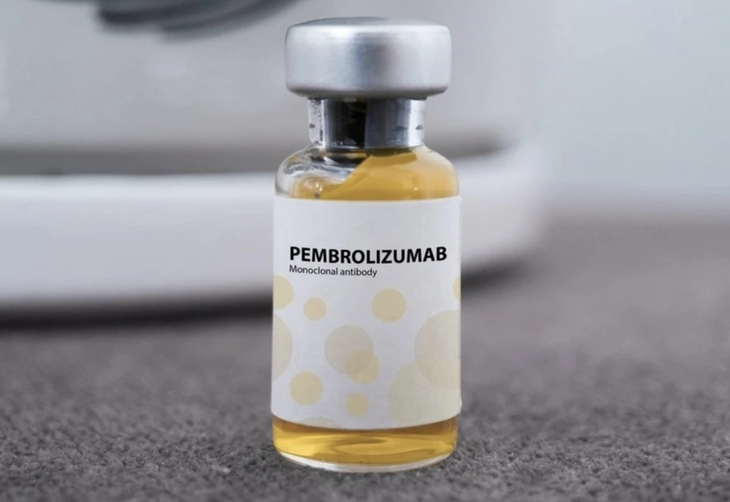
Lek na Pembrorię produkowany w Rosji - Zdjęcie: Incentra
Wietnamski Urząd ds. Leków (Leków) i Ministerstwo Zdrowia wydały właśnie certyfikaty rejestracji do obrotu w Wietnamie dla 14 szczepionek i produktów biologicznych. Wśród nich znajduje się lek Pembroria, którego głównym składnikiem aktywnym jest pembrolizumab o stężeniu 100 mg/4 ml, produkowany przez spółkę z ograniczoną odpowiedzialnością „PK-137” (Rosja) i zakład w Zjednoczonych Emiratach Arabskich zarejestrowany do obrotu w Wietnamie.
Od wczoraj, 11 listopada, wiele osób interesuje się tą informacją, ponieważ pojawiły się informacje, że Pembroria właśnie weszła do Wietnamu w fazie 3 badań klinicznych, nie jest jeszcze oficjalnym produktem, a jej dystrybucja przebiega w pośpiechu. Inne źródła twierdzą, że produkt ten jest zupełnie nowy i „niesie nadzieję wielu pacjentom”, nazywając go nawet „szczepionką przeciwnowotworową”.
Przedstawiciel Departamentu Administracji Leków, rozmawiając z prasą dziś rano, 12 listopada, stwierdził, że oba powyższe źródła informacji są nieprawdziwe.
Według tej osoby, zanim przyznano mu numer rejestracyjny umożliwiający dopuszczenie do obrotu w Wietnamie, profil produktu został oceniony przez eksperta farmakologii z Uniwersytetu Medycznego w Hanoi . Potwierdził on, że produkt w pełni spełnia wymagania dotyczące skuteczności i immunogenności podobne do oryginalnego leku.
Ten produkt ma postać przeciwciała monoklonalnego i przeszedł badania kliniczne w fazach 1, 2 i 3, a ostatnia faza 3 zakończyła się w styczniu 2024 r. Jednak rejestrując produkt w Wietnamie, rada nałożyła surowsze wymogi, aby kontynuować okresową ocenę immunogenności, skuteczności i zarządzania ryzykiem co 3 miesiące...
„To wyższe niż zwykle wymaganie, nie chodzi o produkt, który nie przeszedł badań klinicznych, ale został zarejestrowany do obrotu, jak niektórzy źle rozumieją. Problemem jest również to, że jest to produkt leczniczy, a nie szczepionka” – powiedział przedstawiciel Departamentu Administracji Leków.
Jednak to przeciwciało monoklonalne nie jest nowym wynalazkiem, ponieważ pojawiło się po raz pierwszy w Wietnamie, ale ten sam typ przeciwciała monoklonalnego (leku generycznego) był w obiegu w Wietnamie od wielu lat (od 2017 roku). Agencja ds. Żywności i Leków (FDA) wydała również zezwolenia na obrót 99 rodzajami leków i przeciwciał monoklonalnych stosowanych w leczeniu raka, w tym Pembrorią, do 11 listopada.
Podobnie jak podobne produkty, Pembroria jest wskazana w leczeniu czerniaka, niedrobnokomórkowego raka płuc, klasycznego chłoniaka Hodgkina, raka urotelialnego, raka przełyku, raka jelita grubego, raka szyjki macicy, potrójnie ujemnego raka piersi, gruczolakoraka żołądka, raka dróg żółciowych...
Leczenie powinno być przepisane i nadzorowane przez doświadczonego specjalistę. W zależności od okoliczności, Pembroria może być stosowana w leczeniu dorosłych lub młodzieży w wieku 12 lat i starszych.
Co należy wiedzieć o przeciwciałach monoklonalnych przeciwko Pembrorii
Lek jest produkowany przez firmę Biocad Company (Rosja), zarejestrowaną do obrotu w Wietnamie przez firmę z siedzibą w Zjednoczonych Emiratach Arabskich. Rejestracja pozwala na import, dystrybucję i szerokie stosowanie leku, podobnie jak innych leków, ponieważ nie należy on do specjalnej ani ograniczonej grupy leków.
Wcześniej, w 2017 roku, lek Keytruda firmy MSD Group (USA), jest to lek generyczny, którego substancją czynną jest pembrolizumab i został zarejestrowany w Wietnamie.
Zarówno Keytruda, jak i Pembroria zawierają substancję czynną pembrolizumab, przeciwciało monoklonalne, które pomaga układowi odpornościowemu organizmu rozpoznawać i atakować komórki nowotworowe.
Posiadanie większej liczby licencjonowanych leków zwiększa możliwości pacjentów onkologicznych w Wietnamie w zakresie immunoterapii, w kontekście rosnącego zapotrzebowania na leczenie raka. Szczególnie jeśli chodzi o cenę produktu, ekspert stwierdził, że cena tego produktu z pewnością będzie niższa niż oryginalnego leku, chociaż właściciel oryginalnego leku również ma plan obniżenia jego ceny.
W Rosji Pembroria jest dopuszczona do obrotu od kwietnia 2022 r.
Źródło: https://tuoitre.vn/nga-cancer-treatment-drug-is-approved-or-is-it-just-a-sang-treatment-test-or-is-it-just-a-sang-test-in-viet-nam-20251112120926097.htm




![[Zdjęcie] Premier Pham Minh Chinh bierze udział w konferencji podsumowującej rok rozmieszczania sił zbrojnych w celu ochrony bezpieczeństwa i porządku na szczeblu lokalnym.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/12/1762957553775_dsc-2379-jpg.webp)
![[Zdjęcie] Autostrady przechodzące przez Dong Nai](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/12/1762940149627_ndo_br_1-resize-5756-jpg.webp)




























































































![Przejście Dong Nai OCOP: [Artykuł 3] Powiązanie turystyki z konsumpcją produktów OCOP](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/11/10/1762739199309_1324-2740-7_n-162543_981.jpeg)







Komentarz (0)