Recentemente, a notícia de que o Ministério da Saúde concedeu um certificado de registro de circulação no Vietnã para um medicamento anticancerígeno chamado Pembroria, publicada pelo jornal Dan Tri , recebeu atenção especial do público.
Especificamente, de acordo com a Decisão nº 628/QD-QLD, de 31 de outubro, emitida pela Administração de Medicamentos do Vietnã, Ministério da Saúde , o medicamento Pembroria recebeu um certificado de registro de circulação no Vietnã com validade de 3 anos.
O medicamento Pembroria tem como principal princípio ativo o pembrolizumabe, na concentração de 100 mg/4 ml, produzido pela empresa de responsabilidade limitada "PK-137" (Rússia), preparado na forma de solução concentrada para infusão, com prazo de validade de 24 meses a partir da data de fabricação.

O medicamento Pembroria tem como principal ingrediente ativo o pembrolizumabe (Foto: incentra).
Além da forma acima, de acordo com informações do órgão de registro de circulação, a Pembroria também é preparada na forma de uma solução transparente a ligeiramente opaca, incolor a marrom claro.
Para que tipos de câncer Pembroria é indicado?
De acordo com as instruções de uso da agência reguladora, Pembroria é indicado para diversos tipos de câncer.
São eles: melanoma; câncer de pulmão de células não pequenas; carcinoma de células escamosas da cabeça e pescoço; linfoma de Hodgkin clássico; câncer urotelial; câncer de esôfago; câncer colorretal; câncer não colorretal; câncer cervical e endometrial; carcinoma de células renais; câncer de mama triplo-negativo; adenocarcinoma do estômago ou da junção gastroesofágica; e colangiocarcinoma.
Dependendo do tipo de câncer e do estágio da doença (inicial ou metastático), o Pembromia será prescrito em diferentes faixas etárias, utilizado como monoterapia ou em combinação com quimioterapia e outros medicamentos.
Este medicamento é utilizado tanto em regime ambulatorial quanto hospitalar. O tratamento deve ser iniciado e supervisionado por oncologistas experientes.
Para que o medicamento acima seja prescrito, os pacientes devem realizar o teste PD-L1 (teste imuno-histoquímico para medir a quantidade da proteína PD-L1 na superfície das células cancerígenas), um teste para determinar o status do tumor em relação à instabilidade de microssatélites (MSI) ou deficiência no reparo de erros de pareamento (MMR).
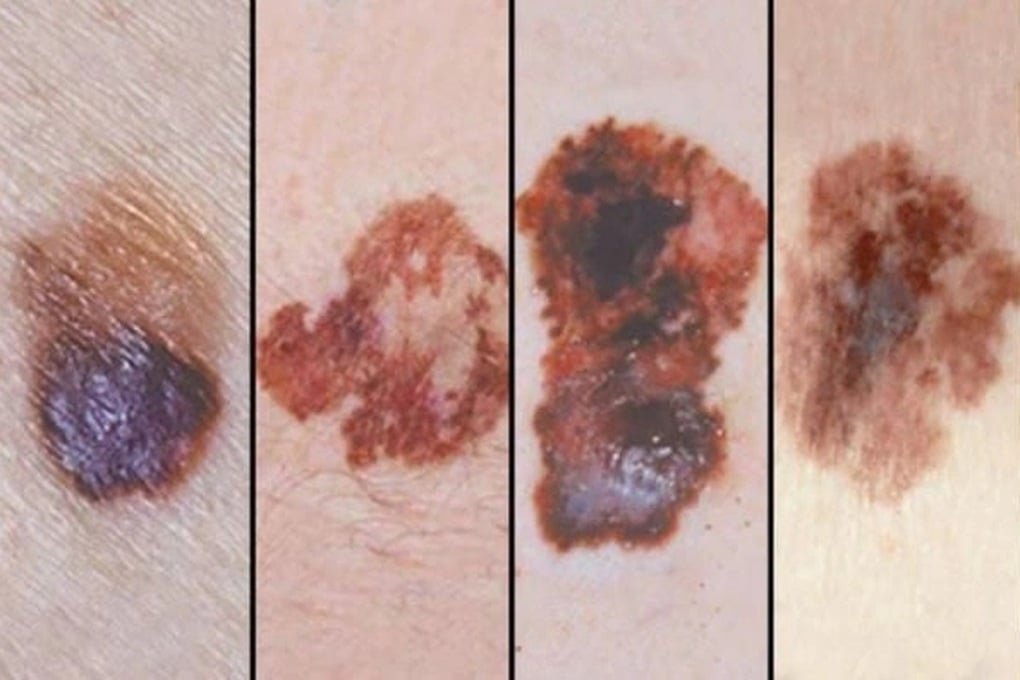
O melanoma maligno é uma das doenças que podem ser tratadas com Pembrolizumab (Foto: BV).
Observações ao usar
Em relação à dosagem, a dose recomendada de Pembrolizumab em adultos é de 200 mg a cada 3 semanas ou 400 mg a cada 6 semanas, administrada por infusão intravenosa.
A dose recomendada de pembrolizumabe como monoterapia em pacientes pediátricos com 3 anos de idade ou mais (com linfoma de Hodgkin clássico) ou pacientes com 12 anos de idade ou mais (com melanoma) é de 2 mg/kg de peso corporal (máximo de 200 mg), administrada por infusão intravenosa a cada 3 semanas.
Em relação ao uso combinado, isso dependerá das propriedades do produto e das terapias concomitantes.
Dependendo do tipo de câncer, recomenda-se que os pacientes recebam tratamento com Pembrolizumabe até que haja evidência de progressão da doença ou toxicidade inaceitável.

Pacientes com câncer recebendo tratamento no Hospital Cho Ray (Foto: Hoang Le).
No tratamento adjuvante de certos tipos de câncer (como melanoma, carcinoma de pulmão de não pequenas células ou carcinoma de células renais), o pembrolizumabe é recomendado pelo fabricante até a recorrência da doença, toxicidade inaceitável ou por até 1 ano…
Além das indicações de tratamento, os pacientes também precisam estar atentos a reações adversas relacionadas ao sistema imunológico ao usar Pembroria, para que possam fazer os ajustes necessários, interromper temporariamente o uso ou suspendê-lo indefinidamente.
Especificamente, os pacientes podem apresentar quadros clínicos como pneumonia (grau 2-3), colite (grau 2-3), nefrite, doenças endócrinas, hepatite, reações subcutâneas graves...
Caso o paciente desenvolva miocardite, encefalite, síndrome de Guillain-Barré (polineuropatia aguda) ou reações pós-injeção graves (grau 3-4), o tratamento com este medicamento deve ser interrompido permanentemente.
Além disso, a segurança e a eficácia do pembrolizumabe em pessoas com menos de 18 anos de idade não foram estabelecidas (exceto em pacientes pediátricos com melanoma e linfoma de Hodgkin clássico). Recomenda-se também que o medicamento seja administrado por via intravenosa durante 30 minutos, e não por injeção intravenosa rápida ou em bolus.
Concessão de registro de circulação para a realização de pesquisas clínicas
Na Seção 5, Artigo 2 (sobre as responsabilidades da unidade de fabricação e da unidade de registro de medicamentos) da Decisão nº 628/QD-QLD, emitida em 31 de outubro, a Administração de Medicamentos do Vietnã, Ministério da Saúde, declarou que, com relação ao medicamento nº 1 no Anexo desta Decisão (Pembroria), após a concessão do certificado de registro de circulação, a empresa deve atualizar periodicamente o progresso da implementação da pesquisa clínica, monitorar a imunogenicidade da fase III e submeter documentos para alterar, complementar e atualizar os dados de monitoramento da imunogenicidade da fase III ao término do período de pesquisa.
Segundo informações da Agência Nacional de Vigilância Sanitária (ANVISA), o Pembroria é um anticorpo monoclonal produzido a partir do produto biológico de referência original da empresa farmacêutica MSD (EUA). Desde 2017, o Keytruda, outro medicamento com o princípio ativo pembrolizumabe, está licenciado para comercialização no Vietnã.
Fonte: https://dantri.com.vn/suc-khoe/thuoc-pembroria-cua-nga-duoc-chi-dinh-cho-cac-loai-ung-thu-gi-20251111231728560.htm


![[Foto] O primeiro-ministro Pham Minh Chinh recebe o ministro do Trabalho e Bem-Estar do Laos, Phosay Sayasone.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/11/1762872028311_dsc-2246-jpg.webp)






























































































![Transição OCOP de Dong Nai: [Artigo 3] Vinculando o turismo ao consumo de produtos OCOP](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/11/10/1762739199309_1324-2740-7_n-162543_981.jpeg)








Comentário (0)