일론 머스크의 뇌 칩 이식 회사인 뉴럴링크는 최초의 인체 임상 시험에 대해 미국 식품의약국(FDA)의 승인을 받았다고 주장합니다.

2016년에 설립된 뉴럴링크는 성명을 통해 이번 조치가 "언젠가는 우리 기술이 많은 사람들에게 도움이 될 수 있는 첫걸음"이라고 밝혔습니다.
머스크의 회사는 트위터를 통해 "임상 시험을 위한 모집은 아직 시작되지 않았습니다."라고 덧붙이며, 앞으로 며칠 안에 더 많은 정보를 제공할 것을 약속했습니다.
억만장자 기업가 일론 머스크는 지난 12월 뉴럴링크가 올해 상반기에 규제 승인을 받을 것이라고 예측했습니다. 그의 예측은 맞았지만, 승인 절차는 쉽지 않았고 작년에 거부되었습니다.
뉴럴링크는 수년간 자사 제품에 대한 기대감을 높여 왔습니다. 2020년 머스크는 발표에서 자사의 칩이 마비나 불면증 같은 질병을 치료할 수 있을 것이라고 주장했습니다. 그는 뉴럴링크 칩이 사용자에게 "초인적인" 시력을 제공할 수도 있다고 덧붙였습니다. 당시 회사는 돼지에 최초로 뇌 칩을 이식하는 시연을 선보였습니다.

2021년, 뉴럴링크(Neuralink) 관계자들이 역대 가장 화제가 된 프레젠테이션 중 하나를 진행했습니다. 페이저(Pager)라는 이름의 원숭이가 TV 앞에 앉아 화면에 나오는 게임, 즉 퐁(Pong)을 집중해서 지켜보았습니다. 이 영장류는 뇌의 양쪽 반구에 이식된 25센트 동전 크기의 반도체 소자 덕분에 눈만으로 움직임을 제어했습니다.
일론 머스크는 2019년부터 FDA에 인체 임상시험 승인을 요청하고 있다고 거듭 주장해 왔습니다. 하지만 회사 관계자들은 2022년까지 규제 당국에 승인을 신청하지 않을 예정입니다. 로이터 통신에 따르면, 뉴럴링크의 첫 번째 승인 신청은 제출 직후 FDA에 의해 거부되었습니다. FDA는 "기기의 리튬 배터리, 이식된 와이어가 뇌로 이동할 위험, 그리고 뇌 조직을 손상시키지 않고 기기를 안전하게 제거하는 어려움"에 대한 우려를 제기한 것으로 알려졌습니다.
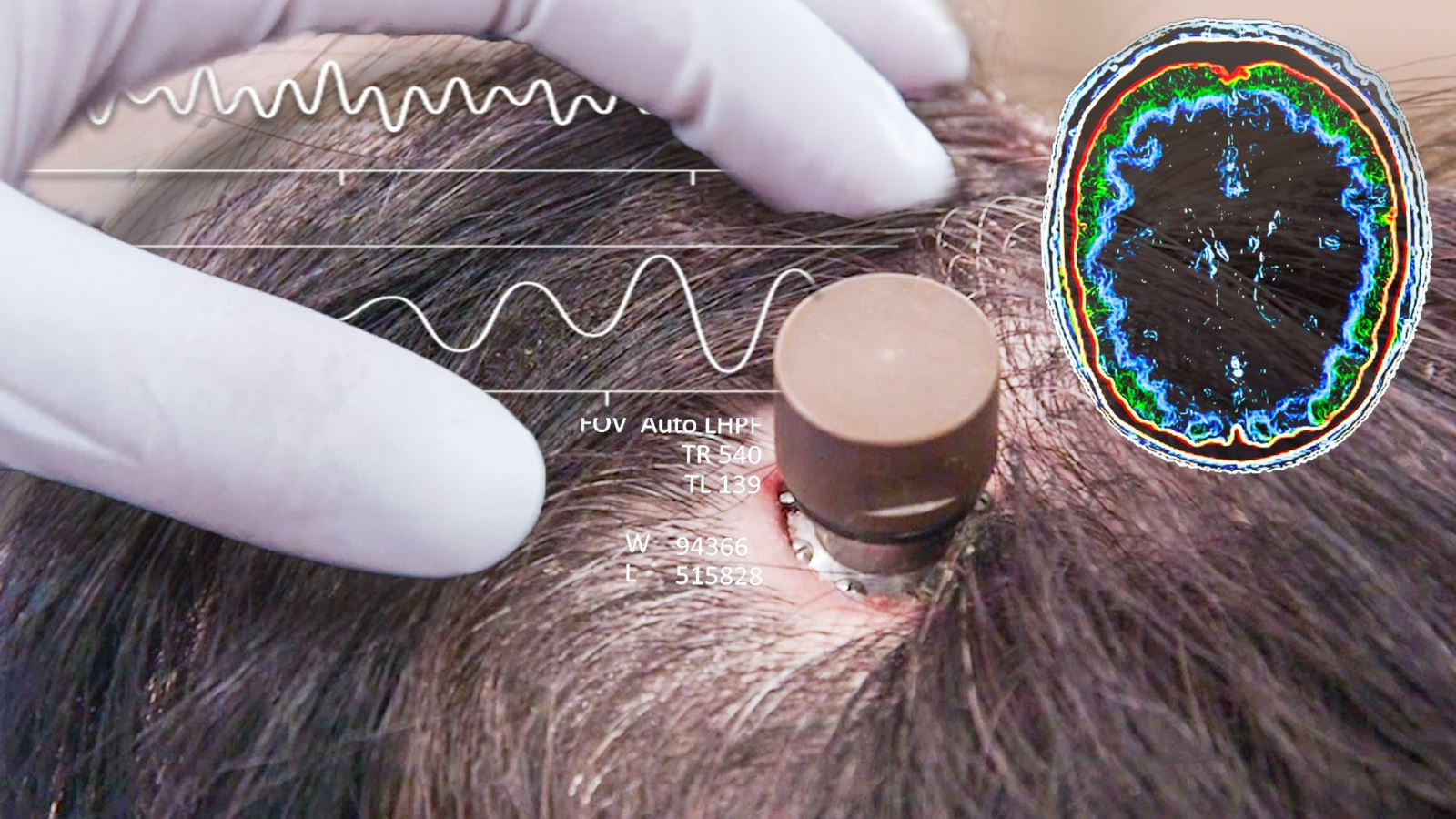
3월 로이터 통신 특별 보도에 따르면, 일부 뉴럴링크 직원들은 뉴럴링크가 FDA가 제기한 문제를 신속하게 해결할 수 있을지에 대한 의구심을 표명했습니다. 미국 국립 보건원 (NIH) 신경공학 프로그램 전 책임자였던 킵 루드윅은 로이터 통신에 "뉴럴링크는 이 제품을 신속하게 시장에 출시하는 데 필요한 사고방식과 경험을 갖추고 있지 않은 것 같다"고 말했습니다.
뉴럴링크는 뇌 이식에 대한 인체 임상 시험을 준비하는 유일한 회사가 아닙니다. 주요 경쟁사 중 하나인 파라드로믹스(Paradromics) 또한 FDA 승인을 추진하고 있습니다.
2015년 설립된 텍사스주 오스틴에 본사를 둔 신경기술 스타트업 파라드로믹스는 이식형 기기 개발에 큰 진전을 이루었습니다. 코넥서스 다이렉트 데이터(Connexus Direct Data)라는 이름의 이 제품은 말이나 타이핑 능력을 잃은 환자를 돕는 의사소통 기기로 알려져 있습니다. 이 기술은 매우 유망하여 FDA는 파라드로믹스에 "혁신 기기(Breakthrough Device)" 지정을 부여했습니다. 이 프로그램은 환자의 치료 및 진단에 도움이 될 수 있다는 이유로 32건의 신청 건에 대해 신속 승인을 허용하는 프로그램입니다.
신생 뇌-컴퓨터 인터페이스(BCI) 산업에 진출하는 또 다른 회사는 Synchron입니다.
이 회사들은 크기, 무게, 성능 면에서 다양한 반도체 제품을 제공하며, 이를 인간의 뇌에 이식하는 수술 방법도 다양합니다. 하지만 이들은 모두 수백만 명의 사람들에게 가져다줄 수 있는 미래의 혜택에 대해 낙관적입니다.
baotintuc.vn에 따르면
[광고_2]
소스 링크



































































































댓글 (0)