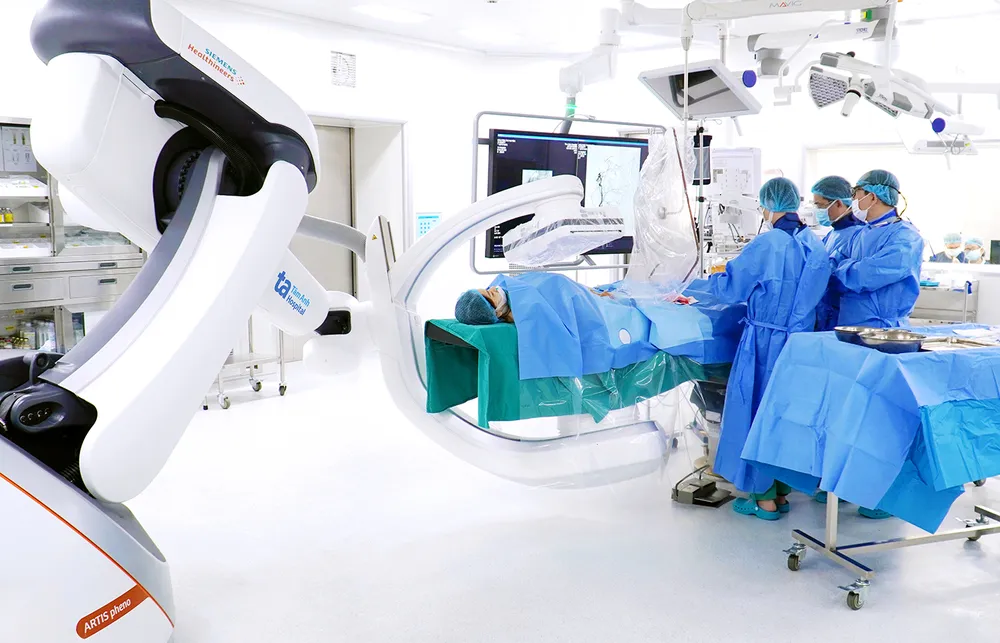
Costuri mai mici, mai multe oportunități de tratament.
La sfârșitul lunii decembrie 2024, Institutul de Cercetare Tam Anh a lansat proiectul VISTA-1 privind imunoterapia orală pentru tratamentul cancerului în Vietnam. După aproape șase luni de implementare a studiului clinic, opt pacienți cu cancer colorectal în stadiu terminal tratați conform protocolului de cercetare nu au prezentat inițial efecte secundare semnificative legate de medicamentul studiat și au demonstrat rezultate promițătoare.
Dl. M. (50 de ani), care a fost prima persoană care a testat medicamentul în cadrul acestui proiect și suferea de cancer colorectal cu metastaze la ficat, a declarat că a urmat diverse scheme de tratament, cum ar fi chimioterapie și terapie țintită, dar fără succes. În ianuarie 2025, s-a înregistrat pentru a participa la studiu și a fost considerat eligibil. „Credeam că nu am alte opțiuni, dar datorită acestei oportunități de a participa la studiu, mă simt ușurat și am mai multă speranță”, a împărtășit dl. M.
Potrivit Dr. Vu Huu Khiem, șeful Departamentului de Oncologie de la Spitalul General Tam Anh din Hanoi , pacienții care au participat la studiu au fost monitorizați îndeaproape pentru siguranță și răspuns la medicamentul de cercetare. Echipa de cercetare nu a înregistrat niciun simptom neobișnuit legat de medicamentul de cercetare la pacienții care l-au utilizat în ultimele trei luni.
„Pentru pacienții cu cancer colorectal avansat care nu mai răspund la schemele de tratament actuale, fiecare îmbunătățire a timpului de supraviețuire în timpul participării lor la acest studiu este de o importanță deosebită. Noi și pacienții am intrat acum în a patra lună a acestei cercetări”, a declarat Dr. Vu Huu Khiem.
La Spitalul Oncologic din orașul Ho Chi Minh, Dr. Phan Tan Thuan, șeful Unității de Studii Clinice, a declarat că unitatea desfășoară în prezent 37 de studii clinice, majoritatea în colaborare cu companii farmaceutice multinaționale (Pharma). De asemenea, spitalul colaborează proactiv cu centrele regionale de cancer pentru a efectua cercetări independente cu valoare academică și aplicații practice. Spitalul utilizează adesea medicamente de nouă generație pentru compararea cu protocoalele standard de tratament. Multe dintre aceste medicamente nu sunt încă disponibile în Vietnam și sunt foarte scumpe, unele costând până la 300 de milioane de VND per ciclu de tratament (3-4 săptămâni). Pacienții care participă la studii primesc medicamentele gratuit, indiferent de ramura specifică de tratament.
„Pe lângă faptul că ajută pacienții să acceseze tratamente moderne mai devreme, aceste studii permit, de asemenea, profesioniștilor locali să stăpânească datele și să evalueze eficacitatea medicamentelor asupra populației vietnameze. Acest lucru scurtează timpul necesar pentru a lansa pe piață medicamente noi. Multe medicamente de nouă generație sunt foarte scumpe. Aici, oferim acces gratuit la medicamente de nouă generație pentru toți pacienții care participă la studiu. Atunci când cercetarea are succes, aceasta poate scurta timpul necesar pentru a lansa pe piață medicamente noi”, a explicat Dr. Phan Tan Thuan.
„Studiile clinice recente au ajutat industria medicală să acceseze rapid tratamente moderne, de la chimioterapia tradițională la imunoterapie și terapii țintite. Aceste progrese nu numai că ajută la prelungirea vieții, dar și la îmbunătățirea calității vieții pacienților, extinzând în același timp accesul la medicamente noi la costuri mai mici pentru pacienți și sistemul de sănătate.”
Ministrul adjunct al Sănătății Nguyen Thi Lien Huong
Mult potențial, dar lipsă de mecanisme.
Potrivit profesorului Guy Thwaites, directorul Unității de Cercetare Clinică de la Universitatea Oxford, Vietnamul este lider în studiile clinice privind medicamentele împotriva malariei încă din 1991, beneficiind pentru milioane de pacienți la nivel global. Cu o populație de aproximativ 100 de milioane, Vietnamul oferă un grup divers de pacienți, ideal pentru studiile clinice. O rată medie de creștere a PIB-ului de 6-7% pe an, coroborată cu o clasă de mijloc în creștere, sporește și mai mult atractivitatea Vietnamului atât pentru donatorii interni, cât și pentru cei internaționali. În ciuda potențialului său mare, piața studiilor clinice din Vietnam se confruntă încă cu mai multe bariere care îi încetinesc dezvoltarea și creează o lipsă de sincronizare. Timpul de aprobare pentru un studiu clinic în Vietnam poate fi de până la 160 de zile - cel mai lung din Asia, în timp ce timpul mediu în alte țări este de aproximativ 75 de zile. În plus, Vietnamul este mult în urma multor țări din regiune, cum ar fi Singapore (18 zile), Indonezia (20 de zile), Japonia (31 de zile)... Acest interval de timp afectează atractivitatea pieței vietnameze pentru sponsorii cercetării.
În plus, studiile clinice necesită o colaborare strânsă între medici, asistente medicale, coordonatori de cercetare și manageri de date. Cu toate acestea, Vietnamul duce în prezent lipsă de o forță de muncă bine pregătită; se confruntă, de asemenea, cu dificultăți financiare și mecanisme de stimulare inadecvate. Un studiu clinic de fază 3 poate costa între 10 și 20 de milioane de dolari. Între timp, mulți investitori au raportat că Vietnamul nu dispune de stimulente fiscale, finanțare pentru cercetare sau mecanisme de cofinanțare similare cu cele din Singapore și Coreea de Sud. Plata fondurilor este adesea întârziată din cauza procedurilor administrative, afectând progresul studiilor și reducând competitivitatea în comparație cu alte țări din regiune.
Pentru a dezvolta sectorul studiilor clinice în Vietnam, Dr. Phan Tan Thuan sugerează simplificarea procedurilor de aprobare printr-un sistem online centralizat, pentru a scurta actualul proces complex de aprobare. În plus, ar trebui implementate înregistrarea online prin intermediul unui portal în limba engleză și documentația bilingvă pentru a eficientiza procesul pentru donatorii internaționali. Pentru a concura cu alte țări din regiune, ar trebui dezvoltate politici preferențiale, cum ar fi scutirile de taxe, finanțarea cercetării sau mecanisme de cofinanțare pentru costurile studiilor, similare programelor din Singapore și Thailanda.
„Vietnam ar trebui să promoveze modele de parteneriat public-privat în cercetarea studiilor clinice pentru a ajuta la partajarea riscurilor și la sporirea resurselor pentru dezvoltarea durabilă a industriei. Împreună cu aceasta, este nevoie de politici pentru investiții în infrastructură, crearea mai multor facilități de testare și extinderea programelor de formare specializată pentru personal prin cooperarea cu universități și organizații internaționale”, a sugerat Dr. Phan Tan Thuan.
Dl. LUKE TRELOAR, Șef al departamentului Infrastructură, Guvern și Sănătate la KPMG Vietnam: Dezvoltarea politicilor de stimulare
Procesul de aprobare a studiilor clinice în Vietnam implică mai mulți pași. În primul rând, obținerea aprobării la nivel local durează între 3 și 12 luni, în funcție de numărul și locația studiilor. În continuare, procesul de aprobare la Ministerul Sănătății durează în medie între 3 și 5 luni. În cele din urmă, obținerea unei licențe de import pentru medicament (pentru studiile clinice) durează în medie între 3 și 4 luni. Numărul de centre și studii clinice din Vietnam este prea mic în raport cu populația sa, riscând să rămână în urmă în cursa pentru a deveni un centru regional de cercetare clinică. Vietnamul are nevoie de politici de investiții în infrastructură, de construire a mai multor facilități de studiu și de extindere a programelor de formare specializată pentru personal prin cooperarea cu universități și organizații internaționale. Pentru a concura cu alte țări din regiune, trebuie să dezvolte politici de stimulare, cum ar fi scutiri de taxe, finanțarea cercetării sau mecanisme de cofinanțare pentru costurile studiilor, similare programelor din Singapore și Thailanda.
Dl. Nguyen Ngo Quang, Director al Departamentului de Știință, Tehnologie și Formare (Ministerul Sănătății): Standardizarea activităților studiilor clinice.
În perioada următoare, Ministerul Sănătății va continua să rafineze cadrul legal și să standardizeze activitățile studiilor clinice în conformitate cu standardele internaționale. Simultan, va consolida capacitatea Consiliului Național de Etică a Cercetării Biomedicale. În prezent, Ministerul Sănătății solicită feedback cu privire la un proiect de Circulară care detaliază reglementările privind studiile clinice medicamentoase. Această Circulară va specifica detaliile studiilor clinice medicamentoase, inclusiv principiile, standardele, procedurile și responsabilitățile legate de testarea medicamentelor pe voluntari pentru a evalua siguranța și eficacitatea medicamentelor, a identifica reacțiile adverse la medicamente (RAM) și a studia farmacocinetica medicamentelor. Conform proiectului de Circulară, principiile studiilor clinice medicamentoase trebuie să asigure rigoarea științifică, obiectivitatea, onestitatea, transparența și să protejeze drepturile participanților la cercetare.
MINH NAM - MINH KHA NG înregistrat
Sursă: https://www.sggp.org.vn/gian-nan-thu-nghiem-lam-sang-post802539.html



![[Foto] Secretarul general, președintele și soția sa își încep vizita de stat în Filipine.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2026/05/31/1780230559452_anh-man-hinh-2026-05-31-luc-19-28-11.png)
![[Fotografie] Admirați „capodoperă” de corali în mijlocul moștenirii vechi de milioane de ani a provinciei Dak Lak.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2026/05/31/1780221235105_anh-man-hinh-2026-05-31-luc-16-53-27.png)

![[Imagine] Poliția din Hanoi a fost încoronată oficial campioană a V-League 2025/2026](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2026/05/31/1780244769054_ndo_br_039d561b692be875b13a-jpg.webp)
![[Foto] Ceremonia solemnă de îmbăiere și procesiunea lui Buddha în Hue](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2026/05/31/1780228263543_1-jpg.webp)





















![[Video] Apus de soare la Laguna Lap An – Unde soarele apune peste plasele de pescuit](https://vphoto.vietnam.vn/thumb/340x192/vietnam/resource/IMAGE/2026/05/31/1780192137701_beach-landscape-sea-water-nature-grass-745871-pxhere-com.jpeg)








































![[Fotografie] Admirați „capodoperă” de corali în mijlocul moștenirii vechi de milioane de ani a provinciei Dak Lak.](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2026/05/31/1780221235105_anh-man-hinh-2026-05-31-luc-16-53-27.png)








































Comentariu (0)