সুইস রোশে ক্যান্সারের ওষুধ অ্যাভাস্টিনের দুই পরিবেশককে ইনজেকশন দেওয়ার পর ১২ জন ডায়াবেটিস রোগী অন্ধ হয়ে যাওয়ার পর পাকিস্তান তদন্ত করছে। অ্যাভাস্টিন ভিয়েতনামেও লাইসেন্সপ্রাপ্ত।
ভিয়েতনামে, ২৭শে সেপ্টেম্বর পর্যন্ত, ভিয়েতনামের ঔষধ প্রশাসন ( স্বাস্থ্য মন্ত্রণালয় ) অ্যাভাস্টিন ব্যবহারের পর দৃষ্টিশক্তি হারানোর সাথে সম্পর্কিত অ্যাভাস্টিনের অবাঞ্ছিত পার্শ্বপ্রতিক্রিয়ার প্রতিফলনকারী কোনও প্রতিবেদন পায়নি।
ভিয়েতনামের ওষুধ প্রশাসন এফ. হফম্যান লা রোচে লিমিটেডের প্রতিনিধি অফিস থেকে এই ঘটনা সম্পর্কে একটি প্রতিবেদন পেয়েছে।
বিশেষ করে, পাকিস্তানে, অবৈধ সরবরাহকারী জিনিয়াস ফার্মাসিউটিক্যাল সার্ভিসের সরবরাহকৃত ইনজেকশন ব্যবহারের পর প্রায় ১২ জন রোগী তাদের দৃষ্টিশক্তি হারিয়ে ফেলেন। ওষুধটির লেবেল ছিল "Inj. Avastin 1.25mg/0.05ml", যার ফলে এটি একটি Roche পণ্য বলে ভুল ধারণা তৈরি হয়েছিল।
রোশের অ্যাভাস্টিন চোখের চিকিৎসায় ব্যবহারের জন্য অনুমোদিত নয়। জিনিয়াস ফার্মাসিউটিক্যাল সার্ভিস অস্বাস্থ্যকর এবং অননুমোদিত পরিস্থিতিতে ১.২৫ মিলিগ্রাম/০.৫ মিলি ডোজ সরবরাহ/পাতলা/পুনরায় প্যাকেজ করেছে।
পাকিস্তানি কর্তৃপক্ষ দূষণের কারণ তদন্ত করছে। সম্ভাব্য কারণগুলির মধ্যে রয়েছে অপর্যাপ্ত জীবাণুমুক্তকরণ, দূষিত শিশি, অজীর্ণ সিরিঞ্জ এবং বিতরণের সময় স্ট্যান্ডার্ড অপারেটিং পদ্ধতি থেকে বিচ্যুতি।
একই সময়ে, পাকিস্তান সরকার রোশের অ্যাভাস্টিন ১০০ মিলিগ্রাম/মিলি (H352B11, B7266B07, B7266B20) এর ৩টি ব্যাচ এবং জিনিয়াস ফার্মাসিউটিক্যাল সার্ভিস কর্তৃক সরবরাহিত সমস্ত ওষুধ প্রত্যাহারের অনুরোধ করেছে।
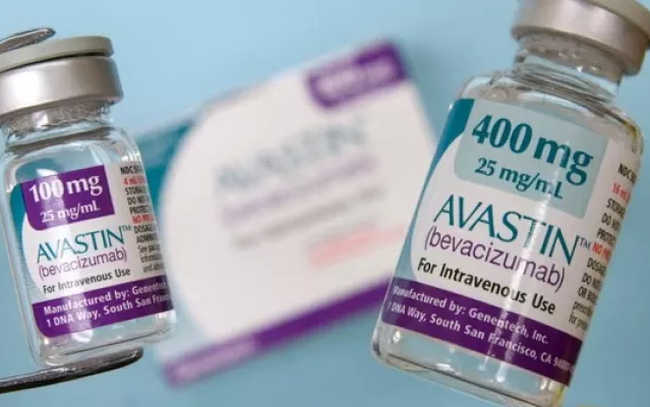
(চিত্র: ২৪ নিউজ এইচডি)।
ভিয়েতনামে, অ্যাভাস্টিন (সক্রিয় উপাদান বেভাসিজুমাব) নামক ওষুধটিকে ৪টি সার্কুলেশন নিবন্ধন শংসাপত্র প্রদান করা হয়েছে, যার সবকটি এখনও বৈধ। যার মধ্যে রয়েছে:
বেভাসিজুমাব ১০০ মিলিগ্রাম/৪ মিলি (১টি ভায়ালের বাক্স x ৪ মিলি; রেজিস্ট্রেশন নম্বর: ৪০০৪১০২৫০১২৩ (QLSP-১১১৮- ১৮); প্রস্তুতকারক: রোচে ডায়াগনস্টিকস জিএমবিএইচ, জার্মানি)।
বেভাসিজুমাব ৪০০ মিলিগ্রাম/১৬ মিলি (১টি ভায়ালের বাক্স x ১৬ মিলি: রেজিস্ট্রেশন নম্বর: ৪০০৪১০২৫০২২৩ (QLSP-১১৯- ১৮); প্রস্তুতকারক: রোচে ডায়াগনস্টিকস জিএমবিএইচ, জার্মানি)।
বেভাসিজুমাব ১০০ মিলিগ্রাম/৪ মিলি (১টি ভায়ালের বাক্স x ১৬ মিলি; নিবন্ধন নম্বর: QLSP-1010-17; প্রস্তুতকারক: এফ. হফম্যান-লা রোচে লিমিটেড, সুইজারল্যান্ড)।
বেভাসিজুমাব ৪০০ মিলিগ্রাম/১৬ মিলি (১টি ভায়ালের বাক্স x ১৬ মিলি; নিবন্ধন নম্বর: QLSP-1011-17; প্রস্তুতকারক: এফ. হফম্যান-লা রোচে লিমিটেড, সুইজারল্যান্ড)।
ভিয়েতনামে অ্যাভাস্টিন নির্দিষ্ট কিছু ক্যান্সারের চিকিৎসার জন্য লাইসেন্সপ্রাপ্ত, যার মধ্যে রয়েছে মেটাস্ট্যাটিক কোলোরেক্টাল ক্যান্সার, অ্যাডভান্সড, মেটাস্ট্যাটিক, অথবা রিকারেন্ট নন-স্মল সেল ফুসফুস ক্যান্সার, অ্যাডভান্সড এবং/অথবা মেটাস্ট্যাটিক রেনাল সেল কার্সিনোমা, গ্লিওব্লাস্টোমা/ম্যালিগন্যান্ট গ্লিওমা (WHO স্টেজ IV); এপিথেলিয়াল ওভারিয়ান, ফ্যালোপিয়ান টিউব এবং প্রাথমিক পেরিটোনিয়াল ক্যান্সার।
সাধারণ সতর্কতা ছাড়াও, FDA-অনুমোদিত প্যাকেজ ইনসার্টে "ইন্ট্রাভিট্রিয়াল ব্যবহারের জন্য নয়" সম্পর্কিত একটি সতর্কতা অন্তর্ভুক্ত রয়েছে।
বিশেষ করে, ওষুধটি দৃষ্টিশক্তির ব্যাঘাত ঘটাতে পারে, এবং ক্যান্সার রোগীদের শিরায় ইনফিউশনের জন্য তৈরি শিশি থেকে অ্যাভাস্টিন মিশ্রণের মাধ্যমে প্রশাসনের একটি অননুমোদিত পদ্ধতি, ইন্ট্রাভিট্রিয়াল ইনজেকশনের পরে চোখের গুরুতর প্রতিকূল ঘটনার পৃথক কেস এবং ক্লাস্টার রিপোর্ট করা হয়েছে।
এই প্রতিক্রিয়াগুলির মধ্যে রয়েছে চোখের ভিতরের সংক্রমণ, এন্ডোফথালমিটিস, ইউভাইটিস, রেটিনা ডিটাচমেন্ট, রেটিনার পিগমেন্ট এপিথেলিয়াল টিয়ার, গ্লুকোমা, চোখের ভিতরের রক্তক্ষরণ... এই ঘটনাগুলির মধ্যে কিছুর ফলে স্থায়ী অন্ধত্ব সহ বিভিন্ন মাত্রার দৃষ্টি ক্ষেত্র ক্ষতি হয়েছে ।
[বিজ্ঞাপন_২]
উৎস





![[ছবি] লাম ডং: টুই ফং-এ একটি সন্দেহজনক হ্রদ ফেটে যাওয়ার পর ক্ষয়ক্ষতির ছবি](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/02/1762078736805_8e7f5424f473782d2162-5118-jpg.webp)

![[ছবি] রাষ্ট্রপতি লুং কুওং মার্কিন যুদ্ধমন্ত্রী পিট হেগসেথকে স্বাগত জানাচ্ছেন](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/02/1762089839868_ndo_br_1-jpg.webp)





































































































মন্তব্য (0)