El 16 de septiembre, un representante de la Administración de Medicamentos informó que Novartis Vietnam había recibido cuatro denuncias de usuarios sobre la posible falsificación de gotas oftálmicas, entre ellas Tobrex, Maxitrol y TobraDex. Tras la verificación, se confirmó que el lote VEE90A de Tobrex de 5 ml era falsificado. Otros tres lotes, incluyendo Tobrex de 5 ml (lote VEE98C), Maxitrol de 5 ml (lote VFD09A) y TobraDex de 5 ml (lote VHN07A), también eran sospechosos de ser falsificados. Todos estos productos se encontraban circulando fuera del sistema de distribución oficial de la compañía. El representante de la Administración de Medicamentos indicó que dichos productos se vendían ampliamente en el mercado.
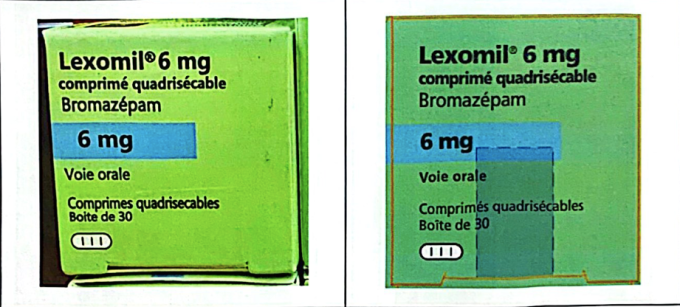
El segundo caso corresponde a la pastilla para dormir de alta dosis Lexomil 6 mg, propiedad de Cheplapharm Arzneimottel GmbH. La policía de Ciudad Ho Chi Minh confiscó el lote número F3193F01, con fecha de caducidad diciembre de 2027, y el fabricante confirmó que era falsificada. Este lote se fabricó originalmente para su comercialización en Francia, no para su importación a Vietnam. Actualmente, Lexomil 6 mg no cuenta con un número de registro para su comercialización en Vietnam, por lo que su venta y uso son ilegales.
Finalmente, está el medicamento Aclasta (que contiene ácido zoledrónico), utilizado para el tratamiento de la osteoporosis. Una farmacia en Kien Giang reportó un producto con fecha de producción de agosto de 2024 y fecha de caducidad de julio de 2027. La empresa registrada confirmó que este lote de medicamentos no fue importado oficialmente y que el empaque presentaba anomalías. Específicamente, los medicamentos Aclasta originales fabricados después de mayo de 2024 han reemplazado el logotipo de Novartis por el de Sandoz. Por lo tanto, se sospecha que los productos fabricados posteriormente que aún conservan el logotipo antiguo son falsificados.
Ante esta situación, la Administración de Medicamentos solicitó a los departamentos de salud locales que notificaran a hospitales, farmacias y a la población que no comercializaran ni utilizaran los medicamentos mencionados. Se asignaron unidades para inspeccionar, monitorear y rastrear con urgencia el origen de los productos infractores.
La agencia gestora recomienda que las personas revisen cuidadosamente la información del envase y la comparen con los datos del medicamento autorizado en el portal de la Administración de Medicamentos. Si detectan alguna anomalía, deben informar inmediatamente a las autoridades para que tomen las medidas oportunas.
PV (síntesis)Fuente: https://baohaiphong.vn/bo-y-te-canh-bao-khan-3-loai-thuoc-bi-nghi-lam-gia-521002.html


![[Foto] Lam Dong: Primer plano de un lago ilegal con un muro roto](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/03/1762166057849_a5018a8dcbd5478b1ec4-jpg.webp)

![[Foto] El primer ministro Pham Minh Chinh recibe al presidente de la Asociación de Amistad Japón-Vietnam en la región de Kansai.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/03/1762176259003_ndo_br_dsc-9224-jpg.webp)

![[Foto] Feria de Otoño 2025 y récords impresionantes](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/03/1762180761230_ndo_br_tk-hcmt-15-jpg.webp)
![[Foto] El secretario general To Lam recibe al embajador de Singapur, Jaya Ratnam](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/03/1762171461424_a1-bnd-5309-9100-jpg.webp)







































































































Kommentar (0)