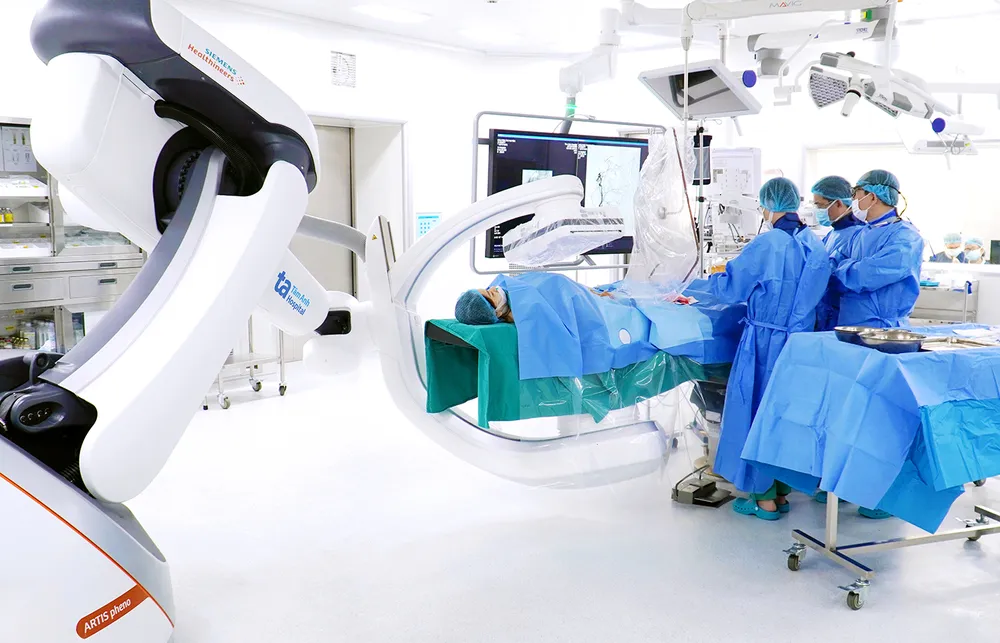
עלויות נמוכות יותר, יותר הזדמנויות טיפול.
בסוף דצמבר 2024, מכון המחקר טאם אנה השיק את פרויקט VISTA-1 בנושא אימונותרפיה פומית לטיפול בסרטן בווייטנאם. לאחר כמעט שישה חודשי יישום הניסוי, שמונה חולים עם סרטן המעי הגס בשלב סופי שטופלו לפי פרוטוקול המחקר לא הראו בתחילה תופעות לוואי משמעותיות הקשורות לתרופת המחקר והראו תוצאות מבטיחות.
מר מ. (בן 50), שהיה הראשון שבדק את התרופה בפרויקט זה וסבל מסרטן המעי הגס והחלחולת ששלח גרורות לכבד, אמר שעבר טיפולים שונים כגון כימותרפיה וטיפול ממוקד, אך ללא הצלחה. בינואר 2025 הוא נרשם להשתתף במחקר ונחשב זכאי. "חשבתי שאין לי אפשרויות אחרות, אבל בזכות ההזדמנות הזו להשתתף במחקר, אני מרגיש הקלה ויש לי יותר תקווה", שיתף מר מ.
לדברי ד"ר וו הוו חיאם, ראש המחלקה האונקולוגית בבית החולים הכללי טאם אנה בהאנוי , המטופלים שהשתתפו במחקר היו במעקב צמוד אחר בטיחותם ותגובהם לתרופת המחקר. צוות המחקר לא תיעד תסמינים חריגים הקשורים לתרופת המחקר במטופלים שהשתמשו בה בשלושת החודשים האחרונים.
"עבור חולים עם סרטן המעי הגס מתקדם שאינם מגיבים עוד למשטרי הטיפול הנוכחיים, כל שיפור בזמן ההישרדות במהלך השתתפותם במחקר זה הוא בעל משמעות רבה. אנחנו והחולים נכנסנו כעת לחודש הרביעי של מחקר זה", אמר ד"ר וו הוו חיאם.
בבית החולים האונקולוגי של הו צ'י מין סיטי, ד"ר פאן טאן תואן, ראש יחידת הניסויים הקליניים, ציין כי היחידה עורכת כיום 37 מחקרים קליניים, רובם בשיתוף פעולה עם חברות תרופות רב-לאומיות (Pharma). בית החולים משתף פעולה באופן יזום גם עם מרכזי סרטן אזוריים כדי לערוך מחקר עצמאי בעל ערך אקדמי ויישומים מעשיים. בית החולים משתמש לעתים קרובות בתרופות מהדור החדש להשוואה עם פרוטוקולי טיפול סטנדרטיים. רבות מתרופות אלו אינן זמינות עדיין בווייטנאם והן יקרות מאוד, כאשר חלקן עולות עד 300 מיליון וייטנאם דונג למחזור טיפול (3-4 שבועות). חולים המשתתפים במחקרים מקבלים את התרופה ללא תשלום, ללא קשר לענף הטיפול הספציפי שלהם.
"בנוסף לסיוע לחולים בגישה מוקדמת יותר לטיפול מודרני, מחקרים אלה גם מאפשרים לאנשי מקצוע מקומיים לשלוט בנתונים ולהעריך את יעילות התרופות על האוכלוסייה הווייטנאמית. זה מקצר את הזמן שלוקח להביא תרופות חדשות לשוק. תרופות רבות מהדור החדש יקרות מאוד. כאן, אנו מספקים גישה חופשית לתרופות מהדור החדש לכל החולים המשתתפים במחקר. כאשר המחקר מצליח, הוא יכול לקצר את הזמן שלוקח להביא תרופות חדשות לשוק", הסביר ד"ר פאן טאן תואן.
"ניסויים קליניים אחרונים סייעו לתעשיית הבריאות לגשת במהירות לטיפולים מודרניים, החל מכימותרפיה מסורתית ועד אימונותרפיה וטיפולים ממוקדים. התקדמויות אלו לא רק מסייעות להאריך את החיים אלא גם לשפר את איכות חייהם של המטופלים, תוך הרחבת הגישה לתרופות חדשות בעלויות נמוכות יותר עבור המטופלים ומערכת הבריאות."
סגן שר הבריאות נגוין ת'י ליאן הואונג
הרבה פוטנציאל, אבל חוסר במנגנונים.
לדברי פרופסור גיא תווייטס, מנהל יחידת המחקר הקליני באוניברסיטת אוקספורד, וייטנאם מובילה בניסויי תרופות למלריה מאז 1991, ומועילה למיליוני חולים ברחבי העולם. עם אוכלוסייה של כ-100 מיליון איש, וייטנאם מספקת קבוצת חולים מגוונת, אידיאלית לניסויים קליניים. קצב צמיחה ממוצע של 6-7% בתמ"ג לשנה, בשילוב עם מעמד ביניים הולך וגדל, מגביר עוד יותר את האטרקטיביות של וייטנאם עבור תורמים מקומיים ובינלאומיים כאחד. למרות הפוטנציאל הרב שלו, שוק הניסויים הקליניים בווייטנאם עדיין מתמודד עם מספר חסמים המאטים את התפתחותו ויוצרים חוסר סנכרון. זמן האישור לניסוי קליני בווייטנאם יכול להיות עד 160 ימים - הארוך ביותר באסיה, בעוד שהזמן הממוצע במדינות אחרות הוא כ-75 ימים. יתר על כן, וייטנאם מפגרת הרחק אחרי מדינות רבות באזור כמו סינגפור (18 ימים), אינדונזיה (20 ימים), יפן (31 ימים)... מסגרת זמן זו משפיעה על האטרקטיביות של השוק הווייטנאמי עבור נותני חסות למחקר.
יתר על כן, ניסויים קליניים דורשים שיתוף פעולה הדוק בין רופאים, אחיות, רכזי מחקר ומנהלי נתונים. עם זאת, וייטנאם חסר כיום כוח אדם מיומן היטב; היא גם מתמודדת עם קשיים כלכליים ומנגנוני תמריצים לא מספקים. ניסוי קליני שלב 3 יכול לעלות בין 10 ל-20 מיליון דולר. בינתיים, משקיעים רבים דיווחו כי וייטנאם חסרים תמריצי מס, מימון מחקר או מנגנוני מימון משותף בדומה לאלה שבסינגפור ובדרום קוריאה. חלוקת המימון מתעכבת לעתים קרובות עקב הליכים מנהליים, מה שמשפיע על התקדמות הניסויים ומפחית את התחרותיות בהשוואה למדינות אחרות באזור.
כדי לפתח את מגזר הניסויים הקליניים בווייטנאם, ד"ר פאן טאן תואן מציע לפשט את הליכי האישור באמצעות מערכת מקוונת מרכזית כדי לקצר את תהליך האישור המורכב הנוכחי. בנוסף, יש ליישם רישום מקוון באמצעות פורטל בשפה האנגלית ותיעוד דו-לשוני כדי לייעל את התהליך עבור תורמים בינלאומיים. כדי להתחרות במדינות אחרות באזור, יש לפתח מדיניות מועדפת כגון פטורים ממס, מימון מחקר או מנגנוני מימון משותף לעלויות הניסויים, בדומה לתוכניות בסינגפור ובתאילנד.
"וייטנאם צריכה לקדם מודלים של שותפות ציבורית-פרטית במחקר ניסויים קליניים כדי לסייע בחלוקת סיכונים ולשפר משאבים לפיתוח בר-קיימא בתעשייה. יחד עם זאת, יש צורך במדיניות להשקעה בתשתיות, יצירת מתקני בדיקה נוספים והרחבת תוכניות הכשרה ייעודיות לצוות באמצעות שיתוף פעולה עם אוניברסיטאות וארגונים בינלאומיים", הציע ד"ר פאן טאן תואן.
מר לוק טרלואר, ראש מחלקת תשתיות, ממשלה ובריאות ב-KPMG וייטנאם: פיתוח מדיניות תמריצים
תהליך אישור הניסויים הקליניים בווייטנאם כולל שלבים רבים. ראשית, קבלת אישור ברמה המקומית אורכת בין 3 ל-12 חודשים, בהתאם למספר המחקר ולמיקוםו. לאחר מכן, תהליך האישור במשרד הבריאות אורכת בממוצע 3 עד 5 חודשים. לבסוף, קבלת רישיון ייבוא לתרופה (לניסויים בתרופות) אורכת בממוצע 3 עד 4 חודשים. מספר מרכזי הניסויים הקליניים והמחקרים בווייטנאם נמוך מדי ביחס לאוכלוסייתה, דבר המסכן את עצמה בפיגור במרוץ להפוך למרכז מחקר קליני אזורי. וייטנאם זקוקה למדיניות להשקעה בתשתיות, בניית מתקני ניסוי נוספים והרחבת תוכניות הכשרה ייעודיות לצוות באמצעות שיתוף פעולה עם אוניברסיטאות וארגונים בינלאומיים. כדי להתחרות במדינות אחרות באזור, עליה לפתח מדיניות תמריצים כגון פטורים ממס, מימון מחקר או מנגנוני מימון משותף לעלויות הניסויים, בדומה לתוכניות בסינגפור ובתאילנד.
מר נגוין נגו קוואנג, מנהל מחלקת המדע, הטכנולוגיה וההכשרה (משרד הבריאות): סטנדרטיזציה של פעילויות ניסויים קליניים.
בתקופה הקרובה, משרד הבריאות ימשיך לחדד את המסגרת המשפטית ולתקנן את פעילויות הניסויים הקליניים בהתאם לתקנים בינלאומיים. במקביל, הוא יחזק את יכולותיה של המועצה הלאומית לאתיקה במחקר ביו-רפואי. נכון לעכשיו, משרד הבריאות מבקש משוב על טיוטת חוזר המפרט תקנות בנוגע לניסויים קליניים בתרופות. חוזר זה יפרט את פרטי הניסויים הקליניים בתרופות, כולל עקרונות, סטנדרטים, נהלים ואחריות הקשורים לבדיקת תרופות על מתנדבים כדי להעריך את בטיחותן ויעילותן של תרופות, לזהות תגובות שליליות לתרופות (ADRs) ולבדוק את הפרמקוקינטיקה של תרופות. על פי טיוטת החוזר, עקרונות הניסויים הקליניים בתרופות חייבים להבטיח קפדנות מדעית, אובייקטיביות, יושר, שקיפות ולהגן על זכויותיהם של משתתפי המחקר.
MINH NAM - MINH KHA NG הוקלט
מקור: https://www.sggp.org.vn/gian-nan-thu-nghiem-lam-sang-post802539.html


![[תמונה] משטרת האנוי הוכתרה רשמית כאלופת ליגת ה-V לעונת 2025/2026](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2026/05/31/1780244769054_ndo_br_039d561b692be875b13a-jpg.webp)


![[תמונה] טקס רחצה חגיגי ותהלוכת בודהה בהואה](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2026/05/31/1780228263543_1-jpg.webp)
![[תמונה] התפעלו מ"יצירת המופת" של האלמוגים בתוך המורשת בת מיליון השנים של מחוז דאק לק.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2026/05/31/1780221235105_anh-man-hinh-2026-05-31-luc-16-53-27.png)
![[תמונה] המזכיר הכללי, הנשיא ואשתו מתחילים את ביקורם הממלכתי בפיליפינים.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2026/05/31/1780230559452_anh-man-hinh-2026-05-31-luc-19-28-11.png)





















![[וידאו] שקיעה בלגונה לאפ אן – המקום בו השמש שוקעת מעל רשתות הדיג](https://vphoto.vietnam.vn/thumb/340x192/vietnam/resource/IMAGE/2026/05/31/1780192137701_beach-landscape-sea-water-nature-grass-745871-pxhere-com.jpeg)








































![[תמונה] התפעלו מ"יצירת המופת" של האלמוגים בתוך המורשת בת מיליון השנים של מחוז דאק לק.](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2026/05/31/1780221235105_anh-man-hinh-2026-05-31-luc-16-53-27.png)







































תגובה (0)