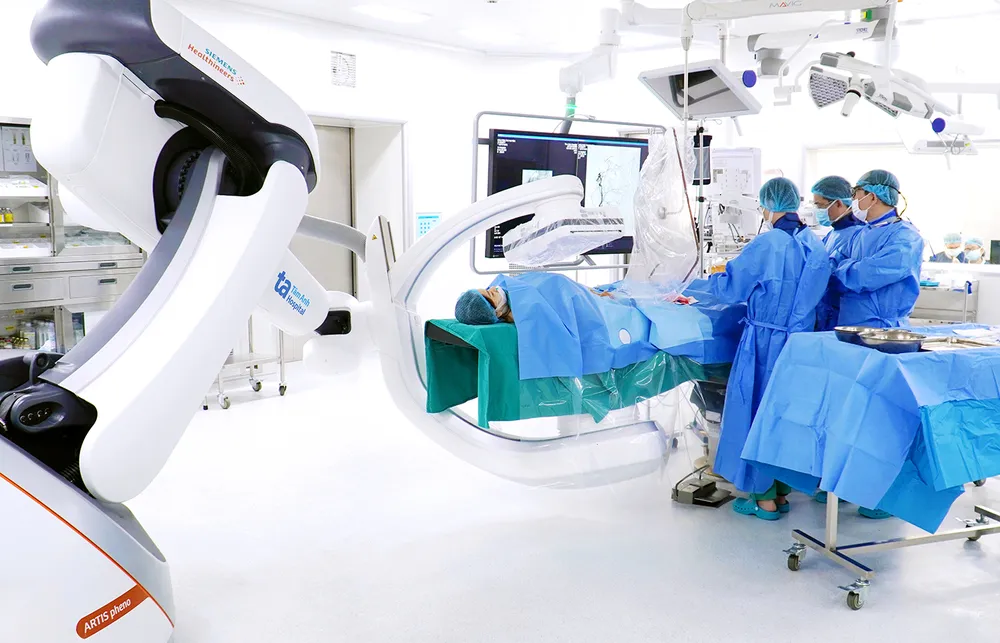
Lagere kosten, meer behandelingsmogelijkheden.
Eind december 2024 lanceerde het Tam Anh Research Institute het VISTA-1-project voor orale immunotherapie bij de behandeling van kanker in Vietnam. Na bijna zes maanden proefbehandeling vertoonden acht patiënten met terminale darmkanker, behandeld volgens het onderzoeksprotocol, aanvankelijk geen significante bijwerkingen van het onderzoeksmedicijn en veelbelovende resultaten.
De heer M. (50 jaar), die als eerste het medicijn in dit project testte en leed aan darmkanker met uitzaaiingen naar de lever, vertelde dat hij verschillende behandelingen had ondergaan, zoals chemotherapie en doelgerichte therapie, maar zonder succes. In januari 2025 meldde hij zich aan voor deelname aan de studie en werd hij geschikt bevonden. "Ik dacht dat ik geen andere opties meer had, maar dankzij deze kans om aan de studie deel te nemen, voel ik me opgelucht en heb ik meer hoop", aldus de heer M.
Volgens dr. Vu Huu Khiem, hoofd van de afdeling Oncologie van het Tam Anh Algemeen Ziekenhuis in Hanoi , werden de patiënten die aan het onderzoek deelnamen nauwlettend in de gaten gehouden wat betreft veiligheid en reactie op het onderzoeksmedicijn. Het onderzoeksteam heeft geen ongebruikelijke symptomen geconstateerd die verband houden met het onderzoeksmedicijn bij patiënten die het de afgelopen drie maanden hebben gebruikt.
"Voor patiënten met vergevorderde darmkanker die niet meer reageren op de huidige behandelingen, is elke verbetering van de overlevingstijd tijdens hun deelname aan dit onderzoek van groot belang. Wij en de patiënten zijn nu de vierde maand van dit onderzoek ingegaan", aldus dr. Vu Huu Khiem.
In het oncologisch ziekenhuis van Ho Chi Minh-stad verklaarde dr. Phan Tan Thuan, hoofd van de afdeling Klinische Studies, dat de afdeling momenteel 37 klinische studies uitvoert, voornamelijk in samenwerking met multinationale farmaceutische bedrijven. Het ziekenhuis werkt ook proactief samen met regionale kankercentra om onafhankelijk onderzoek te verrichten met academische waarde en praktische toepassingen. Het ziekenhuis gebruikt vaak geneesmiddelen van de nieuwe generatie ter vergelijking met standaardbehandelingsprotocollen. Veel van deze geneesmiddelen zijn nog niet beschikbaar in Vietnam en zijn erg duur, sommige kosten tot wel 300 miljoen VND per behandelingscyclus (3-4 weken). Patiënten die deelnemen aan de studies ontvangen de medicatie gratis, ongeacht hun specifieke behandelingsrichting.
“Naast het feit dat patiënten hierdoor eerder toegang krijgen tot moderne behandelingen, stellen deze studies binnenlandse professionals ook in staat om gegevens te verzamelen en de effectiviteit van geneesmiddelen op de Vietnamese bevolking te evalueren. Dit verkort de tijd die nodig is om nieuwe geneesmiddelen op de markt te brengen. Veel geneesmiddelen van de nieuwe generatie zijn erg duur. Wij bieden hier gratis toegang tot geneesmiddelen van de nieuwe generatie aan alle patiënten die aan het onderzoek deelnemen. Als het onderzoek succesvol is, kan dit de tijd die nodig is om nieuwe geneesmiddelen op de markt te brengen aanzienlijk verkorten”, aldus dr. Phan Tan Thuan.
"Recente klinische onderzoeken hebben de gezondheidszorgsector geholpen om snel toegang te krijgen tot moderne behandelingen, van traditionele chemotherapie tot immunotherapie en doelgerichte therapieën. Deze vooruitgang helpt niet alleen om de levensduur te verlengen, maar verbetert ook de levenskwaliteit van patiënten, terwijl de toegang tot nieuwe geneesmiddelen tegen lagere kosten voor zowel patiënten als het zorgsysteem wordt vergroot."
Viceminister van Volksgezondheid Nguyen Thi Lien Huong
Veel potentie, maar een gebrek aan mechanismen.
Volgens professor Guy Thwaites, directeur van de Clinical Research Unit aan de Universiteit van Oxford, is Vietnam sinds 1991 een koploper in klinische studies naar malariamedicijnen, waarvan miljoenen patiënten wereldwijd hebben geprofiteerd. Met een bevolking van ongeveer 100 miljoen mensen biedt Vietnam een diverse patiëntengroep, ideaal voor klinische studies. Een gemiddelde bbp-groei van 6-7% per jaar, in combinatie met een groeiende middenklasse, versterkt de aantrekkelijkheid van Vietnam voor zowel binnenlandse als internationale donoren. Ondanks het grote potentieel kampt de markt voor klinische studies in Vietnam nog steeds met diverse belemmeringen die de ontwikkeling vertragen en een gebrek aan synchronisatie veroorzaken. De goedkeuringstijd voor een klinische studie in Vietnam kan oplopen tot 160 dagen – de langste in Azië, terwijl de gemiddelde tijd in andere landen rond de 75 dagen ligt. Bovendien loopt Vietnam ver achter op veel landen in de regio, zoals Singapore (18 dagen), Indonesië (20 dagen) en Japan (31 dagen). Deze lange doorlooptijd beïnvloedt de aantrekkelijkheid van de Vietnamese markt voor onderzoeksponsors.
Bovendien vereisen klinische studies een nauwe samenwerking tussen artsen, verpleegkundigen, onderzoekscoördinatoren en datamanagers. Vietnam kampt momenteel echter met een tekort aan goed opgeleid personeel, financiële problemen en ontoereikende stimuleringsmechanismen. Een fase 3-klinische studie kan tussen de 10 en 20 miljoen dollar kosten. Veel investeerders melden bovendien dat Vietnam geen fiscale stimuleringsmaatregelen, onderzoeksfinanciering of cofinancieringsmechanismen kent zoals die in Singapore en Zuid-Korea. De uitbetaling van subsidies wordt vaak vertraagd door administratieve procedures, wat de voortgang van studies belemmert en de concurrentiepositie ten opzichte van andere landen in de regio verzwakt.
Om de sector voor klinische studies in Vietnam te ontwikkelen, stelt dr. Phan Tan Thuan voor om de goedkeuringsprocedures te vereenvoudigen door middel van een gecentraliseerd online systeem. Dit verkort het huidige complexe goedkeuringsproces. Daarnaast zou online registratie via een Engelstalig portaal en tweetalige documentatie moeten worden ingevoerd om het proces voor internationale donoren te stroomlijnen. Om te kunnen concurreren met andere landen in de regio, zouden preferentiële beleidsmaatregelen zoals belastingvrijstellingen, onderzoeksfinanciering of cofinancieringsmechanismen voor studiekosten, vergelijkbaar met programma's in Singapore en Thailand, moeten worden ontwikkeld.
"Vietnam zou publiek-private samenwerkingsmodellen in klinisch onderzoek moeten bevorderen om risico's te delen en middelen te versterken voor een duurzame ontwikkeling van de sector. Daarnaast is er behoefte aan beleid om te investeren in infrastructuur, meer testfaciliteiten te creëren en gespecialiseerde trainingsprogramma's voor personeel uit te breiden door samenwerking met universiteiten en internationale organisaties", aldus dr. Phan Tan Thuan.
De heer Luke Treloar, hoofd Infrastructuur, Overheid en Gezondheidszorg bij KPMG Vietnam: Het ontwikkelen van stimuleringsbeleid
Het goedkeuringsproces voor klinische studies in Vietnam omvat vele stappen. Ten eerste duurt het verkrijgen van goedkeuring op lokaal niveau tussen de 3 en 12 maanden, afhankelijk van het aantal en de locatie van de studie. Vervolgens duurt de goedkeuringsprocedure bij het Ministerie van Volksgezondheid gemiddeld 3 tot 5 maanden. Ten slotte duurt het verkrijgen van een importvergunning voor het geneesmiddel (voor geneesmiddelenonderzoek) gemiddeld 3 tot 4 maanden. Het aantal centra voor klinisch onderzoek en studies in Vietnam is te laag in verhouding tot de bevolking, waardoor het land het risico loopt achter te blijven in de race om een regionaal centrum voor klinisch onderzoek te worden. Vietnam heeft beleid nodig om te investeren in infrastructuur, meer onderzoeksfaciliteiten te bouwen en gespecialiseerde trainingsprogramma's voor personeel uit te breiden door samenwerking met universiteiten en internationale organisaties. Om te kunnen concurreren met andere landen in de regio, moet het stimulerend beleid ontwikkelen, zoals belastingvrijstellingen, onderzoekssubsidies of cofinancieringsmechanismen voor onderzoekskosten, vergelijkbaar met programma's in Singapore en Thailand.
De heer Nguyen Ngo Quang, directeur van het Departement Wetenschap, Technologie en Opleiding (Ministerie van Volksgezondheid): Standaardisering van klinische onderzoeksactiviteiten.
In de komende periode zal het Ministerie van Volksgezondheid het wettelijk kader verder verfijnen en de activiteiten van klinische proeven standaardiseren in overeenstemming met internationale normen. Tegelijkertijd zal het de capaciteit van de Nationale Raad voor Biomedische Ethiek versterken. Momenteel vraagt het Ministerie van Volksgezondheid om feedback op een conceptcirculaire met gedetailleerde regelgeving voor klinische geneesmiddelenproeven. Deze circulaire zal de details van klinische geneesmiddelenproeven specificeren, inclusief principes, normen, procedures en verantwoordelijkheden met betrekking tot het testen van geneesmiddelen op vrijwilligers om de veiligheid en werkzaamheid van geneesmiddelen te beoordelen, bijwerkingen te identificeren en de farmacokinetiek van geneesmiddelen te bestuderen. Volgens het conceptcirculaire moeten de principes van klinische geneesmiddelenproeven wetenschappelijke nauwkeurigheid, objectiviteit, eerlijkheid en transparantie waarborgen en de rechten van de deelnemers aan het onderzoek beschermen.
MINH NAM - MINH KHA NG opgenomen
Bron: https://www.sggp.org.vn/gian-nan-thu-nghiem-lam-sang-post802539.html


![[Foto] Secretaris-generaal en president To Lam en de president van de Filipijnen in gesprek.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2026/06/01/1780286997787_anh-man-hinh-2026-06-01-luc-11-09-43.png)


![[Foto] Receptie ter verwelkoming van secretaris-generaal en president To Lam en zijn vrouw tijdens hun staatsbezoek aan de Filipijnen](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2026/06/01/1780295488620_vna-potal-chieu-dai-chao-mung-tong-bi-thu-chu-tich-nuoc-to-lam-va-phu-nhan-tham-cap-nha-nuoc-toi-philippines-8798060-7855-jpg.webp)















































































































Reactie (0)