ในการประชุมภาคบ่ายของวันที่ 21 พฤศจิกายน สมัยประชุมที่ 8 ของ สภานิติบัญญัติแห่งชาติ ชุดที่ 15 โดยผู้แทนส่วนใหญ่เห็นด้วย สภานิติบัญญัติแห่งชาติได้ผ่านกฎหมายแก้ไขและเพิ่มเติมมาตราต่างๆ ของกฎหมายว่าด้วยเภสัชกรรมอย่างเป็นทางการ

ด้วยคะแนนเสียงเห็นชอบถึง 88.94% ของผู้แทนทั้งหมด กฎหมายแก้ไขและเพิ่มเติมมาตราต่างๆ ของกฎหมายการเภสัชกรรมจึงได้รับการอนุมัติอย่างเป็นทางการในการประชุมสมัชชาแห่งชาติครั้งที่ 8 สมัยที่ 15
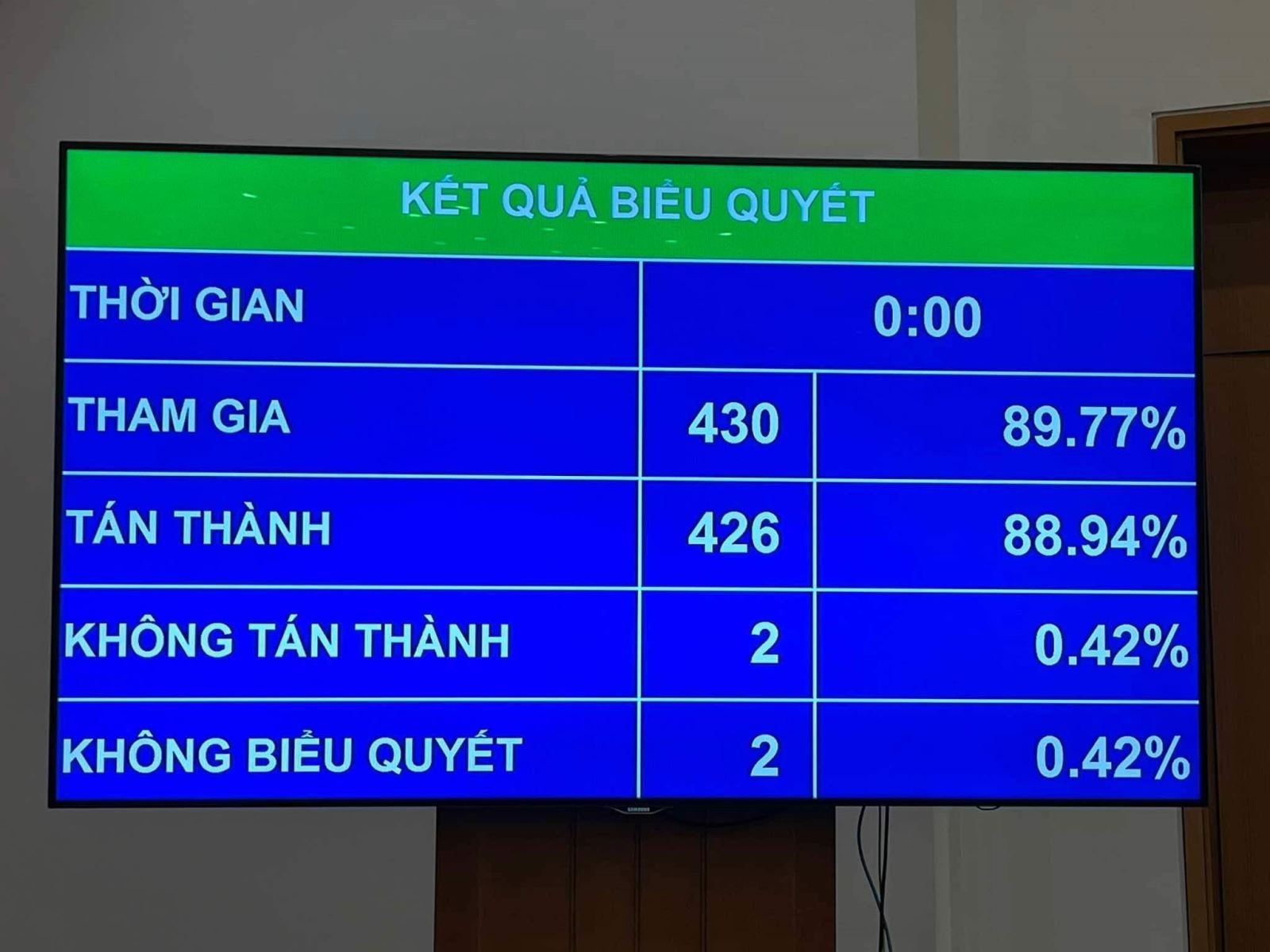
ก่อนที่สมาชิกสภานิติบัญญัติแห่งชาติจะลงมติเห็นชอบร่างกฎหมายแก้ไขและเพิ่มเติมมาตราต่างๆ ของกฎหมายว่าด้วยเภสัชกรรม สภานิติบัญญัติแห่งชาติได้ลงมติเห็นชอบเนื้อหา 2 ประการของกฎหมายดังกล่าว ได้แก่
เกี่ยวกับข้อ 23 มาตรา 1 ว่าด้วยสิทธิและความรับผิดชอบของสถานประกอบการที่จัดตั้งเครือร้านยาและร้านขายยาในเครือร้านยา ผลการลงคะแนนคือผู้แทน 89.14% เห็นด้วย
ลงคะแนนเสียงเกี่ยวกับมาตรา 30 ข้อ 1 ว่าด้วยอำนาจ บันทึก ขั้นตอน และระยะเวลาในการออกและต่ออายุใบรับรองการลงทะเบียนการหมุนเวียนยาและส่วนประกอบของยา ผลการลงคะแนนคือผู้แทน 86.22% เห็นด้วย
ก่อนการลงคะแนนเสียง นางสาวเหงียน ถุ่ย อันห์ ประธานคณะกรรมการสังคมของรัฐสภาอ่านรายงานเกี่ยวกับการรับ การอธิบาย และการแก้ไขร่างกฎหมายแก้ไขและเพิ่มเติมมาตราต่างๆ ของกฎหมายเภสัชกรรม
โดยเฉพาะเกี่ยวกับนโยบายของรัฐเกี่ยวกับผลิตภัณฑ์ยาและการพัฒนาอุตสาหกรรมยา (มาตรา 7 และ 8 (แก้ไข) โดยคำนึงถึงความคิดเห็นของผู้แทน คณะกรรมาธิการสามัญสภาแห่งชาติได้สั่งให้ทบทวนมาตรา 7 (แก้ไข) เพื่อให้แน่ใจว่าสะท้อนเนื้อหาหลักของหลักการ โดยเพิ่มบทบัญญัติว่า "มีนโยบายควบคุมจำนวนใบรับรองการขึ้นทะเบียนจำหน่ายยาสำหรับยาที่มีส่วนประกอบออกฤทธิ์และวัสดุยาเดียวกันให้สอดคล้องกับสภาพ เศรษฐกิจและสังคม ในแต่ละช่วงเวลา" ในมาตรา 14 และ "ให้ความสำคัญกับการลงทุนในการพัฒนาโครงสร้างพื้นฐานด้านเทคโนโลยีสารสนเทศ การดำเนินการเปลี่ยนแปลงทางดิจิทัลในกิจกรรมด้านเภสัชกรรม" ในมาตรา 15 อย่างไรก็ตาม เพื่อให้นโยบายสามารถนำไปปฏิบัติได้ โดยเฉพาะบทบัญญัติในมาตรา 8, 13, 14 คณะกรรมาธิการสามัญสภาแห่งชาติจึงต้องการขออนุญาตให้รัฐบาลกำหนดมาตรานี้โดยละเอียดต่อไป
เกี่ยวกับนโยบายการให้สิทธิพิเศษและการสนับสนุนการลงทุนในการพัฒนาอุตสาหกรรม คณะกรรมาธิการถาวรของสภานิติบัญญัติแห่งชาติ (National Assembly Committee) ได้ตกลงกับ รัฐบาล ในการรับรองมาตรา 8 วรรค 1 ตามตัวเลือกที่ 1 เกี่ยวกับนโยบายการให้สิทธิพิเศษและการสนับสนุนการลงทุนสำหรับโครงการที่เพิ่งจัดตั้งใหม่ในภาคเภสัชกรรมที่มีทุนการลงทุนรวม 3,000 พันล้านดองหรือมากกว่า โดยต้องจ่ายเงินอย่างน้อย 1,000 พันล้านดอง ภายใน 3 ปี นับจากวันที่ได้รับหนังสือรับรองการจดทะเบียนการลงทุนหรือวันที่ได้รับอนุมัติจากนโยบายการลงทุน โดยพิจารณาจากความคิดเห็นของผู้แทนส่วนใหญ่ พร้อมกันนี้ เพื่อให้เกิดความสอดคล้องกันในนโยบายการให้สิทธิพิเศษและการสนับสนุนการลงทุนพิเศษในภาคเภสัชกรรม คณะกรรมาธิการถาวรของสภานิติบัญญัติแห่งชาติได้ขอให้รัฐบาลให้ความสำคัญต่อการแสดงแรงจูงใจทางภาษีเมื่อแก้ไขกฎหมายภาษีและกฎหมายที่เกี่ยวข้อง รวมถึงร่างกฎหมายว่าด้วยภาษีเงินได้นิติบุคคล (แก้ไขแล้ว)
ส่วนกิจการร้านยาในเครือ (มาตรา 17 ก. (เพิ่มเติม) มาตรา 31 32 33 36 37 และ 38 (แก้ไข) มาตรา 47 ก. (เพิ่มเติม) คณะกรรมาธิการสามัญสมัชชาแห่งชาติได้พิจารณาและแก้ไขบทบัญญัติเกี่ยวกับร้านยาในเครือตามความเห็นของผู้แทน รวมถึงเนื้อหาการมอบหมายให้รัฐมนตรีว่าการกระทรวงสาธารณสุขควบคุมการหมุนเวียนผู้รับผิดชอบด้านเภสัชกรรมระหว่างร้านยาในเครือดังที่แสดงในข้อ g วรรค 2 มาตรา 47 ก. (เพิ่มเติม) ควบคุมความรับผิดชอบของร้านยาในเครือในการระงับการดำเนินการชั่วคราวในกรณีที่สถานประกอบการที่จัดระบบร้านยาระงับการดำเนินการชั่วคราวเป็นเวลา 6 เดือนขึ้นไป (ข้อ d วรรค 4 มาตรา 47 ก. (เพิ่มเติม) และให้ยุติการดำเนินการเมื่อสถานประกอบการที่จัดระบบร้านยาหยุดดำเนินการชั่วคราว (ข้อ d วรรค 4 มาตรา 47 ก. (เสริม)
ว่าด้วยการซื้อขายยาและส่วนประกอบยาโดยอีคอมเมิร์ซ (มาตรา 6, 32 และ 42 (แก้ไข)) ตามความคิดเห็นของผู้แทน เพื่อให้แน่ใจว่ามีการบริหารจัดการสถานการณ์ที่อาจเกิดขึ้นในทางปฏิบัติอย่างทันท่วงที นอกเหนือจากสิทธิและความรับผิดชอบที่กำหนดไว้ในร่างกฎหมายแล้ว คณะกรรมาธิการถาวรของรัฐสภาได้เพิ่มมาตราที่กำหนดให้สถานประกอบการธุรกิจยาที่ใช้ระบบอีคอมเมิร์ซต้องปฏิบัติตามกฎข้อบังคับของรัฐบาลว่าด้วยการขายส่งยา ส่วนผสมยา และการขายปลีกยาโดยใช้ระบบอีคอมเมิร์ซ ในข้อ h วรรค 4 มาตรา 42 (แก้ไข) พร้อมกันนี้ ให้สรุปข้อกำหนดเกี่ยวกับสิทธิและความรับผิดชอบของสถานประกอบการยาในการประกอบธุรกิจผ่านระบบอีคอมเมิร์ซในข้อ 4 มาตรา 42 (แก้ไขเพิ่มเติม)
เกี่ยวกับการออก ขยายเวลา เปลี่ยนแปลง และเพิ่มเติมหนังสือรับรองการขึ้นทะเบียนการจำหน่ายยา (มาตรา 56 (แก้ไขเพิ่มเติม) โดยนำหลักการคิดสร้างสรรค์ในการตีความกฎหมายมาปฏิบัติ คณะกรรมาธิการถาวรของสภานิติบัญญัติแห่งชาติได้แก้ไขเนื้อหาที่แก้ไขในมาตรา 56 โดยไม่ได้กำหนดไว้ในกฎหมายโดยเฉพาะ แต่มอบหมายให้รัฐมนตรีว่าการกระทรวงสาธารณสุขกำหนดเอกสารและขั้นตอนในการออก ขยายเวลา เปลี่ยนแปลง และเพิ่มเติมหนังสือรับรองการขึ้นทะเบียนการจำหน่ายยาและส่วนประกอบทางเภสัชกรรมในมาตรา 56
นอกจากนี้ การยอมรับความคิดเห็นของผู้แทนที่เสนอให้ศึกษาและเพิ่มเติมกฎระเบียบเพื่อจำกัดการออกใบสำคัญการขึ้นทะเบียนจำหน่ายยาใหม่สำหรับยาที่มีการซ้ำซ้อน เพื่อจำกัดการใช้มาตรการเพื่อ “สงวน” การขึ้นทะเบียนใบอนุญาตจำหน่ายเนื่องจากค่าธรรมเนียมใบอนุญาตที่ต่ำ โดยในอนาคตอันใกล้นี้ มาตรา 56 (แก้ไขเพิ่มเติม) วรรค 7 กำหนดว่าจะไม่ต่ออายุใบสำคัญการขึ้นทะเบียนจำหน่ายยาที่ไม่มีจำหน่ายในท้องตลาดเป็นเวลา 5 ปี พร้อมกันนี้ มาตรา 7 (แก้ไขเพิ่มเติม) มาตรา 14 บัญญัติให้รัฐมีนโยบายควบคุมจำนวนใบรับรองการขึ้นทะเบียนจำหน่ายยาสำหรับยาที่มีส่วนประกอบสำคัญและสมุนไพรเดียวกัน และมอบหมายให้รัฐบาลจัดทำระเบียบปฏิบัติอย่างละเอียด
ในส่วนการบริหารจัดการราคาของยา (คำอธิบายเงื่อนไขในมาตรา 44, 45, 46 และ 47 มาตรา 2 (แก้ไข) มาตรา 107, 109, 110, 112 และ 113 (แก้ไข) ยกเลิกมาตรา 114) : โดยรับเอาความคิดเห็นของผู้แทน คณะกรรมาธิการสามัญของสภานิติบัญญัติแห่งชาติได้พิจารณาและเห็นด้วยกับข้อเสนอของรัฐบาลในการกำกับดูแลมาตรการในการประกาศราคาขายส่งที่คาดว่าจะใช้กับยาที่ต้องสั่งโดยแพทย์ นี่เป็นมาตรการเฉพาะในการบริหารราคาของยา เนื่องจากยาที่ต้องสั่งโดยแพทย์นั้นมีสัดส่วนของตลาดค่อนข้างมาก และใช้กันแพร่หลายในสถานพยาบาล และผู้ป่วยจะต้องซื้อยาตามใบสั่งของแพทย์ นอกจากนี้ กระทรวงสาธารณสุขยังได้แนะนำราคาขายส่งยาที่คาดว่าจะให้แก่ผู้ประกอบการค้ายา เพื่อจำกัดการปรับขึ้นราคายาในแต่ละระดับ ระดับกลาง และการปรับขึ้นราคาเมื่อถึงมือผู้บริโภค พร้อมกันนี้ ให้รักษาข้อกำหนดปัจจุบันเกี่ยวกับอัตรากำไรขายปลีกสูงสุดของยาที่จำหน่ายในสถานประกอบการปลีกยาภายในบริเวณสถานตรวจสุขภาพและสถานพยาบาล
เกี่ยวกับข้อเสนอของผู้แทนเกี่ยวกับมาตรการการประกาศราคา เนื่องจากเนื้อหานี้ได้ดำเนินการตามกฎหมายว่าด้วยราคา คณะกรรมาธิการถาวรของสภานิติบัญญัติแห่งชาติได้เสนอให้รัฐบาลทบทวนเอกสารแนะนำและระเบียบโดยละเอียดของกฎหมายว่าด้วยราคา พ.ศ. 2566 เพื่อเสริมระเบียบเกี่ยวกับเกณฑ์ในการคัดเลือกรายชื่อสถานประกอบการที่ต้องประกาศราคา เพื่อให้มั่นใจว่ามีการนำไปปฏิบัติอย่างสอดคล้องและโปร่งใสในท้องถิ่น พร้อมกันนี้ ให้ติดตามกระบวนการดำเนินการอย่างใกล้ชิด ตรวจพบความยากลำบากและปัญหาในการจัดการอย่างทันท่วงที ขอให้กระทรวงสาธารณสุขปรับปรุงรายชื่อยาหลักอย่างสม่ำเสมอเพื่อให้แน่ใจว่ามีแนวทางที่ครบถ้วนสอดคล้องกับบทบัญญัติของกฎหมายว่าด้วยราคา
ส่วนบทบัญญัติเกี่ยวกับการนำไปปฏิบัติ (มาตรา 3) : ในการตอบสนองต่อความคิดเห็นของผู้แทน คณะกรรมาธิการถาวรของสภาแห่งชาติได้แก้ไขผลการดำเนินการและบทบัญญัติการเปลี่ยนผ่านดังที่แสดงไว้ในมาตรา 3 ของร่างกฎหมาย ดังนั้น กฎหมายจะมีผลบังคับใช้ตั้งแต่วันที่ 1 กรกฎาคม 2568 (มาตรา 3 วรรค 1) และจะใช้บังคับตั้งแต่วันที่ 1 มกราคม 2568 เฉพาะบทบัญญัติเกี่ยวกับการขยายระยะเวลาหนังสือรับรองการขึ้นทะเบียนการหมุนเวียนยาและส่วนประกอบของยา และบทบัญญัติเกี่ยวกับการค้าส่งยาและส่วนประกอบของยาโดยสถานประกอบการผลิต นำเข้า และค้าส่งยา (มาตรา 3 วรรค 2) เพื่อแก้ไขปัญหาในธุรกิจยาอย่างทันท่วงที
ความคิดเห็นของสมาชิกสภานิติบัญญัติแห่งชาติได้รับการศึกษาอย่างจริงจัง พิจารณาอย่างถี่ถ้วน และร่างกฎหมายได้รับการแก้ไขในเนื้อหาที่เฉพาะเจาะจง เช่น (i) แนวคิดเรื่อง "ยาที่ไม่ต้องมีใบสั่งแพทย์" และ "ยาเทคโนโลยีขั้นสูง" (ii) กำหนดว่าผู้รับผิดชอบความเชี่ยวชาญด้านเภสัชกรรมในองค์กรเครือร้านยาต้องมีวุฒิการศึกษาระดับปริญญาตรีด้านเภสัชกรรมและมีประสบการณ์ปฏิบัติงานวิชาชีพ 2 ปีในสถานพยาบาลที่เหมาะสม (iii) เพื่อให้แน่ใจว่ามีความโปร่งใสและความสอดคล้องกันในระเบียบข้อบังคับเกี่ยวกับสิทธิของสถานประกอบการผลิต สถานประกอบการส่งออกและนำเข้า สถานประกอบการค้าส่งยาและส่วนผสมยา และธุรกิจยาที่มีการลงทุนจากต่างประเทศ (iv) อนุญาตให้สถานพยาบาลตรวจและรักษาสามารถนำเข้ายาที่ไม่มีใบรับรองการจดทะเบียนจำหน่ายในประเทศเวียดนาม เพื่อให้บริการความต้องการการรักษาพิเศษของผู้ป่วยในสถานพยาบาลตามข้อ 1 วรรค 2 ข้อ 60 และมอบหมายให้รัฐบาลกำหนดรายละเอียดเกี่ยวกับการถ่ายโอนยาตามข้อ d ข้อ 7 ข้อ 60 (v) มอบหมายให้รัฐมนตรีว่าการกระทรวงสาธารณสุขกำหนดรูปแบบและวิธีการแจ้งข้อมูลยา (แทนรัฐบาลในปัจจุบัน) และปรับปรุงถ้อยคำ สไตล์ และเทคนิคทางกฎหมายในมาตราและมาตราส่วนใหญ่ของร่างกฎหมาย
ร่างกฎหมายแก้ไขใหม่ ประกอบด้วย 3 มาตรา โดยมาตรา 1 แก้ไขเพิ่มเติม 50 มาตรา ยกเลิก 2 ประเด็น 2 วรรคและ 1 มาตรา ของกฎหมายเภสัชกรรมฉบับปัจจุบัน และเพิ่มมาตราใหม่ 3 มาตรา มาตรา 2 แก้ไขและเพิ่มเติมภาคผนวกหมายเลข 01 ที่ออกร่วมกับกฎหมายราคาหมายเลข 16/2023/QH15 มาตรา 3 ว่าด้วยเงื่อนไขการบังคับใช้
เนื้อหาการรับ การชี้แจง และการปรับปรุงได้นำเสนอไว้โดยเฉพาะในรายงานเลขที่ 1062 โดยมีเนื้อหาหลัก 06 ประการ เนื้อหาเฉพาะ 10 ประการ และเนื้อหาอื่นๆ
หากเปรียบเทียบกับกฎหมายฉบับปัจจุบัน ร่างกฎหมายมีประเด็นพื้นฐานใหม่ 7 กลุ่ม ดังนี้
นโยบายของรัฐเกี่ยวกับผลิตภัณฑ์ยายังคงได้รับการพัฒนาให้สมบูรณ์แบบยิ่งขึ้น เป็นการสถาปนามุมมองของพรรคด้วยเป้าหมายที่จะพัฒนาอุตสาหกรรมยาของเวียดนามให้กลายเป็นอุตสาหกรรมแกนนำ ด้วยเหตุนี้ ร่างกฎหมายจึงได้เพิ่มบทบัญญัติที่สร้างสรรค์มากขึ้นหลายประการเมื่อเทียบกับกฎหมายการเภสัชกรรม พ.ศ. 2559 เพื่อดึงดูดการลงทุนและส่งเสริมการวิจัยและพัฒนาการผลิตยาและส่วนประกอบของยาให้มากขึ้น เช่น นโยบายที่ให้สิทธิพิเศษเกี่ยวกับขั้นตอนการบริหารเมื่อออกใบรับรองการลงทะเบียนจำหน่ายและใบอนุญาตนำเข้า นโยบายที่จะใช้กลไกการให้สิทธิพิเศษและการสนับสนุนจากกองทุนสนับสนุนเพื่อกิจกรรมทางวิทยาศาสตร์และเทคโนโลยีในการวิจัย พัฒนา การทดลองทางคลินิก การถ่ายทอดเทคโนโลยี การผลิตยาและส่วนประกอบทางเภสัชกรรม นโยบายการรักษาราคาและลดราคาสำหรับกลุ่มยาบางกลุ่มที่มีการถ่ายทอดเทคโนโลยีการผลิต นโยบายการเปลี่ยนแปลงทางดิจิทัลในกิจกรรมด้านเภสัชกรรม กำหนดขนาดโครงการในภาคเภสัชกรรมที่เข้าเกณฑ์ได้รับสิทธิประโยชน์และการสนับสนุนการลงทุนพิเศษ และมอบหมายให้รัฐบาลออกระเบียบรายละเอียดเพื่อให้แน่ใจว่ามีความเป็นไปได้และทำให้แนวนโยบายของรัฐเกี่ยวกับเภสัชกรรมและการพัฒนาอุตสาหกรรมเภสัชกรรมเกิดขึ้นจริง
การสร้างช่องทางทางกฎหมายสำหรับรูปแบบและวิธีการทางธุรกิจใหม่ๆ ซึ่งได้แก่ (i) การกำกับดูแลการจัดตั้งเครือร้านยาเป็นประเภทการจัดตั้งธุรกิจยาแบบแยกจากกัน เงื่อนไขทางธุรกิจ สิทธิและความรับผิดชอบในการจัดตั้งเครือร้านยา ร้านขายยาในเครือร้านยา โดยเฉพาะอย่างยิ่ง สิทธิในการหมุนเวียนยาและสิทธิในการหมุนเวียนผู้ที่รับผิดชอบด้านความเชี่ยวชาญด้านยาระหว่างร้านขายยาต่างๆ ในเครือร้านยา (ii) กฎระเบียบเกี่ยวกับการค้ายาและส่วนประกอบยาทางอีคอมเมิร์ซ โดยเฉพาะกฎระเบียบเสริมเกี่ยวกับเครื่องมือทางอิเล็กทรอนิกส์ ประเภทของยาและส่วนประกอบยาที่ได้รับอนุญาตให้ซื้อขายทางอีคอมเมิร์ซ เพิ่มเติมสิทธิและความรับผิดชอบของสถานประกอบการธุรกิจยาตามวิธีการนี้
กำหนดสิทธิและความรับผิดชอบของธุรกิจยาที่ลงทุนจากต่างประเทศไว้ในกฎหมาย เพื่อให้เกิดการประชาสัมพันธ์และความโปร่งใสในการบริหารจัดการของรัฐ
การขยายสิทธิของสถานประกอบการผลิต สถานประกอบการส่งออกและนำเข้า สถานประกอบการขายส่งยาและส่วนผสมยาให้สามารถจำหน่ายโดยตรงให้กับสถานพยาบาล สถานบำบัดยา สถานทดสอบ สถานวิจัยและฝึกอบรม และสถานที่อื่นๆ อีกหลายแห่ง อนุญาตให้สถานตรวจรักษาสามารถนำเข้ายามาเพื่อตอบสนองความต้องการการรักษาพิเศษของผู้ป่วยในสถานตรวจรักษาได้
ส่งเสริมการปฏิรูปขั้นตอนการบริหารงานในการขึ้นทะเบียนจำหน่ายยาและส่วนประกอบของยา เพื่อจำแนกยาและส่วนประกอบของยาตามคุณสมบัติของยาแต่ละระดับ ตลอดจนการหมุนเวียนเพื่อปรับแก้ไขบันทึก ขั้นตอน ระยะเวลาในการอนุญาต ขยายเวลา เปลี่ยนแปลง และเพิ่มเติมใบรับรองการขึ้นทะเบียนจำหน่ายยาและส่วนประกอบของยาให้เหมาะสม เพื่อเพิ่มความสามารถในการเข้าถึงยาได้เร็วสำหรับประชาชน โดยยังคงรักษาประสิทธิภาพของการบริหารจัดการของรัฐ การควบคุมคุณภาพ ความปลอดภัย และประสิทธิผลของยา เพิ่มกฎเกณฑ์จำกัดการออกหมายเลขทะเบียนการจำหน่ายซ้ำ พร้อมกันนี้ยังมีกฎระเบียบเฉพาะเกี่ยวกับบันทึกและขั้นตอนการลงทะเบียนยา ส่วนประกอบของยา การทดสอบยา และการค้ายาโดยทั่วไปเพื่อตอบสนองข้อกำหนดด้านการป้องกันประเทศ ความมั่นคง ภัยธรรมชาติ ภัยพิบัติ และโรคระบาด
ยกเลิกขั้นตอนการยืนยันข้อมูลยา เสริมสร้างการกระจายอำนาจ การมอบอำนาจ ส่งเสริมบทบาทของกรมควบคุมโรค ในการเรียกคืนและจัดการยาที่ละเมิดคุณภาพในพื้นที่บริหารจัดการอย่างทันท่วงที เพื่อให้การใช้ยาเกิดความปลอดภัยและมีประสิทธิภาพ
กำหนดมาตรการบริหารราคาให้สอดคล้องกับพ.ร.บ.ว่าด้วยราคา และมีมาตรการเฉพาะในการบริหารราคาของยา คือ ประกาศและประกาศซ้ำราคาขายส่งคาดหวังที่ใช้กับยาที่ต้องสั่งโดยแพทย์ โดยให้การขายส่งยาผ่านตัวกลางไม่เกินราคาขายส่งคาดหวังที่ประกาศไว้
วีเอ็นเอ
ที่มา: https://baohanam.com.vn/chinh-tri/nguoi-dai-bieu-nhan-dan/quoc-hoi-chinh-thuc-thong-qua-luat-duoc-sua-doi-140545.html


![[ภาพ] เลขาธิการพรรคโตลัมเข้าร่วมการประชุมเพื่อทบทวนการดำเนินการตามคำสั่งหมายเลข 05 ของโปลิตบูโรในรอบ 10 ปี และประเมินผลลัพธ์ของการดำเนินการตามคำสั่งหมายเลข 09 ของคณะกรรมการพรรคความมั่นคงสาธารณะส่วนกลาง](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/19/2f44458c655a4403acd7929dbbfa5039)
![[ภาพ] ประธานาธิบดีเลือง เกวง มอบป้ายสมาชิกพรรคครบรอบ 40 ปี ให้แก่หัวหน้าสำนักงานประธานาธิบดีเล คานห์ ไห](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/19/a22bc55dd7bf4a2ab7e3958d32282c15)
![[ภาพ] ภาพพาโนรามาพิธีเปิดการแข่งขันเทเบิลเทนนิสชิงแชมป์แห่งชาติหนังสือพิมพ์หนานดาน ครั้งที่ 43](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/19/5e22950340b941309280448198bcf1d9)

![[ภาพ] ภาพระยะใกล้ของสะพาน Tang Long เมือง Thu Duc หลังจากซ่อมแซมร่องน้ำ](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/19/086736d9d11f43198f5bd8d78df9bd41)


















![[ภาพ] นายกรัฐมนตรี Pham Minh Chinh ตรวจสอบความคืบหน้าโครงการศูนย์นิทรรศการและการแสดงสินค้าแห่งชาติ](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/19/35189ac8807140d897ad2b7d2583fbae)




























































![[วิดีโอ] - เพิ่มมูลค่าผลิตภัณฑ์ OCOP ของกวางนามผ่านการเชื่อมโยงการค้า](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/5/17/5be5b5fff1f14914986fad159097a677)



การแสดงความคิดเห็น (0)