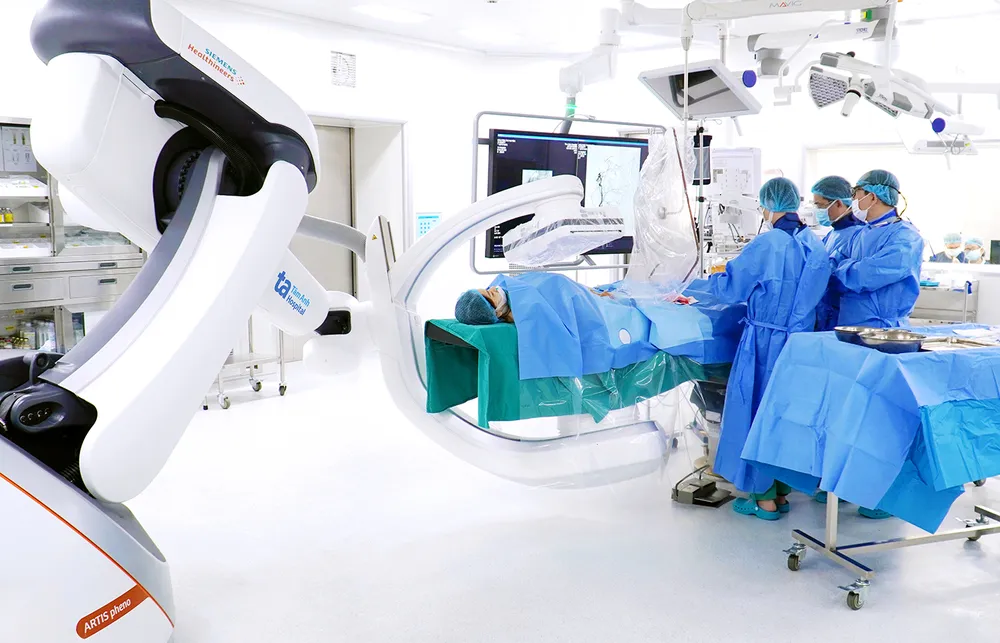
Lavere kostnader, flere behandlingsmuligheter.
Sent i desember 2024 lanserte Tam Anh Research Institute VISTA-1-prosjektet om oral immunterapi for kreftbehandling i Vietnam. Etter nesten seks måneder med gjennomføring av studien har åtte pasienter med endestadiet av kolorektalkreft behandlet i henhold til forskningsprotokollen i utgangspunktet ikke vist noen signifikante bivirkninger relatert til forskningslegemidlet og har vist lovende resultater.
Herr M. (50 år gammel), som var den første personen som testet legemidlet i dette prosjektet og led av kolorektal kreft som hadde metastasert til leveren, sa at han hadde gjennomgått ulike behandlingsregimer som cellegift og målrettet terapi, men uten hell. I januar 2025 registrerte han seg for å delta i studien og ble ansett som kvalifisert. «Jeg trodde jeg ikke hadde noen andre alternativer, men takket være denne muligheten til å delta i studien, føler jeg meg lettet og har mer håp», delte herr M.
Ifølge Dr. Vu Huu Khiem, leder for onkologisk avdeling ved Tam Anh General Hospital i Hanoi , ble pasientene som deltok i studien nøye overvåket for sikkerhet og respons på forskningslegemidlet. Forskningsteamet har ikke registrert noen uvanlige symptomer relatert til forskningslegemidlet hos pasienter som har brukt det de siste tre månedene.
«For pasienter med avansert kolorektalkreft som ikke lenger responderer på nåværende behandlingsregimer, er enhver forbedring i overlevelsestid under deltakelsen i denne studien av stor betydning. Vi og pasientene har nå gått inn i den fjerde måneden av denne forskningen», sa dr. Vu Huu Khiem.
Ved Ho Chi Minh City Oncology Hospital uttalte Dr. Phan Tan Thuan, leder for klinisk studieenhet, at enheten for tiden gjennomfører 37 kliniske studier, hovedsakelig i samarbeid med multinasjonale farmasøytiske selskaper (Pharma). Sykehuset samarbeider også proaktivt med regionale kreftsentre for å utføre uavhengig forskning med akademisk verdi og praktiske anvendelser. Sykehuset bruker ofte nye generasjons legemidler for sammenligning med standard behandlingsprotokoller. Mange av disse legemidlene er ennå ikke tilgjengelige i Vietnam og er svært dyre, og noen koster opptil 300 millioner VND per behandlingssyklus (3–4 uker). Pasienter som deltar i studiene får medisinen gratis, uavhengig av deres spesifikke behandlingsgren.
«I tillegg til å hjelpe pasienter med å få tilgang til moderne behandling tidligere, gjør disse studiene det også mulig for innenlandske fagfolk å beherske data og evaluere effektiviteten av legemidler på den vietnamesiske befolkningen. Dette forkorter tiden det tar å bringe nye legemidler ut på markedet. Mange nye generasjons legemidler er svært dyre. Her gir vi gratis tilgang til nye generasjons legemidler for alle pasienter som deltar i studien. Når forskningen er vellykket, kan det forkorte tiden det tar å bringe nye legemidler ut på markedet», forklarte dr. Phan Tan Thuan.
«Nylige kliniske studier har hjulpet helsevesenet med å raskt få tilgang til moderne behandlinger, fra tradisjonell cellegift til immunterapi og målrettede terapier. Disse fremskrittene bidrar ikke bare til å forlenge livet, men forbedrer også livskvaliteten for pasienter, samtidig som de utvider tilgangen til nye legemidler til lavere kostnader for pasienter og helsevesenet.»
Visehelseminister Nguyen Thi Lien Huong
Mye potensial, men mangel på mekanismer.
Ifølge professor Guy Thwaites, direktør for den kliniske forskningsenheten ved Oxford University, har Vietnam vært ledende innen malariamedisinstudier siden 1991, noe som har kommet millioner av pasienter globalt til gode. Med en befolkning på omtrent 100 millioner tilbyr Vietnam en mangfoldig pasientgruppe, ideell for kliniske studier. En gjennomsnittlig BNP-vekstrate på 6–7 % per år, kombinert med en voksende middelklasse, øker Vietnams attraktivitet for både innenlandske og internasjonale givere. Til tross for det store potensialet står markedet for kliniske studier i Vietnam fortsatt overfor flere barrierer som bremser utviklingen og skaper mangel på synkronisering. Godkjenningstiden for en klinisk studie i Vietnam kan være opptil 160 dager – den lengste i Asia, mens gjennomsnittstiden i andre land er rundt 75 dager. Videre henger Vietnam langt bak mange land i regionen, som Singapore (18 dager), Indonesia (20 dager), Japan (31 dager)... Denne tidsrammen påvirker det vietnamesiske markedets attraktivitet for forskningssponsorer.
Videre krever kliniske studier tett samarbeid mellom leger, sykepleiere, forskningskoordinatorer og dataansvarlige. Vietnam mangler imidlertid for tiden en velutdannet arbeidsstyrke; landet står også overfor økonomiske vanskeligheter og utilstrekkelige insentivmekanismer. En klinisk fase 3-studie kan koste mellom 10 og 20 millioner dollar. I mellomtiden har mange investorer rapportert at Vietnam mangler skatteinsentiver, forskningsfinansiering eller samfinansieringsmekanismer som ligner på de i Singapore og Sør-Korea. Utbetaling av finansiering blir ofte forsinket på grunn av administrative prosedyrer, noe som påvirker studienes fremdrift og reduserer konkurranseevnen sammenlignet med andre land i regionen.
For å utvikle sektoren for kliniske studier i Vietnam foreslår dr. Phan Tan Thuan å forenkle godkjenningsprosedyrene gjennom et sentralisert nettbasert system for å forkorte den nåværende komplekse godkjenningsprosessen. I tillegg bør nettbasert registrering via en engelskspråklig portal og tospråklig dokumentasjon implementeres for å effektivisere prosessen for internasjonale givere. For å konkurrere med andre land i regionen bør det utvikles preferansepolitikker som skattefritak, forskningsfinansiering eller samfinansieringsmekanismer for studiekostnader, i likhet med programmene i Singapore og Thailand.
«Vietnam bør fremme offentlig-private partnerskapsmodeller i klinisk forskning for å bidra til å dele risikoer og forbedre ressursene for bærekraftig industriutvikling. I tillegg til dette er det behov for politikk for å investere i infrastruktur, opprette flere testfasiliteter og utvide spesialiserte opplæringsprogrammer for personell gjennom samarbeid med universiteter og internasjonale organisasjoner», foreslo dr. Phan Tan Thuan.
Herr LUKE TRELOAR, leder for infrastruktur, offentlig sektor og helsevesen hos KPMG Vietnam: Utvikling av insentivpolitikk
Godkjenningsprosessen for kliniske studier i Vietnam involverer mange trinn. For det første tar det mellom 3 og 12 måneder å få godkjenning på lokalt nivå, avhengig av antall og plassering av studien. Deretter tar godkjenningsprosessen hos Helsedepartementet i gjennomsnitt 3 til 5 måneder. Til slutt tar det i gjennomsnitt 3 til 4 måneder å få en importlisens for legemidlet (for legemiddelstudier). Antallet kliniske studiesentre og studier i Vietnam er for lavt i forhold til befolkningen, og risikerer å falle akterut i kappløpet om å bli et regionalt klinisk forskningssenter. Vietnam trenger politikk for å investere i infrastruktur, bygge flere studiefasiliteter og utvide spesialiserte opplæringsprogrammer for personell gjennom samarbeid med universiteter og internasjonale organisasjoner. For å konkurrere med andre land i regionen må landet utvikle insentivpolitikk som skattefritak, forskningsfinansiering eller samfinansieringsmekanismer for studiekostnader, i likhet med programmene i Singapore og Thailand.
Herr Nguyen Ngo Quang, direktør for departementet for vitenskap, teknologi og opplæring (Helsedepartementet): Standardisering av kliniske studier.
I den kommende perioden vil Helsedepartementet fortsette å forbedre det juridiske rammeverket og standardisere kliniske studier i tråd med internasjonale standarder. Samtidig vil det styrke kapasiteten til Det nasjonale rådet for biomedisinsk forskningsetikk. Helsedepartementet ber for tiden om tilbakemeldinger på et utkast til rundskriv som beskriver forskrifter for kliniske legemiddelstudier. Dette rundskrivet vil spesifisere detaljene for kliniske legemiddelstudier, inkludert prinsipper, standarder, prosedyrer og ansvar knyttet til testing av legemidler på frivillige for å vurdere legemidlers sikkerhet og effekt, identifisere bivirkninger og studere legemidlers farmakokinetikk. I følge utkastet til rundskrivet må prinsippene for kliniske legemiddelstudier sikre vitenskapelig stringens, objektivitet, ærlighet, åpenhet og beskytte forskningsdeltakernes rettigheter.
MINH NAM - MINH KHA NG spilt inn
Kilde: https://www.sggp.org.vn/gian-nan-thu-nghiem-lam-sang-post802539.html



















































































































Kommentar (0)