Pakistanul investighează doi distribuitori ai medicamentului anticancerigen Avastin, produs de Roche în Elveția, după ce 12 pacienți diabetici au orbit după ce au primit injecții cu acest medicament. Avastin este, de asemenea, autorizat în Vietnam.
În Vietnam, la data de 27 septembrie, Administrația pentru Medicamente din Vietnam ( Ministerul Sănătății ) nu a primit niciun raport care să reflecte efectele secundare nedorite ale Avastinului legate de pierderea vederii de către pacienți după utilizarea Avastinului.
Administrația pentru Medicamente din Vietnam a primit un raport de la Reprezentanța F. Hoffmann La Roche Ltd. despre incident.
Mai exact, în Pakistan, aproximativ 12 pacienți și-au pierdut vederea după ce au folosit injecții furnizate de furnizorul ilegal Genius Pharmaceutical Service. Medicamentul era etichetat „Injecție cu Avastin 1,25 mg/0,05 ml”, ceea ce a dus la percepția falsă că ar fi un produs Roche.
Avastin de la Roche nu este aprobat pentru nicio utilizare oftalmică. Genius Pharmaceutical Service a furnizat/diluat/reambalat doza de 1,25 mg/0,5 ml în condiții insalubre și neaprobate.
Autoritățile pakistaneze investighează cauza contaminării. Printre cauzele posibile se numără sterilizarea inadecvată, flacoanele contaminate, seringile nesterilizate și abaterile de la procedurile standard de operare în timpul administrării.
În același timp, guvernul pakistanez a solicitat retragerea de pe piață a 3 loturi de Avastin 100mg/ml (H352B11, B7266B07, B7266B20) de la Roche și a tuturor medicamentelor furnizate de Genius Pharmaceutical Service.
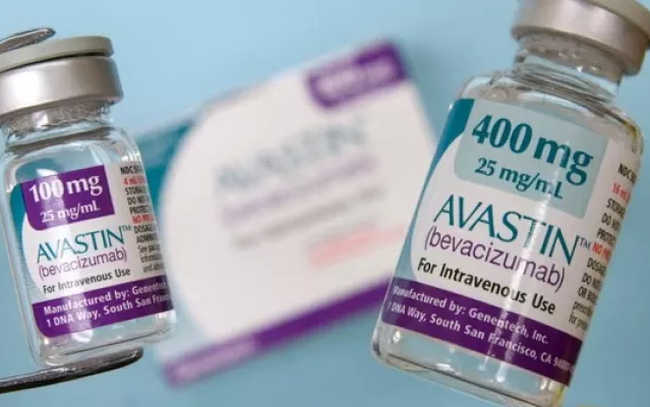
(Ilustrație: 24 News HD).
În Vietnam, medicamentul Avastin (ingredient activ Bevacizumab) a primit 4 certificate de înregistrare a circulației, toate fiind încă valabile. Printre acestea se numără:
Bevacizumab 100 mg/4 ml (cutie cu 1 flacon x 4 ml; număr de înregistrare: 400410250123 (QLSP-1118-18); producător: Roche Diagnostics GmbH, Germania).
Bevacizumab 400 mg/16 ml (cutie cu 1 flacon x 16 ml: număr de înregistrare: 400410250223 (QLSP-1119-18); producător: Roche Diagnostics GmbH, Germania).
Bevacizumab 100 mg/4 ml (cutie cu 1 flacon x 16 ml; număr de înregistrare: QLSP-1010-17; producător: F. Hoffmann-La Roche Ltd., Elveția).
Bevacizumab 400 mg/16 ml (Cutie cu 1 flacon x 16 ml; număr de înregistrare: QLSP-1011-17; producător: F. Hoffmann-La Roche Ltd., Elveția).
Avastin este autorizat în Vietnam pentru tratamentul anumitor tipuri de cancer, inclusiv cancerul colorectal metastatic, cancerul pulmonar fără celule mici, avansat, metastatic sau recurent, carcinomul renal avansat și/sau metastatic, glioblastom/gliom malign (stadiul IV OMS); cancer ovarian epitelial, cancer al trompelor uterine și cancer peritoneal primar.
Pe lângă avertismentele generale, prospectul aprobat de FDA include un avertisment privind „nu este destinat utilizării intravitroase”.
Mai exact, medicamentul poate provoca tulburări de vedere, iar în urma injectării intravitroase, o cale de administrare neaprobată pentru amestecurile de Avastin din flacoane destinate perfuziei intravenoase la pacienții cu cancer, au fost raportate cazuri individuale și grupuri de evenimente adverse oculare grave.
Aceste reacții includ infecție intraoculară, endoftalmită, uveită, dezlipire de retină, ruptură a epiteliului pigmentar retinian, glaucom, hemoragie intraoculară… Unele dintre aceste evenimente au dus la diferite grade de pierdere a câmpului vizual, inclusiv orbire permanentă .
Sursă







![[Foto] Președintele Luong Cuong îl primește pe secretarul de război al SUA, Pete Hegseth](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/02/1762089839868_ndo_br_1-jpg.webp)






































































































Comentariu (0)