Selon l'Administration des médicaments du Vietnam (ministère de la Santé), Femancia est produit par Me Di Sun Pharmaceutical Joint Stock Company (quartier An Loi, quartier Hoa Loi, ville de Ben Cat, province de Binh Duong (anciennement), maintenant rue An Loi, quartier Hoa Loi, ville de Ho Chi Minh).
Récemment, Femancia a été prescrit par de nombreux établissements médicaux pour traiter les patients souffrant d’anémie due à une carence en fer ou en acide folique et est vendu dans de nombreuses pharmacies à travers le pays.
En plus d'être indiqué dans les cas d'anémie ferriprive, ce médicament est également utilisé pour prévenir l'anémie chez les sujets ayant des besoins accrus en fer et en acide folique comme les femmes enceintes, les femmes qui allaitent, les personnes qui viennent de subir une intervention chirurgicale et les personnes atteintes de maladies graves qui sont en phase de convalescence.
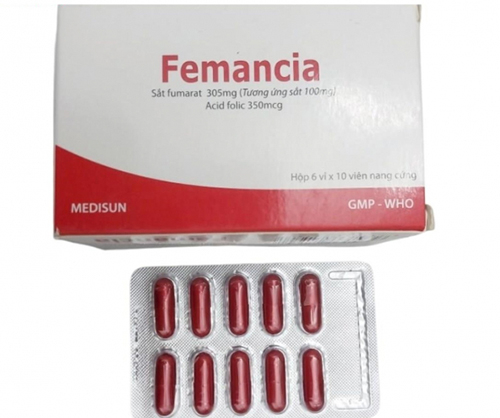
Cependant, après inspection et tests, les autorités ont découvert que le lot de médicament Femancia, numéro d'enregistrement VD-27929-17, forme posologique, capsule dure, fer élémentaire (sous forme de fumarate ferreux 305 mg) 100 mg, acide folique 350 mcg violait le niveau 2.
Afin d'assurer la sécurité des utilisateurs, l'Administration des médicaments du Vietnam ( ministère de la Santé ) a annoncé un rappel obligatoire de ce lot de médicaments à toutes les entreprises, établissements médicaux et utilisateurs.
Selon la circulaire 11/2018/TT-BYT du ministre de la Santé réglementant la qualité des médicaments et des ingrédients des médicaments, les médicaments de niveau 2 sont des médicaments dont il est prouvé qu'ils ne garantissent pas une efficacité thérapeutique complète ou qu'ils présentent un risque d'être dangereux pour les utilisateurs, mais pas au point de causer de graves dommages à la santé ou de ne pas affecter la vie de l'utilisateur.
L'Administration des médicaments du Vietnam exige que les établissements de commerce et d'utilisation de médicaments, les établissements d'examen et de traitement médicaux ne commercialisent, ne fournissent, ne distribuent ni n'utilisent Femancia et mettent en quarantaine tous les médicaments restants dans les établissements et retournent les médicaments aux établissements fournisseurs conformément à la réglementation.
Le Département de la Santé de Ho Chi Minh-Ville inspecte et supervise la société par actions pharmaceutique Me Di Sun pour rappeler et gérer le médicament Femancia rappelé susmentionné conformément à la réglementation ; en même temps, évaluer l'efficacité du rappel du médicament (le rappel est-il complet, le produit est-il susceptible de continuer à circuler, à être utilisé et présente-t-il un risque d'affecter négativement la santé des utilisateurs ou non).
En plus du retrait de l'enregistrement du médicament de la liste des médicaments bénéficiant d'un certificat d'enregistrement pour la circulation au Vietnam, l'Administration des médicaments du Vietnam a déclaré que Femanica ne serait pas produit et ne circulerait pas sur le marché à partir du 16 juillet.
Ces derniers temps, dans le cadre de la lutte contre la contrefaçon dans le secteur médical, de nombreux médicaments non conformes, voire contrefaits, ont été découverts. Selon l'Administration vietnamienne des médicaments, en juin, l'unité a inspecté 38 installations, dont 17 ont été reconnues comme non conformes, notamment aux principes des BPF, à la qualité des médicaments et aux conditions de stockage.
Le ministère a pris des décisions visant à suspendre temporairement la production, à demander la destruction de lots de médicaments de qualité inférieure, à rappeler et à cesser temporairement de recevoir des demandes d'un certain nombre d'entreprises.
Source : https://cand.com.vn/y-te/vi-sao-thuoc-dieu-tri-thieu-mau-femancia-bi-cam-san-xuat-luu-hanh--i775163/





























































































![[Infographie] En 2025, 47 produits obtiendront l'OCOP national](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/7/16/5d672398b0744db3ab920e05db8e5b7d)





Comment (0)