
"मिनी ब्रेन" का सफल विकास आधुनिक बायोमेडिकल इंजीनियरिंग और तंत्रिका विज्ञान में एक बड़ा कदम है - फोटो: एआई
एडवांस्ड साइंस पत्रिका में प्रकाशित एक लेख में, जॉन्स हॉपकिन्स विश्वविद्यालय (अमेरिका) की एक शोध टीम ने बताया कि ये तंत्रिका कोशिका समूह 40 दिन के मानव भ्रूण जितनी ही सक्रियता प्रदर्शित करते हैं। इससे पार्किंसंस और अल्ज़ाइमर जैसी तंत्रिका संबंधी बीमारियों के इलाज की नई संभावनाएँ खुलती हैं।
"कृत्रिम मस्तिष्क" वास्तविकता के करीब पहुँच रहे हैं
मानव मस्तिष्क ऑर्गेनॉइड कहे जाने वाले ये कोशिका समूह बहु-क्षमता वाले स्टेम कोशिकाओं से संवर्धित होते हैं, जिनमें मस्तिष्क के विभिन्न क्षेत्रों में विभेदित होने की क्षमता होती है। ये चेतन नहीं होते, लेकिन स्मृति और सीखने जैसे बुनियादी कार्य कर सकते हैं।
हाल के वर्षों में, 3D प्रौद्योगिकी के विकास के कारण, ये ऑर्गेनोइड्स न केवल बायोइलेक्ट्रिक गतिविधि का प्रदर्शन कर सकते हैं, बल्कि सरल रोबोट को भी नियंत्रित कर सकते हैं, या यहां तक कि पोंग जैसे बुनियादी वीडियो गेम भी खेल सकते हैं, जिसे कभी न्यूरोबायोलॉजी के क्षेत्र में चमत्कार माना जाता था।
हालाँकि, अब तक बनाए गए ज़्यादातर ऑर्गेनॉइड केवल मस्तिष्क के एक विशिष्ट क्षेत्र, जैसे सेरेब्रल कॉर्टेक्स, मिडब्रेन या सेरिबैलम, का अनुकरण करते हैं, लेकिन मस्तिष्क के क्षेत्रों द्वारा गतिविधियों के समन्वय के वास्तविक तरीके को पुन: प्रस्तुत नहीं करते हैं। अगर हम तंत्रिका-विकासात्मक या मानसिक विकारों का अध्ययन करना चाहते हैं, तो विज्ञान को एक ऐसे मॉडल की आवश्यकता है जो संपूर्ण मानव मस्तिष्क को क्रियाशील रूप में दर्शाए।
शोधकर्ता एनी कथूरिया के अनुसार, ऑटिज़्म का अध्ययन करने के लिए हम किसी व्यक्ति से उसके मस्तिष्क को देखने की अनुमति नहीं मांग सकते। लेकिन संपूर्ण-मस्तिष्क ऑर्गेनॉइड मॉडल हमें रोग प्रक्रिया की सीधे निगरानी करने, उपचारों की प्रभावशीलता का परीक्षण करने और यहाँ तक कि उपचार पद्धति को व्यक्तिगत बनाने में सक्षम बना सकते हैं।
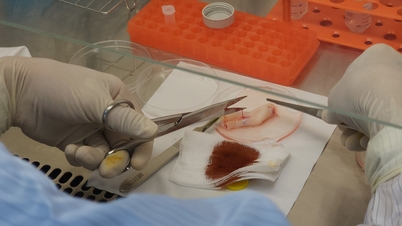
वर्षों के प्रयोगों के बाद, कथूरिया की टीम दुनिया की पहली बहु-क्षेत्रीय मस्तिष्क ऑर्गेनॉइड (एमआरबीओ) विकसित करने वाली टीमों में से एक बन गई। सबसे पहले, उन्होंने मानव मस्तिष्क के विभिन्न क्षेत्रों से न्यूरॉन्स और उनकी अंतर्निहित रक्त वाहिकाओं को अलग-अलग कल्चर डिश में संवर्धित किया। फिर इन क्षेत्रों को एक "बायो-सुपरग्लू" प्रोटीन का उपयोग करके जोड़ा गया, जो ऊतकों को एक-दूसरे से जुड़ने और परस्पर क्रिया करने में सक्षम बनाता है।
परिणामस्वरूप, मस्तिष्क के विभिन्न क्षेत्रों में समकालिक विद्युतीय गतिविधि उत्पन्न होने लगी, जिससे एक एकीकृत नेटवर्क का निर्माण हुआ। उल्लेखनीय रूप से, शोध दल ने रक्त-मस्तिष्क अवरोध (ब्लड-ब्रेन बैरियर) की प्रारंभिक उपस्थिति भी दर्ज की। यह कोशिकाओं की वह परत है जो मस्तिष्क को घेरे रहती है और मस्तिष्क में प्रवेश करने वाले पदार्थों को नियंत्रित करने में मदद करती है।
तंत्रिका संबंधी रोगों के उपचार में नए अवसर
यद्यपि ये मॉडल वास्तविक मानव मस्तिष्क से बहुत छोटे होते हैं, फिर भी प्रत्येक एमआरबीओ में केवल 6-7 मिलियन न्यूरॉन्स होते हैं, जबकि एक वयस्क में इनकी संख्या अरबों में होती है। हालाँकि, लगभग 80% कोशिकाएँ प्रारंभिक भ्रूण विकास की विशेषता रखती हैं, इसलिए ये मॉडल अभूतपूर्व विश्लेषणात्मक अवसर प्रदान करते हैं।
जॉन्स हॉपकिन्स टीम के अनुसार, एमआरबीओ का उपयोग जानवरों के बजाय मानव मॉडलों पर दवाओं के परीक्षण के लिए किया जा सकता है। वर्तमान में, 85-90% दवाएँ चरण 1 नैदानिक परीक्षणों में विफल हो जाती हैं, और तंत्रिका संबंधी रोगों के उपचार हेतु दवाओं के लिए यह दर 96% तक है, जिसका मुख्य कारण यह है कि पूर्व-नैदानिक अध्ययन चूहों या अन्य पशु मॉडलों पर अत्यधिक निर्भर होते हैं।
एमआरबीओ परीक्षण की ओर बढ़ने से प्रगति में तेजी लाने और सफलता दर में सुधार करने में मदद मिल सकती है।
शोधकर्ता एनी कथूरिया ने कहा, "अल्ज़ाइमर रोग, ऑटिज़्म और सिज़ोफ्रेनिया, ये सभी पूरे मस्तिष्क को प्रभावित करते हैं, न कि केवल एक क्षेत्र को। अगर हम यह समझ लें कि मस्तिष्क के विकास के शुरुआती चरणों में क्या होता है, तो हमें उपचार के लिए बिल्कुल नए लक्ष्य मिल सकते हैं।"
विशेषज्ञों का कहना है कि यह शोध आधुनिक बायोमेडिकल इंजीनियरिंग और तंत्रिका विज्ञान में एक बड़ा कदम है। जटिल ऑर्गेनॉइड मॉडल से, वैज्ञानिक व्यक्तिगत निदान और उपचार के चरण में आगे बढ़ सकते हैं, जहाँ प्रत्येक रोगी के पास दवाओं के प्रभावों का सटीक परीक्षण करने के लिए बनाया गया अपना मस्तिष्क मॉडल होगा।
इसके अलावा, भविष्य की संभावनाओं में मस्तिष्क-कंप्यूटर इंटरफेस और यहां तक कि जैविक ऑर्गेनोइड्स पर आधारित कृत्रिम बुद्धिमत्ता के लिए एक नई दिशा भी शामिल है।
स्रोत: https://tuoitre.vn/dot-pha-nuoi-cay-thanh-cong-nao-nguoi-thu-nho-20250729171444933.htm







![[फोटो] डैन माउंटेन जिनसेंग, किन्ह बाक भूमि के लिए प्रकृति का एक अनमोल उपहार](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F11%2F30%2F1764493588163_ndo_br_anh-longform-jpg.webp&w=3840&q=75)
































































































टिप्पणी (0)