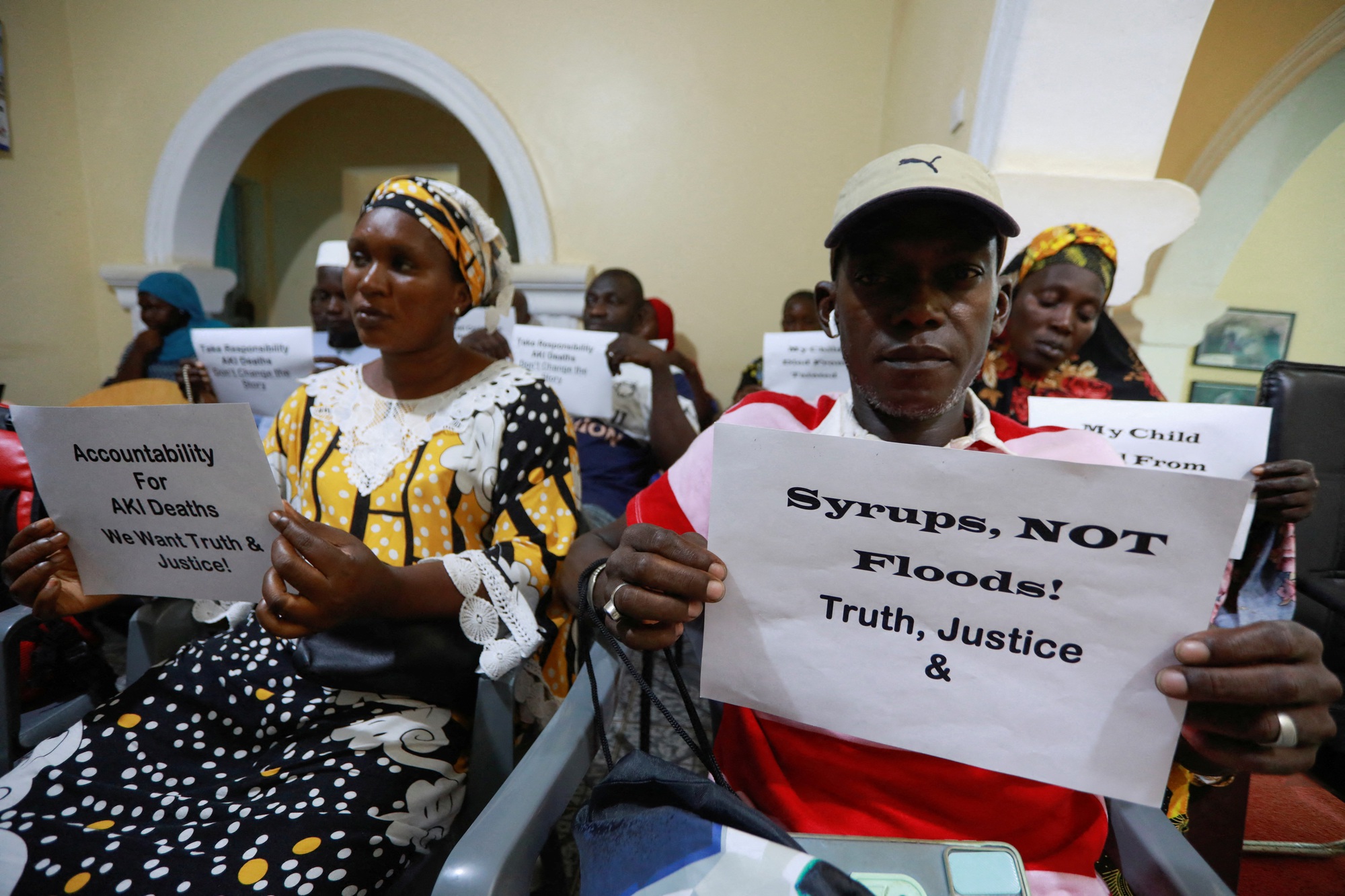
감비아에서 열린 기자회견에서 기침약 관련 질병으로 사망한 어린이들의 부모들
로이터는 7월 25일, 세계 보건 기구(WHO)가 지난 4월 마셜 제도와 미크로네시아에서 발견된 위험 성분이 포함된 기침약 제품에 대해 발표한 이후 인도가 제약 회사의 제조 허가를 정지했다고 보도했습니다.
인도 규제 당국은 인도에서 생산된 기침약이 작년에 감비아와 우즈베키스탄에서 최소 89명의 어린이 사망과 관련이 있는 것으로 밝혀지자 제약 회사를 조사하고 있습니다.
이러한 조치는 저렴한 의약품을 전 세계적으로 공급하는 " 세계 의 약국"으로서 인도의 이미지를 보호하기 위한 노력입니다.
기침약으로 아이 사망, 부모와 의사들 정부 조치 요구하며 격렬하게 투쟁
WHO는 QP Pharmachem Company(인도 펀잡에 본사 있음)의 기침 시럽에서 채취한 샘플에서 중독을 일으킬 수 있는 디에틸렌 글리콜과 에틸렌 글리콜이 허용 범위를 넘는 수준으로 검출되었다고 경고했습니다.
QP Pharmachem Ltd는 모든 주장을 부인했으며 정지 처분에 대해 항소할 계획이라고 밝혔습니다.
한편, 바라티 프라빈 파와르 보건부 차관은 의회에 보고하면서 제조 시설에서 채취한 약물 샘플은 "표준 품질이 아닌" 것으로 결론지어졌다고 밝혔습니다.
그녀는 당국이 QP Pharmachem Ltd와 아동 사망 사건과 관련된 제품을 생산하는 Maiden Pharmaceuticals와 Marion Biotech Pvt. Ltd.라는 두 회사의 제조 및 수출 허가를 정지했다고 덧붙였습니다.
QP Pharmachem CEO 수디르 파탁은 회사 생산이 중단되었음을 확인했습니다. 그는 시럽 생산을 시작하기 전에 성분을 테스트했다고 밝혔습니다.
그는 캄보디아에만 제품을 수출하고 있으며, 그 제품이 어떻게 마셜 제도와 미크로네시아에 도달할 수 있는지 모른다고 말했습니다.
인도는 6월부터 기침약 수출에 대한 검사를 강화했으며, 기업들이 수출하기 전에 정부 연구소에서 분석 인증서를 받도록 요구했습니다.
[광고_2]
소스 링크































![[사진] 국회의장, "국제금융센터 건설·운영 및 베트남에 대한 제언" 세미나 참석](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/7/28/76393436936e457db31ec84433289f72)




































































댓글 (0)