Printre cele peste 500 de medicamente și mărci originale cărora Administrația Medicamentelor din Vietnam le-a acordat numere de înregistrare noi și extinse pentru această dată, există 414 medicamente produse pe plan intern.

Știrile de la Ministerul Sănătății din 13 mai arată că Administrația pentru Medicamente tocmai a extins numerele de înregistrare pentru peste 500 de medicamente și medicamente specializate pentru licitație și tratament.
Dintre acestea, 414 medicamente produse pe plan intern au avut înregistrările de circulație prelungite pentru 5 ani (409 medicamente) și 3 ani (5 medicamente). În plus, au fost anunțate 68 de medicamente generice. Acesta este al treilea anunț de medicamente generice făcut de Ministerul Sănătății de la începutul anului.
Există 28 de medicamente și ingrediente farmaceutice cu certificate de înregistrare în circulație care pot fi utilizate în continuare în conformitate cu prevederile articolului 3, clauza 1, din Rezoluția Adunării Naționale nr. 80/2023/QH15 din 9 ianuarie 2023. Aceasta este a 13-a prelungire a Ministerului Sănătății pentru implementarea Rezoluției 80 a Adunării Naționale.
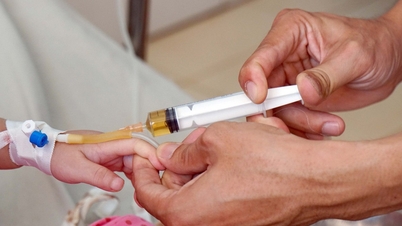
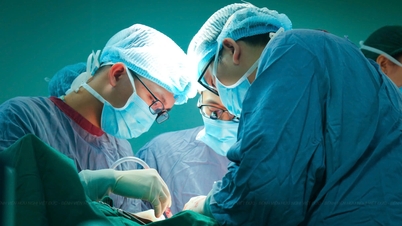
Produsele farmaceutice și produsele farmaceutice originale cărora li s-au acordat recent numere de înregistrare în circulație și cărora li s-au reînnoit numerele de înregistrare în ultima vreme sunt destul de diverse din punct de vedere al efectelor farmacologice, incluzând medicamente pentru tratarea cancerului, bolilor cardiovasculare, hipertensiunii arteriale, diabetului, medicamente antivirale, medicamente pentru tratarea bolilor respiratorii, antibiotice, antipiretice, analgezice, alte medicamente antiinflamatoare comune... și vaccinuri și produse biologice care sunt foarte solicitate pentru utilizare în examinări și tratamente medicale, precum și în prevenirea bolilor.
Ministerul Sănătății solicită ca unitățile de fabricare și înregistrare a medicamentelor să fie responsabile de fabricarea medicamentelor în conformitate cu înregistrările și documentele înregistrate la Ministerul Sănătății și să tipărească numărul de înregistrare emis de Ministerul Sănătății din Vietnam pe eticheta medicamentului.
Unitățile de producție au permisiunea de a fabrica și pune în circulație medicamente controlate special numai dacă dețin un Certificat de eligibilitate pentru activitatea farmaceutică, domeniul de activitate al medicamentelor controlate special este adecvat domeniului de activitate al unității, respectând prevederile articolului 143, clauza 5, din Decretul Guvernului nr. 54/2017/ND-CP din 8 mai 2017 care detaliază o serie de articole și măsuri pentru implementarea Legii privind farmacia.
Anterior, în martie și începutul lunii aprilie 2024, Ministerul Sănătății a emis noi emiteri, prelungiri și anunțuri pentru mii de medicamente produse pe plan intern, medicamente generice și medicamente și ingrediente farmaceutice, în temeiul Rezoluției 80 a Adunării Naționale (al 12-lea anunț de prelungire).
Sursă




![[Foto] Prim-ministrul Pham Minh Chinh prezidează a doua reuniune a Comitetului director pentru dezvoltarea economică privată.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/01/1762006716873_dsc-9145-jpg.webp)





































































































Comentariu (0)