En los últimos años, un cambio fundamental en nuestra comprensión del cáncer ha sido el descubrimiento de que los microorganismos no solo residen en el intestino, sino también en el tejido tumoral, incluyendo tumores sólidos como los de mama, próstata y pulmón. Estas comunidades microbianas (denominadas colectivamente microbioma intratumoral o microbioma asociado al tumor) interactúan directamente con las células cancerosas, las células inmunitarias y el entorno circundante, influyendo así en la biología del tumor, la respuesta al tratamiento y el pronóstico.
¿La microbiota del tejido tumoral es diferente de la microbiota intestinal?
Anteriormente se creía que el tejido tumoral era una «zona estéril», pero análisis genómicos y de secuenciación recientes han revelado la presencia de ADN/ARN microbiano en muchas muestras de tumores resecados. Estos microorganismos pueden residir dentro de las células cancerosas, dentro de las células inmunitarias o incrustados en el tejido conectivo circundante. La composición y la densidad de los microorganismos varían según el tipo de tumor y el paciente; por ejemplo, los tumores de mama presentan una diversidad microbiana relativamente alta en comparación con otros tumores. Su localización (intracelular o extracelular) determina cómo afectan al tejido enfermo.
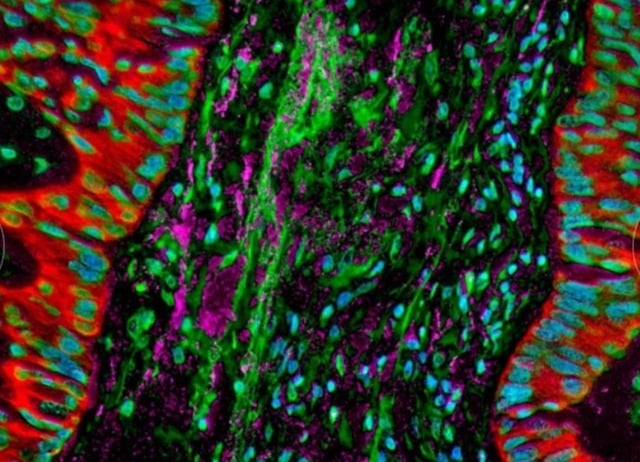
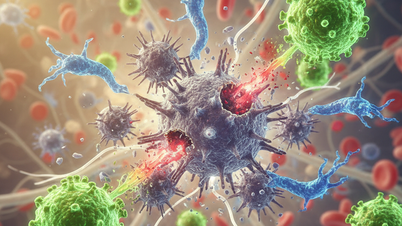
Las imágenes microscópicas muestran bacterias que residen en las células del cáncer de pulmón, alterando la respuesta inmunitaria del organismo.
El papel de las bacterias y los virus en el tejido mamario, prostático y pulmonar
La microbiota local puede modular el entorno inmunitario de forma supresora o activadora. Algunos microbios desencadenan señales inflamatorias crónicas (p. ej., mediante receptores de reconocimiento de patrones como los TLR), lo que conlleva un aumento de las citocinas proinflamatorias, que atraen células inmunitarias supresoras (macrófagos M2, Tregs), ayudando así a los tumores a evadir la respuesta inmunitaria. Por el contrario, algunas bacterias o virus pueden estimular la inmunidad celular (aumento de la presentación de antígenos, activación de linfocitos T CD8+) y contribuir a la eficacia de la inmunoterapia. Por lo tanto, la misma microbiota puede ser beneficiosa o perjudicial según el contexto.
Algunas bacterias producen toxinas o compuestos que dañan el ADN, causando mutaciones y promoviendo la progresión del cáncer. Por el contrario, otros microorganismos pueden inducir un metabolismo que reduce el crecimiento de las células tumorales. En el tejido mamario, diversos estudios han documentado la presencia de bacterias implicadas en vías inflamatorias y metabólicas; en la próstata, los cambios microbianos se asocian con la progresión de la enfermedad y la respuesta a la terapia antiandrogénica; y en el pulmón, el microbioma endógeno puede interactuar con la inflamación inducida por el tabaquismo y modificar el microambiente para que los tumores respondan menos a la inmunoterapia.
La presencia o composición del microbioma intratumoral puede alterar la eficacia de la quimioterapia, la radioterapia y, sobre todo, la inmunoterapia. Entre los mecanismos se incluyen alteraciones del microambiente (pH, nutrición), la inactivación local del fármaco (algunas bacterias poseen enzimas que lo degradan) o la modulación de la presentación de antígenos y la infiltración de células inmunitarias. Diversos estudios han demostrado que las diferencias en la microbiota tumoral se asocian con la respuesta o la resistencia a los inhibidores de puntos de control inmunitario (ICI).
Modificación local del microbioma en el tejido tumoral: estrategias existentes y en investigación
La idea de interferir directamente con el microbioma tumoral está abriendo nuevas vías de tratamiento. Algunos de los enfoques que se han desarrollado o se están desarrollando incluyen:
En algunos modelos experimentales, el uso de antibióticos para eliminar especies patógenas en tumores ha alterado la respuesta tisular a los fármacos. Sin embargo, los antibióticos sistémicos tienen efectos generalizados (y pueden alterar la microbiota intestinal necesaria para la inmunidad), por lo que el uso de antibióticos locales o el desarrollo de antibióticos selectivos para las especies objetivo es prioritario.
La idea consiste en introducir bacterias modificadas genéticamente en el tejido tumoral para que secreten citocinas inmunoestimulantes, enzimas metabólicas que alteren el pH o enzimas que degraden los inmunosupresores. Algunos ensayos preclínicos que utilizan bacterias atenuadas para administrar fármacos localmente han mostrado resultados prometedores.
Se han estudiado los virus oncolíticos para destruir directamente las células cancerosas y, simultáneamente, estimular la inmunidad antitumoral. La combinación de virus oncolíticos con la edición del microbioma podría potenciar la activación local de las células T y ampliar las respuestas sistémicas.
Aunque el tema que aquí se aborda es la microbiología local, es importante señalar que existe un eje intestino-tumor: las alteraciones del microbioma intestinal (por ejemplo, a través de la dieta, los probióticos o el trasplante de microbiota fecal) pueden alterar indirectamente el microbioma intratumoral y la inmunidad sistémica, influyendo así en el tejido tumoral del pulmón, la mama o la próstata.

Los científicos están analizando el ADN microbiano en el tejido tumoral para encontrar especies que influyan en la eficacia del tratamiento del cáncer.
Desafíos y consideraciones clínicas
- Distinguir entre "causa" y "efecto": muchos estudios actuales todavía describen correlaciones, pero no han confirmado una relación causal entre la microbiología y la progresión tumoral.
- Estandarización técnica: el muestreo, el aislamiento de ADN/ARN, la prevención de la contaminación exógena y el análisis bioinformático requieren estandarización para obtener resultados fiables.
- Gran variabilidad entre pacientes: el microbioma depende de cada individuo; las intervenciones deben ser individualizadas.
- Seguridad: La introducción de bacterias o virus vivos en el tejido tumoral conlleva un riesgo de infección o reacción inmunitaria excesiva; estas terapias requieren pruebas rigurosas.
El estudio del microbioma asociado a tumores abre una nueva dimensión en la biología oncológica: el microbioma local puede actuar tanto como promotor del cáncer como herramienta para la modulación inmunitaria y la administración dirigida de fármacos a los tumores. Gracias a los avances en secuenciación, histología, biomimética y técnicas de ingeniería del microbioma, en un futuro próximo se vislumbra que las estrategias terapéuticas dirigidas al microbioma local —desde bacterias bioingenierizadas y fagos selectivos hasta virus oncolíticos inmunocompetentes— se integrarán en la terapia multimodal.
Sin embargo, el camino clínico aún es largo; la estandarización de las pruebas, la demostración de la causalidad y la garantía de la seguridad serán requisitos previos antes de que estas intervenciones se adopten ampliamente.
Fuente: https://suckhoedoisong.vn/lieu-co-the-chua-ung-thu-bang-cach-dieu-chinh-vi-sinh-trong-mo-u-169251028135655078.htm





























































































![Transición de Dong Nai OCOP: [Artículo 3] Vinculación del turismo con el consumo de productos OCOP](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/11/10/1762739199309_1324-2740-7_n-162543_981.jpeg)












Kommentar (0)