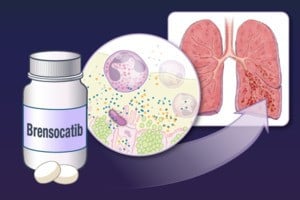
ການຕັດສິນໃຈດັ່ງກ່າວໄດ້ຖືກເຫັນວ່າເປັນບາດກ້າວອັນໃຫຍ່ຫຼວງຕໍ່ການດູແລສຸຂະພາບທາງເດີນຫາຍໃຈ, ຍ້ອນວ່າປະຈຸບັນບໍ່ມີການປິ່ນປົວທີ່ໄດ້ຮັບການອະນຸມັດສໍາລັບການນໍາໃຊ້ໂດຍກົງຕໍ່ກັບພະຍາດ.
NCFB ເປັນພະຍາດຊໍາເຮື້ອທີ່ທໍາລາຍເສັ້ນທາງຫາຍໃຈແລະຄ່ອຍໆຫຼຸດຜ່ອນການເຮັດວຽກຂອງປອດ, ເຮັດໃຫ້ເກີດອາການໄອຢ່າງຕໍ່ເນື່ອງ, ຫາຍໃຈສັ້ນແລະການຂັດຂວາງການໄຫຼວຽນຂອງອາກາດ. ມັນມັກຈະເກີດຈາກການອັກເສບແລະການຕິດເຊື້ອຊ້ໍາຊ້ອນ, ເຊິ່ງສາມາດເກີດຂື້ນໂດຍຫຼາຍໆສາເຫດ, ລວມທັງການຕິດເຊື້ອທາງເດີນຫາຍໃຈ, ພະຍາດ autoimmune ຫຼືຄວາມຜິດປົກກະຕິຂອງພູມຕ້ານທານ. ໃນສະຫະພາບເອີຣົບ, ຈໍານວນຄົນທີ່ມີ NCFB ຄາດຄະເນຢູ່ລະຫວ່າງ 400,000 ຫາ 3 ລ້ານຄົນ, ຊີ້ໃຫ້ເຫັນຄວາມຕ້ອງການອັນຮີບດ່ວນສໍາລັບການປິ່ນປົວທີ່ປອດໄພແລະປະສິດທິຜົນ.
ການອະນຸຍາດດ້ານການຕະຫຼາດຂອງ brensocatib ແມ່ນອີງໃສ່ການທົບທວນ ທາງວິທະຍາສາດ ໃນທາງບວກໂດຍອົງການຢາເອີຣົບ (EMA), ເຊິ່ງສະແດງໃຫ້ເຫັນເຖິງປະສິດທິພາບຂອງຢາໃນການຊັກຊ້າຄວາມຄືບຫນ້າຂອງພະຍາດແລະການຄວບຄຸມອາການຮ້າຍແຮງ. Brensocatib ເປັນຢາຕາມໃບສັ່ງແພດ, ຄວນຖືກນໍາໃຊ້ພາຍໃຕ້ການຊີ້ນໍາຂອງທ່ານຫມໍແລະອາດຈະເຮັດໃຫ້ເກີດຜົນຂ້າງຄຽງບາງຢ່າງ, ເຊິ່ງໄດ້ລະບຸໄວ້ຢ່າງເຕັມທີ່ໃນຂໍ້ມູນຜະລິດຕະພັນ. ຢາບໍ່ໄດ້ຖືກແນະນໍາໃຫ້ໃຊ້ໃນແມ່ຍິງຖືພາແລະຄວນຈະຖືກກໍານົດໄວ້ດ້ວຍຄວາມລະມັດລະວັງໃນກຸ່ມຄົນເຈັບພິເສດ.
Brensocatib ເຮັດວຽກໂດຍການດັດແປງການຕອບສະຫນອງອັກເສບໃນເສັ້ນທາງຫາຍໃຈ, ດັ່ງນັ້ນການຫຼຸດຜ່ອນຄວາມສ່ຽງຕໍ່ການຕິດເຊື້ອຄືນໃຫມ່. ການອະນຸມັດຂອງ EC ບໍ່ພຽງແຕ່ແກ້ໄຂຄວາມຕ້ອງການ ດ້ານການປິ່ນປົວ ທີ່ບໍ່ໄດ້ຮັບການຕອບສະຫນອງຫຼາຍປີ, ແຕ່ຍັງເປີດຄວາມເປັນໄປໄດ້ຂອງການປັບປຸງຄຸນນະພາບຊີວິດໄລຍະຍາວຂອງຄົນເຈັບທີ່ມີ NCFB, ຊ່ວຍໃຫ້ພວກເຂົາຄວບຄຸມອາການແລະຮັກສາກິດຈະກໍາປະຈໍາວັນຂອງເຂົາເຈົ້າ.
ທີ່ມາ: https://nhandan.vn/eu-cap-phep-thuoc-moi-dieu-tri-benh-phoi-man-tinh-nghiem-trong-post924109.html



![[ຮູບພາບ] ທ່ານປະທານປະເທດ ເລືອງເກື່ອງ ໄດ້ຮັບຕ້ອນທ່ານປະທານສະພາແຫ່ງຊາດ ສເກົາຫຼີ Woo Won Shik](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F11%2F21%2F1763720046458_ndo_br_1-jpg.webp&w=3840&q=75)
![[ຮູບພາບ] ທ່ານເລຂາທິການໃຫຍ່ To Lam ຕ້ອນຮັບປະທານສະພາສູງ ສເຊັກ Milos Vystrcil](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F11%2F21%2F1763723946294_ndo_br_1-8401-jpg.webp&w=3840&q=75)
![[ຮູບພາບ] ທ່ານປະທານສະພາແຫ່ງຊາດ Tran Thanh Man ເຈລະຈາກັບປະທານສະພາສູງ ສ.ເຊັກໂກ Milos Vystrcil](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F11%2F21%2F1763715853195_ndo_br_bnd-6440-jpg.webp&w=3840&q=75)
![[ຮູບພາບ] ໄປຢ້ຽມຢາມ Hung Yen ເພື່ອຊົມເຊີຍ "ພະຍາກອນໄມ້" ວັດຖຸບູຮານໃນໃຈກາງຂອງເຂດທົ່ງພຽງພາກເຫນືອ](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F11%2F21%2F1763716446000_a1-bnd-8471-1769-jpg.webp&w=3840&q=75)

































































































(0)