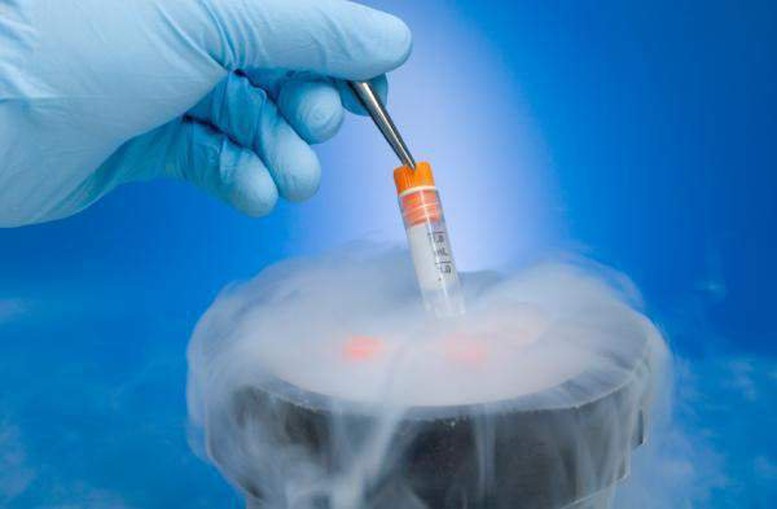
La instalación que recibe esperma, óvulos y embriones (muestras) es responsable de considerar los deseos del remitente/receptor de la muestra y de decidir aceptar muestras transferidas desde otras instalaciones de almacenamiento.
Esta Circular estipula las normas de salud para los receptores de esperma, óvulos y embriones; la entrega y recepción de esperma, óvulos y embriones entre instalaciones que almacenan esperma, óvulos y embriones; la lista mínima de técnicas de examen y tratamiento médico que deben realizar las instalaciones que realizan fertilización in vitro; informes estadísticos, gestión de datos e intercambio de información sobre apoyo reproductivo.
Normas sanitarias para los receptores de esperma, óvulos y embriones
De acuerdo con la Circular, la receptora de esperma, óvulos o embriones no debe padecer enfermedades o anormalidades de los órganos reproductivos hasta el punto de no poder quedar embarazada; enfermedades que puedan poner en peligro la vida de la mujer durante el embarazo; enfermedades mentales u otras enfermedades que le imposibiliten percibir o controlar su comportamiento.
Las personas con enfermedades agudas deben retrasar la transferencia de embriones hasta que el tratamiento sea estable.
El jefe del establecimiento que realice la fecundación in vitro o una persona legalmente autorizada es responsable de organizar y realizar los exámenes, consultas y concluir que las condiciones de salud son suficientes para recibir espermatozoides, óvulos y embriones de acuerdo a las normas anteriores.
Entrega y recepción de espermatozoides, óvulos y embriones entre instalaciones
Además, la Circular regula la entrega y recepción de espermatozoides, óvulos y embriones entre las instalaciones de almacenamiento de espermatozoides, óvulos y embriones.
En caso de que la persona que envía esperma, óvulos, embriones (en adelante denominados muestras) o la persona que recibe muestras donadas desee transferir las muestras del actual lugar de almacenamiento a otro lugar de almacenamiento:
El centro que conserva la muestra informa al remitente/receptor de la muestra donada sobre las normas para el transporte de la muestra, los riesgos que pueden encontrarse durante el proceso de transporte y cuenta con opiniones escritas sobre el acuerdo de transferencia de la muestra.
El centro de recepción de muestras es responsable de considerar los deseos del remitente/receptor de las muestras y de decidir si acepta muestras transferidas desde otras instalaciones de almacenamiento. La entrega y la recepción solo pueden realizarse con el consentimiento por escrito del centro de recepción de muestras.
El transporte de las muestras debe ser realizado por personal médico del centro receptor o del centro de entrega, con la participación del remitente/receptor de la muestra donada o de una persona legalmente autorizada. Si el remitente/receptor de la muestra donada o de una persona legalmente autorizada no está presente, el remitente/receptor deberá autorizar al centro receptor o al centro de entrega para que realice el transporte de la muestra.
El costo del transporte de la muestra corre por cuenta del remitente/receptor de la muestra donada. Durante el transporte, la muestra debe almacenarse en un congelador especializado y sellado junto al centro de entrega de muestras.
La instalación receptora de muestras es responsable de verificar el sello y los documentos adjuntos antes de firmar el acta de entrega de la muestra y devolver una copia original a la parte que realiza la entrega.
La presente Circular entra en vigor el 1 de octubre de 2025.
Minh Hien
Fuente: https://baochinhphu.vn/quy-dinh-tieu-chuan-suc-khoe-cua-nguoi-nhan-tinh-trung-noan-phoi-10225081416132671.htm






















![[Foto] La especial relación de solidaridad entre Vietnam y Cuba](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/8/15/5f06c789ab1647c384ccb78b222ad18e)
![[Foto] Marchando firmemente bajo la bandera militar: Listos para la gran fiesta](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/8/15/86df2fb3199343e0b16b178d53f841ec)





![[Foto] El puente Binh Khanh de Ciudad Ho Chi Minh está listo para llegar a la meta](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/8/14/b0dcfb8ba9374bd9bc29f26e6814cee2)



































































Kommentar (0)