ປາກິສຖານກໍາລັງສືບສວນສອງຜູ້ຈໍາຫນ່າຍຢາປິ່ນປົວມະເຮັງສະວິດ Roche Avastin ຫຼັງຈາກຄົນເຈັບທີ່ເປັນໂລກເບົາຫວານ 12 ຄົນໄດ້ຕາບອດຫຼັງຈາກໄດ້ຮັບການສັກຢາຢາ. Avastin ຍັງໄດ້ຮັບໃບອະນຸຍາດຢູ່ໃນຫວຽດນາມ.
ໃນວັນທີ 27 ກັນຍານີ້, ກະຊວງສາທາລະນະສຸກ ຫວຽດນາມ ຍັງບໍ່ທັນໄດ້ຮັບບົດລາຍງານໃດໆທີ່ສະແດງໃຫ້ເຫັນເຖິງຜົນກະທົບຂ້າງຄຽງທີ່ບໍ່ຕ້ອງການຂອງ Avastin ກ່ຽວກັບຄົນເຈັບເສຍວິໄສທັດຫຼັງຈາກການໃຊ້ Avastin.
ອົງການຢາເສບຕິດຂອງຫວຽດນາມໄດ້ຮັບລາຍງານຈາກຫ້ອງການຜູ້ຕາງໜ້າບໍລິສັດ F. Hoffmann La Roche Ltd. ກ່ຽວກັບເຫດການດັ່ງກ່າວ.
ໂດຍສະເພາະ, ໃນປະເທດປາກີສະຖານ, ຄົນເຈັບປະມານ 12 ຄົນໄດ້ສູນເສຍສາຍຕາຫຼັງຈາກໃຊ້ການສັກຢາທີ່ສະຫນອງໂດຍຜູ້ສະຫນອງທີ່ຜິດກົດຫມາຍ Genius Pharmaceutical Service. ຢາດັ່ງກ່າວຖືກຕິດສະຫຼາກ "Inj. Avastin 1.25mg/0.05ml" ເຮັດໃຫ້ເກີດຄວາມເຂົ້າໃຈຜິດວ່າມັນເປັນຜະລິດຕະພັນ Roche.
Roche's Avastin ບໍ່ໄດ້ຮັບການອະນຸມັດສໍາລັບການນໍາໃຊ້ ophthalmic ໃດໆ. Genius Pharmaceutical Service ສະໜອງ/ເຈືອຈາງ/ບັນຈຸຄືນໃໝ່ໃນປະລິມານ 1.25 ມກ/0.5 ມລ ພາຍໃຕ້ເງື່ອນໄຂທີ່ບໍ່ໄດ້ຮັບການອະນາໄມ ແລະ ບໍ່ໄດ້ຮັບການອະນຸມັດ.
ອຳນາດການປົກຄອງປາກິສຖານພວມສືບສວນຫາສາເຫດທີ່ພາໃຫ້ເກີດການປົນເປື້ອນດັ່ງກ່າວ. ສາເຫດທີ່ເປັນໄປໄດ້ລວມມີການຂ້າເຊື້ອບໍ່ພຽງພໍ, ຊ່ອງຄອດທີ່ປົນເປື້ອນ, ເຂັມສັກຢາທີ່ບໍ່ໄດ້ຂ້າເຊື້ອ ແລະ ຄວາມເສື່ອມເສີຍຈາກຂັ້ນຕອນການປະຕິບັດມາດຕະຖານໃນລະຫວ່າງການແຈກຢາຍ.
ໃນຂະນະດຽວກັນ, ລັດຖະບານປາກິສຖານໄດ້ຮຽກຮ້ອງໃຫ້ເອີ້ນຄືນ 3 ຊຸດຂອງ Avastin 100mg / ml (H352B11, B7266B07, B7266B20) ຂອງ Roche ແລະຢາທັງຫມົດທີ່ສະຫນອງໂດຍ Genius Pharmaceutical Service.
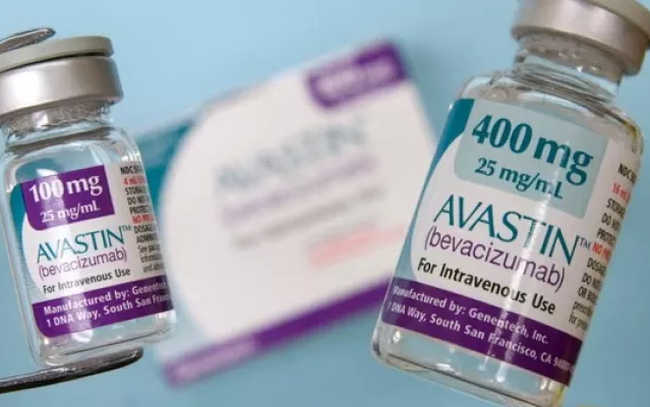
(ຮູບປະກອບ: 24 News HD).
ໃນປະເທດຫວຽດນາມ, ຢາ Avastin (ສານເສບຕິດ Bevacizumab) ໄດ້ຮັບໃບທະບຽນການໄຫຼວຽນຂອງ 4 ໃບ, ທັງໝົດແມ່ນຍັງຖືກຕ້ອງ. ລວມທັງ:
Bevacizumab 100mg/4ml (ກ່ອງ 1 vial x 4ml; ເລກທະບຽນ: 400410250123 (QLSP-1118- 18); ຜູ້ຜະລິດ: Roche Diagnostics GmbH, ເຢຍລະມັນ).
Bevacizumab 400mg/16ml (ກ່ອງ 1 vial x 16ml: ໝາຍເລກທະບຽນ: 400410250223 (QLSP-1119- 18); ຜູ້ຜະລິດ: Roche Diagnostics GmbH, ເຢຍລະມັນ).
Bevacizumab 100mg/4ml (ກ່ອງ 1 vial x 16ml; ໝາຍເລກທະບຽນ: QLSP-1010-17; ຜູ້ຜະລິດ: F. Hoffmann-La Roche Ltd., ສະວິດເຊີແລນ).
Bevacizumab 400mg/16ml (ກ່ອງຂອງ 1 vial x 16ml; ເລກທະບຽນ: QLSP-1011-17; ຜູ້ຜະລິດ: F. Hoffmann-La Roche Ltd., ສະວິດເຊີແລນ).
Avastin ໄດ້ຮັບໃບອະນຸຍາດໃນຫວຽດນາມສໍາລັບການປິ່ນປົວມະເຮັງບາງຊະນິດ, ລວມທັງມະເຮັງລໍາໄສ້ໃຫຍ່ metastatic, ກ້າວຫນ້າ, metastatic, ຫຼືມະເຮັງປອດທີ່ບໍ່ແມ່ນຈຸລັງຂະຫນາດນ້ອຍ recurrent, ກ້າວຫນ້າແລະ / ຫຼືມະເຮັງ renal renal cell carcinoma, glioblastoma / malignant glioma (WHO stage IV); ຮວຍໄຂ່ epithelial, ທໍ່ fallopian, ແລະມະເຮັງ peritoneal ຕົ້ນຕໍ.
ນອກເຫນືອໄປຈາກຄໍາເຕືອນທົ່ວໄປ, ການໃສ່ຊຸດທີ່ໄດ້ຮັບການອະນຸມັດຈາກ FDA ປະກອບມີຄໍາເຕືອນກ່ຽວກັບ "ບໍ່ແມ່ນສໍາລັບການນໍາໃຊ້ intravitreal."
ໂດຍສະເພາະ, ຢາອາດຈະເຮັດໃຫ້ເກີດການລົບກວນສາຍຕາ, ແລະກໍລະນີສ່ວນບຸກຄົນແລະກຸ່ມຂອງເຫດການທາງລົບຕໍ່ຕາທີ່ຮຸນແຮງໄດ້ຖືກລາຍງານຫຼັງຈາກການສັກຢາ intravitreal, ເສັ້ນທາງການບໍລິຫານທີ່ບໍ່ໄດ້ຮັບການອະນຸມັດດ້ວຍການປະສົມ Avastin ຈາກ vials ທີ່ມີຈຸດປະສົງສໍາລັບການສັກຢາທາງເສັ້ນເລືອດໃນຄົນເຈັບທີ່ເປັນມະເຮັງ.
ປະຕິກິລິຍາເຫຼົ່ານີ້ລວມມີການຕິດເຊື້ອທາງສາຍຕາ, endophthalmitis, uveitis, ຮອຍແຕກຂອງ retinal, ເມັດສີ retinal tear epithelial tear, glaucoma, intraocular hemorrhage… ບາງເຫດການເຫຼົ່ານີ້ສົ່ງຜົນໃຫ້ການສູນເສຍສາຍຕາທີ່ແຕກຕ່າງກັນ, ລວມທັງຕາບອດຖາວອນ .
ທີ່ມາ


![[ຮູບພາບ] ຄະນະກໍາມະການຂອງການຍຸຕິທໍາດູໃບໄມ້ລົ່ນ 2025 ກວດສອບຄວາມຄືບຫນ້າຂອງອົງການຈັດຕັ້ງ](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/10/20/1760918203241_nam-5371-jpg.webp)

![[ຮູບພາບ] ປະທານສະພາແຫ່ງຊາດຮັງກາຣີຢ້ຽມຢາມສຸສານປະທານໂຮ່ຈິມິນ](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/10/20/1760941009023_ndo_br_hungary-jpg.webp)
![[ຮູບພາບ] ທ່ານປະທານສະພາແຫ່ງຊາດ Tran Thanh Man ເຈລະຈາກັບປະທານສະພາແຫ່ງຊາດ ຮັງກາຣີ Kover Laszlo](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/10/20/1760952711347_ndo_br_bnd-1603-jpg.webp)

![[ພາບ] ໄຂກອງປະຊຸມສະໄໝສາມັນເທື່ອທີ 10, ສະພາແຫ່ງຊາດຊຸດທີ 15](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/10/20/1760937111622_ndo_br_1-202-jpg.webp)







































































































(0)