Пакистан ведёт расследование в отношении двух дистрибьюторов швейцарского противоракового препарата «Авастин» компании Roche после того, как 12 пациентов с диабетом ослепли после инъекций этого препарата. Препарат «Авастин» также лицензирован во Вьетнаме.
Во Вьетнаме по состоянию на 27 сентября Управление по контролю за лекарственными средствами Вьетнама ( Министерство здравоохранения ) не получало никаких сообщений, отражающих нежелательные побочные эффекты Авастина, связанные с потерей зрения у пациентов после применения Авастина.
Управление по контролю за наркотиками Вьетнама получило сообщение от представительства компании F. Hoffmann La Roche Ltd. об инциденте.
В частности, в Пакистане около 12 пациентов потеряли зрение после инъекций, поставляемых нелегальным поставщиком Genius Pharmaceutical Service. Препарат имел маркировку «Инъекции Авастина 1,25 мг/0,05 мл», что создавало ложное впечатление, будто это препарат компании Roche.
Препарат Авастин компании Roche не одобрен для офтальмологического применения. Компания Genius Pharmaceutical Service поставляла/разводила/переупаковывала дозу 1,25 мг/0,5 мл в антисанитарных и несанкционированных условиях.
Пакистанские власти расследуют причину заражения. Возможные причины включают недостаточную стерилизацию, загрязненные флаконы, нестерилизованные шприцы и отклонения от стандартных рабочих процедур при выдаче препарата.
В то же время правительство Пакистана потребовало отозвать 3 партии препарата Авастин 100 мг/мл (H352B11, B7266B07, B7266B20) компании Roche, а также все препараты, поставленные компанией Genius Pharmaceutical Service.
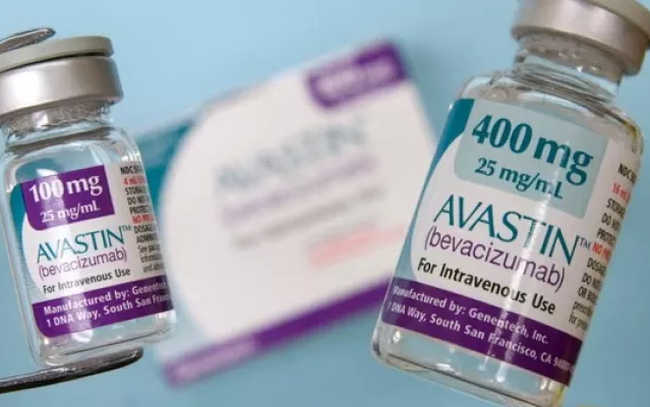
(Иллюстрация: 24 News HD).
Во Вьетнаме препарату Авастин (действующее вещество — бевацизумаб) выдано 4 свидетельства о регистрации в обращении, все из которых действительны. В том числе:
Бевацизумаб 100 мг/4 мл (упаковка 1 флакон x 4 мл; регистрационный номер: 400410250123 (QLSP-1118-18); производитель: Roche Diagnostics GmbH, Германия).
Бевацизумаб 400 мг/16 мл (упаковка 1 флакон x 16 мл: регистрационный номер: 400410250223 (QLSP-1119-18); производитель: Roche Diagnostics GmbH, Германия).
Бевацизумаб 100 мг/4 мл (коробка с 1 флаконом x 16 мл; регистрационный номер: QLSP-1010-17; производитель: F. Hoffmann-La Roche Ltd., Швейцария).
Бевацизумаб 400 мг/16 мл (упаковка 1 флакон x 16 мл; регистрационный номер: QLSP-1011-17; производитель: F. Hoffmann-La Roche Ltd., Швейцария).
Препарат Авастин лицензирован во Вьетнаме для лечения некоторых видов рака, включая метастатический колоректальный рак, запущенный, метастатический или рецидивирующий немелкоклеточный рак легких, запущенную и/или метастатическую почечно-клеточную карциному, глиобластому/злокачественную глиому (стадия IV по классификации ВОЗ), эпителиальный рак яичников, фаллопиевых труб и первичный рак брюшины.
Помимо общих предупреждений, в одобренном FDA листке-вкладыше к препарату содержится предупреждение: «не для интравитреального применения».
В частности, препарат может вызывать нарушения зрения, а отдельные случаи и группы серьезных нежелательных явлений со стороны глаз были зарегистрированы после интравитреальной инъекции — неутвержденного способа введения смесей Авастина из флаконов, предназначенных для внутривенного вливания онкологическим больным.
К таким реакциям относятся внутриглазная инфекция, эндофтальмит, увеит, отслоение сетчатки, разрыв пигментного эпителия сетчатки, глаукома, внутриглазное кровоизлияние... Некоторые из этих событий приводят к различной степени потери поля зрения, включая постоянную слепоту .
Источник



![[Фото] Генеральный секретарь То Лам принимает посла Сингапура Джаю Ратнам](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/03/1762171461424_a1-bnd-5309-9100-jpg.webp)
![[Фото] Премьер-министр Фам Минь Чинь принимает председателя Ассоциации японо-вьетнамской дружбы в регионе Кансай](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/03/1762176259003_ndo_br_dsc-9224-jpg.webp)
![[Фото] Лам Донг: крупный план незаконного озера с разрушенной стеной](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/03/1762166057849_a5018a8dcbd5478b1ec4-jpg.webp)

![[Фото] Осенняя ярмарка 2025 года и впечатляющие рекорды](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/03/1762180761230_ndo_br_tk-hcmt-15-jpg.webp)




































































































Комментарий (0)