פקיסטן חוקרת שני מפיצים של תרופת הסרטן אווסטין של חברת רוש השוויצרית, לאחר ש-12 חולי סוכרת עברו עיוורון לאחר שקיבלו זריקות של התרופה. אווסטין מורשה גם בווייטנאם.
בווייטנאם, נכון ל-27 בספטמבר, מינהל התרופות של וייטנאם ( משרד הבריאות ) לא קיבל דיווחים כלשהם המשקפים תופעות לוואי לא רצויות של אווסטין הקשורות לאובדן ראייה של חולים לאחר שימוש באווסטין.
מינהל התרופות של וייטנאם קיבל דיווח ממשרד הנציגות של חברת F. Hoffmann La Roche Ltd. על התקרית.
באופן ספציפי, בפקיסטן, כ-12 חולים איבדו את ראייתם לאחר שהשתמשו בזריקות שסופקו על ידי הספק הבלתי חוקי Genius Pharmaceutical Service. התרופה סומנה כ-Inj. Avastin 1.25mg/0.05ml", מה שגרם לתפיסה השגויה שמדובר במוצר של Roche.
אווסטין של רוש אינו מאושר לשימוש אופטלמי. חברת Genius Pharmaceutical Service סיפקה/מדללה/ארזה מחדש את המינון של 1.25 מ"ג/0.5 מ"ל בתנאים לא סניטריים ולא מאושרים.
הרשויות בפקיסטן חוקרות את סיבת הזיהום. בין הסיבות האפשריות ניתן למנות עיקור לקוי, בקבוקונים מזוהמים, מזרקים לא מעוקרים וסטיות מנוהלי פעולה סטנדרטיים במהלך מתן התרופות.
במקביל, ממשלת פקיסטן ביקשה את הקריאה לריקול של 3 מנות של אווסטין 100 מ"ג/מ"ל (H352B11, B7266B07, B7266B20) של חברת Roche וכל התרופות שסופקו על ידי חברת Genius Pharmaceutical Service.
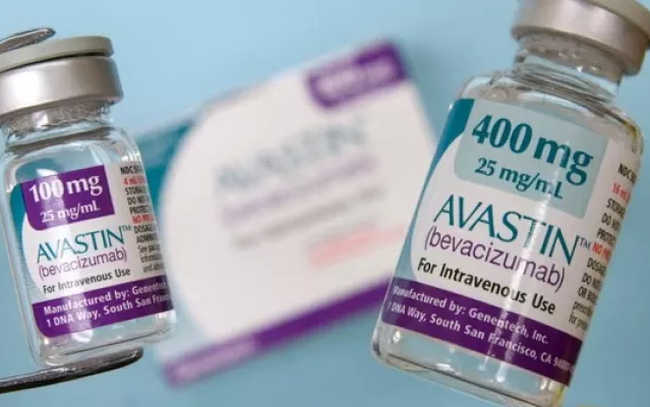
(איור: 24 חדשות HD).
בווייטנאם, התרופה אווסטין (החומר הפעיל בווציזומאב) קיבלה 4 תעודות רישום מסחר, שכולן עדיין בתוקף. ביניהן:
בווצ'יזומאב 100 מ"ג/4 מ"ל (קופסה של בקבוקון אחד x 4 מ"ל; מספר רישום: 400410250123 (QLSP-1118-18); יצרן: Roche Diagnostics GmbH, גרמניה).
בווצ'יזומאב 400 מ"ג/16 מ"ל (קופסה של בקבוקון אחד x 16 מ"ל: מספר רישום: 400410250223 (QLSP-1119-18); יצרן: Roche Diagnostics GmbH, גרמניה).
בווצ'יזומאב 100 מ"ג/4 מ"ל (קופסה של בקבוקון אחד x 16 מ"ל; מספר רישום: QLSP-1010-17; יצרן: F. Hoffmann-La Roche Ltd., שוויץ).
בווצ'יזומאב 400 מ"ג/16 מ"ל (קופסה של בקבוקון אחד x 16 מ"ל; מספר רישום: QLSP-1011-17; יצרן: F. Hoffmann-La Roche Ltd., שוויץ).
אווסטין מורשה בווייטנאם לטיפול בסוגי סרטן מסוימים, כולל סרטן המעי הגס והרקטום גרורתי, סרטן ריאות שאינו מסוג תאים קטנים מתקדם, גרורתי או חוזר, קרצינומה של תאי כליה מתקדמת ו/או גרורתית, גליובלסטומה/גליומה ממאירה (שלב IV של WHO); סרטן אפיתל של השחלות, סרטן החצוצרות וסרטן ראשוני של הצפק.
בנוסף לאזהרות הכלליות, עלון לצרכן שאושר על ידי ה-FDA כולל אזהרה בנוגע ל"לא לשימוש תוך-זגוגי".
באופן ספציפי, התרופה עלולה לגרום להפרעות ראייה, ומקרים בודדים ואשכולות של תופעות לוואי חמורות בעיניים דווחו לאחר הזרקה תוך-זגוגית, דרך מתן לא מאושרת של תערובות אווסטין מבקבוקונים המיועדים לעירוי תוך ורידי בחולי סרטן.
תגובות אלו כוללות זיהום תוך עיני, דלקת ריאות, דלקת ענביה, היפרדות רשתית, קרע באפיתל הפיגמנטי ברשתית, גלאוקומה, דימום תוך עיני... חלק מהאירועים הללו גרמו לדרגות שונות של אובדן שדה ראייה, כולל עיוורון קבוע .
[מודעה_2]
מָקוֹר


![[תמונה] לאם דונג: תקריב של אגם לא חוקי עם קיר שבור](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/03/1762166057849_a5018a8dcbd5478b1ec4-jpg.webp)










































































































תגובה (0)