 |
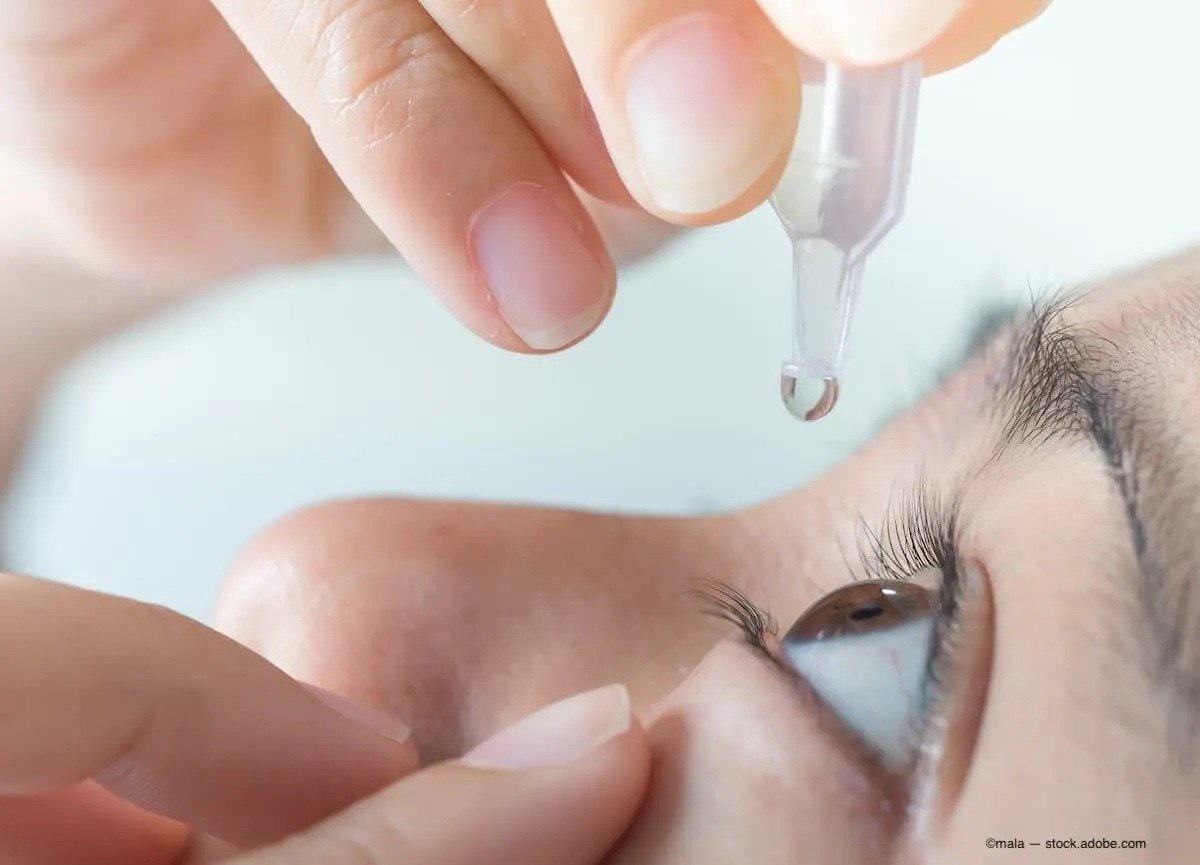
| 米国で、汚染された点眼薬による眼感染症が相次いで報告されています。(出典:AdobeStock/mala) |
深刻な結果
CDCの統計によると、5月18日現在、米国の18州で81人が感染し、5人が死亡(眼球摘出を余儀なくされた4人を含む)、14人が視力を失った。
緑膿菌は好気性グラム陰性桿菌であり、腸管感染症、尿路感染症、肺炎、皮膚炎など、ヒトにさまざまな種類の感染症を引き起こし、患者の傷口や手術切開部を攻撃して重度の敗血症を引き起こします。
緑膿菌は土壌や水などの自然環境に広く存在し、 医療現場でも広く蔓延しています。2017年には、米国で入院患者3万2000人以上が感染し、約2700人が死亡しました。
眼感染症の兆候としては、黄色、緑色、または透明の目やにが出る、目の痛みや不快感、目やまぶたの充血、異物感、光に対する過敏症、視界のぼやけなどが挙げられます。
CDCは現在、米国食品医薬品局(FDA)および州・地方の保健当局と協力し、この広範囲薬剤耐性緑膿菌(Pseudomonas aeruginosa)によるアウトブレイクの調査に取り組んでいます。VIM-GES-CRPAと呼ばれるこの新たなアウトブレイク株は、米国ではこれまで報告されていません。
CDCは特に懸念しており、汚染された点眼薬を使用する人から点眼薬を使用していない人へ緑膿菌が広がる可能性があると警告している。
品質基準を満たさない製品シリーズ
米国では、これらの感染症は10種類の点眼薬と関連付けられており、最も一般的なのはグローバル・ファーマ・ヘルスケア社のEzriCare人工涙液です。この点眼薬はEzriCareとDelsam Pharmaによって販売されています。
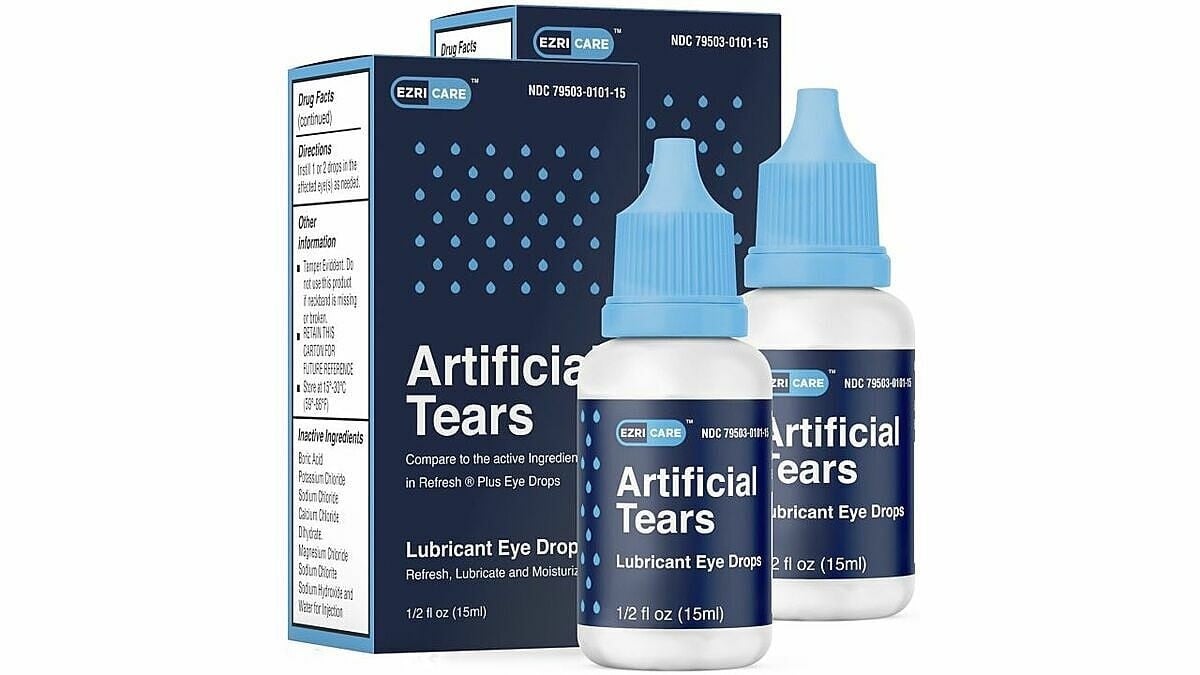 |
| EzriCare人工涙液ブランド。(出典:EzriCare) |
このアウトブレイクは、眼感染症を含む様々な感染症との関連が指摘されています。調査の結果、多くの患者においてエズリケア人工涙液が共通の曝露源となっていることが判明しました。
最も多く報告された汚染製品は、処方箋不要で複数回分ボトルに詰められた防腐剤不使用のEzriCare人工涙液だった。
CDCの研究所の検査により、米国の2つの州で眼感染症のある患者とない患者から採取された、異なるロットのEzriCareの開封済みボトルに、VIM-GES-CRPA菌が存在することが判明しました。
FDAは未開封のEzriCare人工涙液のボトルを検査し、この細菌による汚染も確認した。
FDAは、医療従事者と患者に対し、医薬品に関する合併症や品質問題をFDAのMedWatchプログラムに報告することを推奨しています。また、消費者はFDA消費者苦情コーディネーターに連絡して、医薬品の副作用を報告することもできます。
2月には、Global Pharma Healthcare社の人工涙液製品「EzriCare」が品質保証の不備によりリコールされた。
FDAの報告書によると、FDAはグローバル・ファーマの工場の生産工程を11日間にわたって検査した。その結果、2020年12月から2022年4月までの製品バッチの生産工程において、滅菌レベルが確保されていなかったことが判明した。
CDCの警告
CDCとFDAは、感染に関する情報を受けて、さらなるガイダンスが出るまで、医師はEzriCare人工涙液と、同じ製造業者が製造するDelsam Pharma人工涙液およびDelsam Pharma眼科軟膏の処方を中止し、患者は使用を中止して廃棄するよう勧告した。
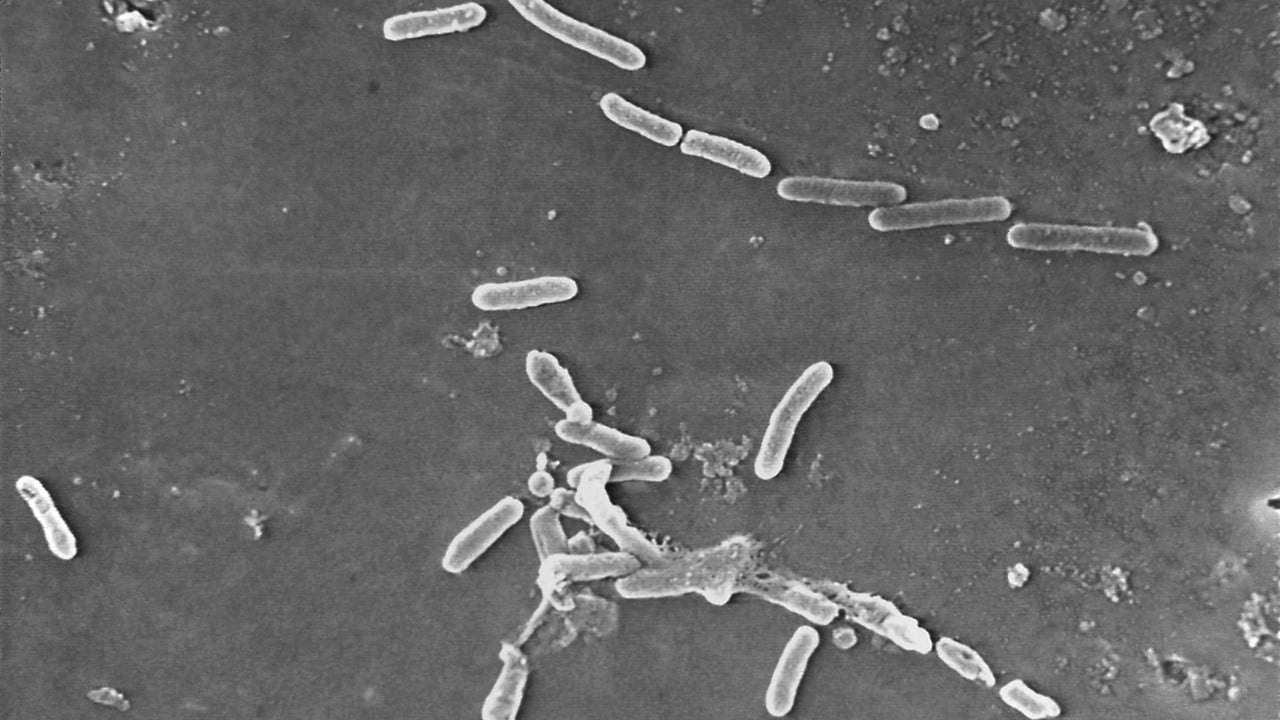 |
| 桿菌性緑膿菌の電子顕微鏡画像。(出典:米国CDC) |
CDCによると、このアウトブレイクに関連するVIM-GES-CRPA株は、セフェピム、セフタジジム、ピペラシリン-タゾバクタム、アズトレオナム、カルバペネム、セフタジジム-アビバクタム、セフトロザン-タゾバクタム、フルオロキノロン、ポリミキシン、アミカシン、ゲンタマイシン、トブラマイシンなどの薬剤に対して広範囲に耐性を示しました。
しかしながら、3つのVIM-GES-CRPA分離株のうち少数の株はセフィデロコールに感受性を示すようでした。しかしながら、臨床医は、この広範囲に耐性を示す菌に感染した患者の治療計画を決定するために、専門家に相談する必要があります。
医療現場でのこの細菌の拡散に関する懸念から、CDC は、医療現場でこの細菌が急速に拡散する可能性があるため、緑膿菌 VIM-GES-CRPA 感染症の患者を治療する医療従事者に対し、他の患者への交差感染を防ぐために感染制御の推奨事項に従うことを推奨しています。
CDC は、医療現場で VIM-GES-CRPA に感染した患者を隔離し、接触予防策を講じることを推奨しています。
[広告2]
ソース

































































































コメント (0)