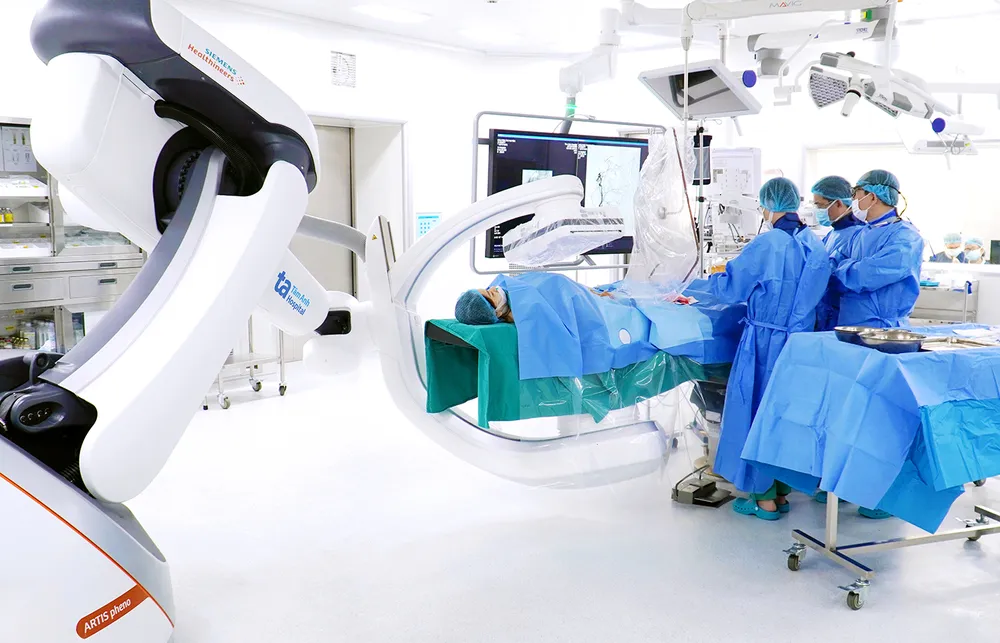
費用が安くなれば、治療の機会も増える。
2024年12月下旬、タムアイン研究所はベトナムでがん治療のための経口免疫療法に関するVISTA-1プロジェクトを開始しました。約6ヶ月間の治験実施後、研究プロトコルに従って治療を受けた末期大腸がん患者8名において、治験薬に関連する重大な副作用は初期段階では認められず、有望な結果が得られました。
このプロジェクトで最初にこの薬の試験を受けたM氏(50歳)は、肝臓に転移した大腸がんを患っており、化学療法や分子標的療法など様々な治療を受けてきたが効果がなかったと語った。2025年1月に治験への参加を登録し、適格と判断されたM氏は、「他に選択肢はないと思っていたが、この治験に参加できる機会を得られたことで、安心し、希望が持てるようになった」と述べた。
ハノイのタムアイン総合病院腫瘍科部長のヴー・フー・キエム医師によると、治験に参加した患者は、安全性と治験薬への反応について綿密にモニタリングされた。研究チームは、過去3か月間治験薬を使用した患者において、治験薬に関連する異常な症状は一切記録していない。
「現在の治療法に反応しなくなった進行性大腸がん患者にとって、この研究への参加期間中に生存期間が少しでも改善することは、非常に大きな意義があります。私たちも患者さんも、この研究が始まって4ヶ月目に入りました」と、ヴー・フー・キエム医師は述べています。
ホーチミン市腫瘍病院の臨床試験部門責任者であるファン・タン・トゥアン医師は、同部門が現在、主に多国籍製薬会社(Pharma)と共同で37件の臨床試験を実施していると述べた。同病院はまた、学術的価値と実用的応用性を備えた独自の研究を行うため、地域の癌センターと積極的に連携している。同病院では、標準治療プロトコルとの比較に新世代の薬剤を頻繁に使用している。これらの薬剤の多くはベトナムではまだ入手できず、非常に高価で、治療サイクル(3~4週間)あたり最大3億ベトナムドンかかるものもある。試験に参加する患者は、治療分野に関わらず、薬剤を無料で受け取ることができる。
「これらの研究は、患者さんがより早く最新の治療を受けられるようにするだけでなく、国内の医療従事者がデータを活用し、ベトナム国民に対する薬剤の効果を評価することを可能にします。これにより、新薬の市場投入までの時間を短縮できます。多くの新世代薬は非常に高価ですが、本研究では、研究に参加するすべての患者さんに新世代薬を無料で提供しています。研究が成功すれば、新薬の市場投入までの時間を短縮できるでしょう」と、ファン・タン・トゥアン医師は説明しました。
「近年の臨床試験により、 医療業界は従来の化学療法から免疫療法、標的療法に至るまで、最新の治療法を迅速に利用できるようになりました。これらの進歩は、患者の寿命を延ばすだけでなく、生活の質を向上させるとともに、患者と医療システムにとってより低コストで新薬へのアクセスを拡大することにも貢献しています。」
グエン・ティ・リエン・フオン保健副大臣
大きな可能性を秘めているが、それを実現する仕組みが不足している。
オックスフォード大学臨床研究ユニット所長のガイ・スウェイツ教授によると、ベトナムは1991年以来マラリア治療薬の臨床試験をリードしており、世界中の何百万人もの患者に恩恵をもたらしている。人口約1億人のベトナムは、臨床試験に理想的な多様な患者集団を提供している。年間平均6~7%のGDP成長率と拡大する中間層は、国内外のドナーにとってベトナムの魅力をさらに高めている。大きな可能性を秘めているにもかかわらず、ベトナムの臨床試験市場は、その発展を遅らせ、同期性の欠如を生み出すいくつかの障壁に直面している。ベトナムでの臨床試験の承認期間は最大160日にも及ぶことがあり、これはアジアで最も長い期間である。一方、他の国の平均期間は約75日である。さらに、ベトナムはシンガポール(18日)、インドネシア(20日)、日本(31日)など、この地域の多くの国に大きく遅れをとっている。この期間が、研究スポンサーにとってのベトナム市場の魅力に影響を与えている。
さらに、臨床試験には医師、看護師、研究コーディネーター、データマネージャー間の緊密な連携が不可欠です。しかし、ベトナムは現在、十分な訓練を受けた人材が不足しており、財政難や不十分なインセンティブ制度にも直面しています。第3相臨床試験には1,000万ドルから2,000万ドルの費用がかかる場合があります。一方、多くの投資家は、ベトナムにはシンガポールや韓国のような税制優遇措置、研究資金、共同融資制度が不足していると指摘しています。資金の交付は行政手続きのために遅れることが多く、試験の進捗に影響を与え、地域内の他国と比較して競争力を低下させています。
ベトナムにおける臨床試験分野の発展に向けて、ファン・タン・トゥアン博士は、現在の複雑な承認プロセスを短縮するため、中央集権型のオンラインシステムによる承認手続きの簡素化を提案している。さらに、国際的な資金提供者にとって手続きを効率化するため、英語ポータルを通じたオンライン登録と二言語対応の文書化を実施すべきである。地域内の他国との競争力を高めるため、シンガポールやタイのプログラムと同様に、税制優遇措置、研究資金、治験費用に対する共同出資制度といった優遇政策を策定する必要がある。
「ベトナムは、臨床試験研究における官民連携モデルを推進し、リスクの共有と持続可能な産業発展のための資源強化を図るべきです。それに加えて、インフラへの投資、検査施設の増設、大学や国際機関との連携による人材育成のための専門研修プログラムの拡充といった政策も必要です」と、ファン・タン・トゥアン博士は提言した。
KPMGベトナムのインフラ・政府・ヘルスケア部門責任者、ルーク・トレロア氏:インセンティブ政策の策定
ベトナムにおける臨床試験の承認プロセスは多くの段階を経る。まず、地方レベルでの承認取得には、研究の数と場所によって3~12ヶ月かかる。次に、保健省での承認プロセスには平均3~5ヶ月かかる。最後に、医薬品(治験用)の輸入許可の取得には平均3~4ヶ月かかる。ベトナムの臨床試験センターと研究の数は人口比で少なすぎるため、地域臨床研究センターとなる競争で後れを取るリスクがある。ベトナムは、インフラへの投資、より多くの治験施設の建設、大学や国際機関との協力による人材育成のための専門研修プログラムの拡充といった政策を必要としている。地域内の他国と競争するためには、シンガポールやタイのプログラムと同様に、税制優遇措置、研究資金、治験費用の共同融資制度といったインセンティブ政策を策定する必要がある。
グエン・ゴ・クアン保健省科学技術訓練局長:臨床試験活動の標準化。
今後、保健省は国際基準に沿って法的枠組みの精緻化と臨床試験活動の標準化を継続する。同時に、国家生物医学研究倫理評議会の能力強化を図る。現在、保健省は臨床薬物試験に関する規制を詳述した通達案について意見を募集している。この通達案では、薬物の安全性と有効性を評価し、副作用(ADR)を特定し、薬物の薬物動態を研究するためにボランティアに薬物を投与する際の原則、基準、手順、責任など、臨床薬物試験の詳細を規定する。通達案によれば、臨床薬物試験の原則は、科学的厳密性、客観性、誠実性、透明性を確保し、研究参加者の権利を保護するものでなければならない。
ミンナム - ミンカーンを記録しました
出典:https://www.sggp.org.vn/gian-nan-thu-nghiem-lam-sang-post802539.html

















































































































コメント (0)