Momenteel richten de meeste klinische onderzoeken in Vietnam zich op de ontwikkeling van nieuwe producten zoals geneesmiddelen, vaccins, medische apparatuur en nieuwe behandelmethoden. Met name de afgelopen jaren is er veel onderzoek gedaan naar celtherapie en gentherapie.
Klinische onderzoeken vereisen strenge goedkeuring en evaluatie voordat ze worden uitgevoerd, omdat het testproces, nieuwe producten en technieken risico's kunnen inhouden voor de vrijwilligers die aan het onderzoek deelnemen.
In werkelijkheid zijn er echter in de loop der jaren studies uitgevoerd op mensen, goedgekeurd door andere ministeries en instanties dan het Ministerie van Volksgezondheid , die niet waren goedgekeurd door de Biomedische Onderzoeksethische Commissie.
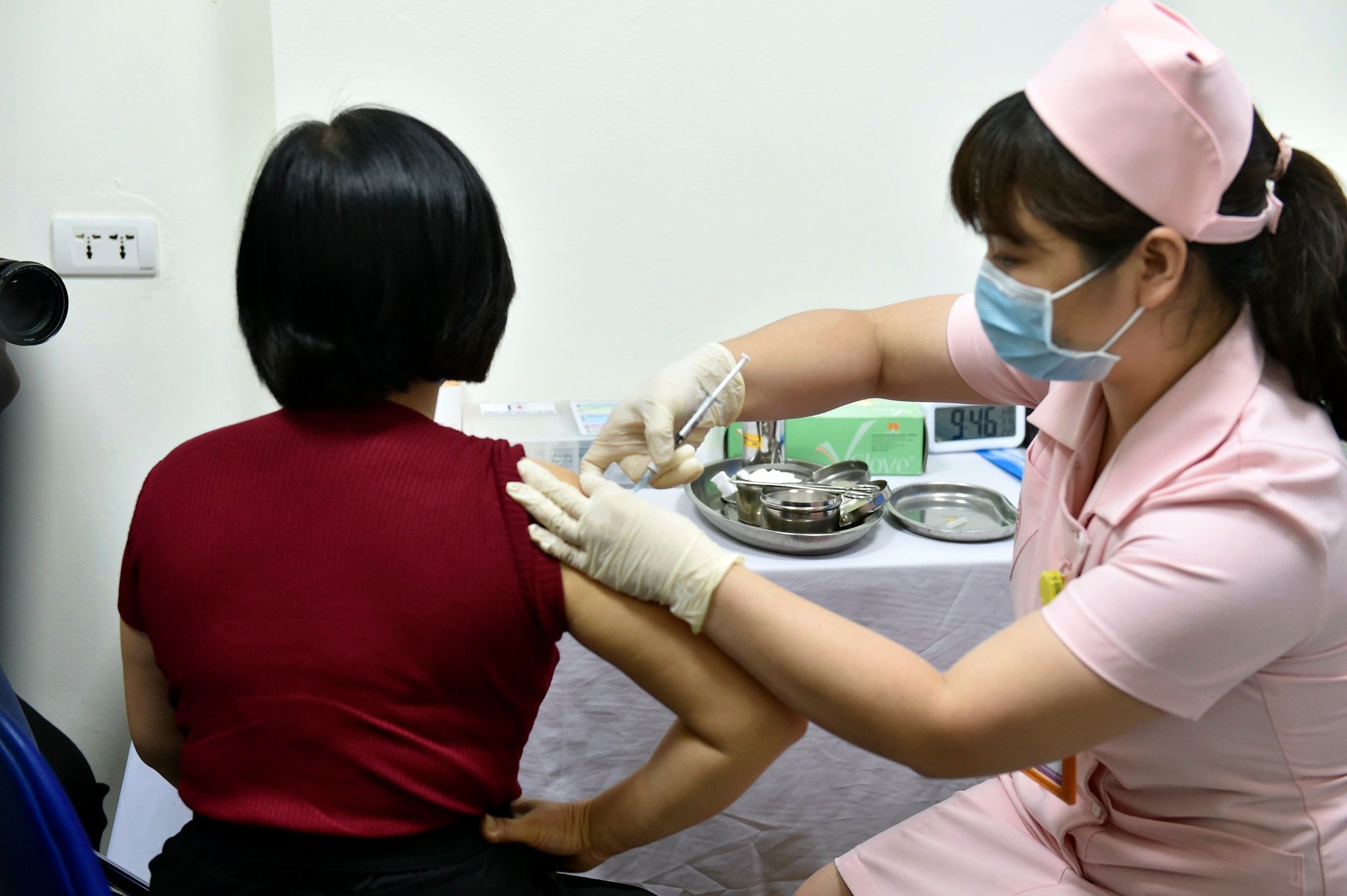
Injecties met het Covivac Covid-19-vaccin tijdens een proef in de Medische Universiteit van Hanoi , maart 2021.
Het Ministerie van Volksgezondheid vraagt om feedback op een conceptcirculaire die het beheer van wetenschappelijke en technologische taken onder haar verantwoordelijkheid regelt. Het concept stelt voor dat onderzoeksprojecten die gefinancierd worden uit niet-budgettaire bronnen of beheerd worden door andere ministeries en agentschappen, maar waarbij onderzoek met menselijke proefpersonen betrokken is, alleen mogen worden uitgevoerd na goedkeuring door de Biomedische Ethiekraad en formele goedkeuring door het Ministerie van Volksgezondheid. Tegelijkertijd benadrukt het concept de rol van lokale raden bij de goedkeuring van onderzoeksvoorstellen, het stroomlijnen van de goedkeuringstijden bij het Ministerie van Volksgezondheid en het waarborgen van de voortgang van het onderzoek.
In Vietnam worden jaarlijks ongeveer 100 klinische onderzoeken uitgevoerd, wat gunstige voorwaarden schept voor binnenlandse toegang tot nieuwe technologieën, producten en methoden in de behandeling en gezondheidszorg, met name voor complexe ziekten zoals kanker en hart- en vaatziekten. Wanneer nieuwe producten en technieken worden goedgekeurd, behoort Vietnam ook tot de eerste landen die er toegang toe krijgen, waaronder geneesmiddelen en vaccins. Voordat een product officieel wordt goedgekeurd, kan het klinische onderzoeksproces echter gezondheids- en levensrisico's met zich meebrengen voor de vrijwilligers; daarom zijn strenge goedkeurings- en monitoringprocedures gedurende het gehele implementatieproces cruciaal.
Volgens de huidige regelgeving is het Ministerie van Volksgezondheid verantwoordelijk voor het beheren, begeleiden en organiseren van de uitvoering van biomedisch onderzoek met menselijke proefpersonen. Voordat wetenschappelijke en technologische taken met betrekking tot biomedisch onderzoek met menselijke proefpersonen worden uitgevoerd, moet de leidende organisatie goedkeuring verkrijgen van de Biomedische Onderzoeksethische Commissie (zoals bepaald in Circulaire nr. 04/2020/TT-BYT).
Bronlink







![[Foto] Twee vliegtuigen zijn succesvol geland en opgestegen op de luchthaven van Long Thanh.](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F12%2F15%2F1765808718882_ndo_br_img-8897-resize-5807-jpg.webp&w=3840&q=75)



































































































Reactie (0)