Пакистан розслідує діяльність двох дистриб'юторів швейцарського препарату від раку Avastin від Roche після того, як 12 пацієнтів з діабетом втратили зір після ін'єкцій цього препарату. Avastin також ліцензовано у В'єтнамі.
Станом на 27 вересня Управління з контролю за лікарськими засобами В'єтнаму ( Міністерство охорони здоров'я ) не отримало жодних повідомлень про небажані побічні ефекти препарату Авастин, пов'язані з втратою зору у пацієнтів після його застосування.
Управління з контролю за лікарськими засобами В'єтнаму отримало повідомлення від представництва компанії F. Hoffmann La Roche Ltd. про інцидент.
Зокрема, у Пакистані близько 12 пацієнтів втратили зір після використання ін'єкцій, наданих нелегальним постачальником Genius Pharmaceutical Service. Препарат мав маркування «Inj. Avastin 1.25mg/0.05ml», що створювало хибне враження, що це продукт Roche.
Авастин від Roche не схвалений для будь-якого офтальмологічного застосування. Компанія Genius Pharmaceutical Service постачала/розводила/перепаковувала дозу 1,25 мг/0,5 мл в антисанітарних та недозволених умовах.
Пакистанська влада розслідує причину забруднення. Серед можливих причин – недостатня стерилізація, забруднені флакони, нестерилізовані шприци та відхилення від стандартних операційних процедур під час видачі ліків.
Водночас уряд Пакистану звернувся з проханням про відкликання 3 партій препарату Авастин 100 мг/мл (H352B11, B7266B07, B7266B20) компанії Roche та всіх препаратів, що постачаються компанією Genius Pharmaceutical Service.
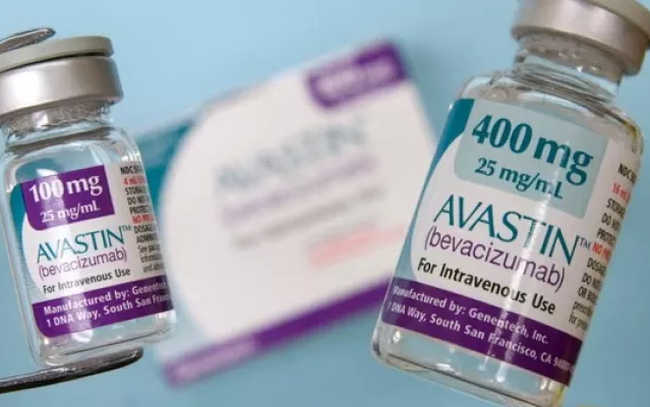
(Ілюстрація: 24 News HD).
У В'єтнамі препарат Авастин (діюча речовина Бевацизумаб) отримав 4 сертифікати реєстрації обігу, всі з яких досі дійсні. Включаючи:
Бевацизумаб 100 мг/4 мл (коробка з 1 флаконом х 4 мл; реєстраційний номер: 400410250123 (QLSP-1118-18); виробник: Roche Diagnostics GmbH, Німеччина).
Бевацизумаб 400 мг/16 мл (коробка з 1 флаконом х 16 мл: реєстраційний номер: 400410250223 (QLSP-1119-18); виробник: Roche Diagnostics GmbH, Німеччина).
Бевацизумаб 100 мг/4 мл (коробка з 1 флаконом х 16 мл; реєстраційний номер: QLSP-1010-17; виробник: F. Hoffmann-La Roche Ltd., Швейцарія).
Бевацизумаб 400 мг/16 мл (Коробка з 1 флаконом х 16 мл; реєстраційний номер: QLSP-1011-17; виробник: F. Hoffmann-La Roche Ltd., Швейцарія).
Авастин ліцензований у В'єтнамі для лікування деяких видів раку, включаючи метастатичний колоректальний рак, запущений, метастатичний або рецидивуючий недрібноклітинний рак легенів, запущену та/або метастатичну нирково-клітинну карциному, гліобластому/злоякісну гліому (стадія IV за класифікацією ВООЗ); епітеліальний рак яєчників, фаллопієвих труб та первинний рак очеревини.
Окрім загальних попереджень, схвалений FDA вкладиш містить попередження щодо «не для інтравітреального застосування».
Зокрема, препарат може спричиняти порушення зору, а також повідомлялося про окремі випадки та групи серйозних побічних ефектів з боку очей після інтравітреальної ін'єкції, що є несхваленим шляхом введення сумішей Авастину з флаконів, призначених для внутрішньовенної інфузії онкологічним хворим.
Ці реакції включають внутрішньоочну інфекцію, ендофтальміт, увеїт, відшарування сітківки, розрив пігментного епітелію сітківки, глаукому, внутрішньоочний крововилив… Деякі з цих подій призвели до різного ступеня втрати поля зору, включаючи постійну сліпоту .
Джерело


![[Фото] Президент Луонг Куонг приймає військового міністра США Піта Хегсета](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/02/1762089839868_ndo_br_1-jpg.webp)
![[Фото] Лам Донг: Зображення руйнувань після ймовірного прориву озера в Туй Фонг](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/02/1762078736805_8e7f5424f473782d2162-5118-jpg.webp)







































































































Коментар (0)