 |
Organoide – winzige dreidimensionale Zellstrukturen – werden seit Langem zur Erforschung von Krankheiten und zum Testen von Medikamenten eingesetzt. Allerdings fehlen den meisten Organoiden Blutgefäße, was ihre Größe, Funktion und Reifung einschränkt. Beispielsweise benötigen die Nieren Blutgefäße zur Blutfilterung und die Lunge zum Gasaustausch.
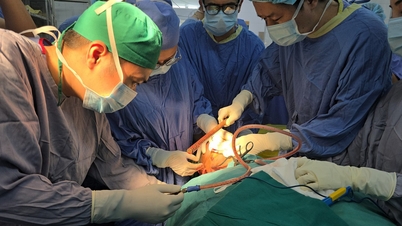
Letzten Monat veröffentlichten zwei unabhängige Forschungsteams in den Fachzeitschriften Science und Cell, wie man vaskularisierte Organoide von Grund auf herstellen kann. Sie begannen mit pluripotenten Stammzellen und manipulierten deren Differenzierung, um sowohl Organgewebe als auch Blutgefäßzellen zu erzeugen.
„Diese Modelle zeigen wirklich die Leistungsfähigkeit des neuen Ansatzes“, sagte Oscar Abilez, Stammzellenexperte an der Stanford University und Mitautor der Herz- und Leberstudie.
Anfangs mischten die Forschungsteams oft Blutgefäßgewebe und anderes Gewebe separat zu einem „Assembloid“ (einem Reagenzglasmodell, das viele Organoide oder andere Zellen kombiniert), aber dieser Ansatz reproduzierte die reale Struktur noch nicht vollständig.
Der Durchbruch gelang durch eine zufällige Entdeckung: Bei der Kultivierung von Epithelzellen stellten mehrere Forschungsgruppen, darunter die Universität Michigan, fest, dass Organoide spontan vermehrt vaskuläre Endothelzellen bilden. Anstatt diese zu eliminieren, versuchten sie, dieses Phänomen in Darmorganoiden nachzubilden.
Mit diesem Hinweis im Hinterkopf versuchten Yifei Miao und ihre Kollegen am Institut für Zoologie der Chinesischen Akademie der Wissenschaften , die gemeinsame Entwicklung von Epithelzellen und Blutgefäßzellen in derselben Kulturschale zu steuern. Anfänglich gestaltete sich dies schwierig, da die beiden Zelltypen für ihr Wachstum entgegengesetzte molekulare Signale benötigten. Dem Team gelang es jedoch, den Zeitpunkt der Zugabe stimulierender Moleküle so anzupassen, dass beide Zelltypen gemeinsam wachsen konnten.
Infolgedessen differenzierten sich die Lungenorganoide nach der Implantation in Mäuse in zahlreiche Zelltypen, darunter auch alveolenspezifische Zellen – die Orte des Gasaustauschs. Auf einem dreidimensionalen Gerüst gezüchtet, ordneten sie sich selbstständig zu alveolenähnlichen Strukturen an. Josef Penninger, Experte am Helmholtz-Zentrum für Infektionsforschung (Deutschland), bewertete dies als einen interessanten Fortschritt.
Abilez schuf auf ähnliche Weise Herzorganoide, die Muskelzellen, Blutgefäße und Nerven enthielten. Die Blutgefäße bildeten kleine Verzweigungen, die sich durch das Gewebe schlängelten. Mit diesem Ansatz entstanden auch Miniaturlebern mit vielen winzigen Blutgefäßen.
Aktuelle Organoide bilden jedoch nur die frühen Stadien der Embryonalentwicklung nach. Laut Penninger müssen Wissenschaftler größere Blutgefäße, Stützgewebe und Lymphgefäße entwickeln, damit Organoide wie echte Organe funktionieren. Die nächste Herausforderung besteht darin, die Gefäßklappen zu öffnen, damit tatsächlich Blut fließen kann. „Das ist ein unglaublich spannendes Forschungsgebiet“, sagt er.
Quelle: https://baoquocte.vn/dot-pha-noi-tang-nhan-tao-tu-hinh-thanh-mach-mau-320722.html






![[Foto] Dan-Berg-Ginseng, ein kostbares Geschenk der Natur an das Kinh-Bac-Land](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F11%2F30%2F1764493588163_ndo_br_anh-longform-jpg.webp&w=3840&q=75)































































































Kommentar (0)