این محصول توسط شرکت GAMMA Pharmaceutical - Cosmetic Production Company Limited توزیع میشود، پس از آنکه مشخص شد این محصول حاوی مواد اعلام نشده در ترکیبات خود است.
طبق اطلاعات مقامات، سری محصولات فراخوان شده دارای شماره سری GMPA010524، تولید شده در تاریخ ۲ مه ۲۰۲۴، با تاریخ انقضای ۲ مه ۲۰۲۷ است و با شماره رسید اعلام ۰۰۰۶۶۹/۲۱/CBMP-HCM صادر شده است.
 |
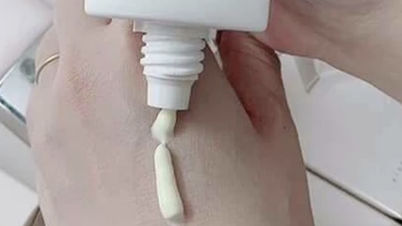
| عکس تصویرسازی. |
این محصول متعلق به شرکت داروسازی گاما - تولید لوازم آرایشی و بهداشتی با مسئولیت محدود (که قبلاً با نام شرکت خصوصی گاما برای تولید مواد شیمیایی آرایشی و بهداشتی شناخته میشد) است که دفتر آن در خیابان نگوین هائو شماره ۱۸، بخش تان تان، ناحیه تان فو، شهر هوشی مین و آدرس تولید آن در گروه ۱، هملت فو هیپ، کمون فو هوا دونگ، ناحیه کو چی، شهر هوشی مین قرار دارد.
نتایج آزمایش نمونه محصول که توسط مرکز آزمایش دارو، لوازم آرایشی و بهداشتی و مواد غذایی، اداره بهداشت استان ین بای، طبق گواهی آزمایش شماره 25L-020MP مورخ 17 ژوئن انجام شد، نشان داد که این محصول حاوی دو ماده نگهدارنده رایج در لوازم آرایشی، متیل پارابن و پروپیل پارابن، است.
با این حال، این دو ماده در فرمول محصول اعلام شده به مقامات اعلام نشده بودند و به طور جدی مقررات مربوط به اعلام مواد تشکیل دهنده لوازم آرایشی را نقض میکردند.
در پاسخ به تخلفات فوق، سازمان دارو درخواست تعلیق توزیع و فراخوان فوری این محصول در سراسر کشور را داد. در عین حال، از مشاغل و کاربران لوازم آرایشی درخواست کرد که فوراً فروش و استفاده از این سری پاککننده صورت را متوقف کرده و محصول را به تأمینکننده برگردانند.
این وزارتخانه همچنین از وزارت بهداشت استانها و شهرهای تحت مدیریت مرکزی درخواست کرد تا کسب و کارها و کاربران لوازم آرایشی در منطقه را از تصمیم تعلیق مطلع کنند و همزمان بازرسیها و نظارت بر فرآیند فراخوان و معدومسازی محصولات را انجام دهند و با متخلفان مطابق با مقررات جاری برخورد جدی کنند.
در مورد شرکت گاما، سازمان دارو از این شرکت میخواهد که اطلاعیه فراخوان را به تمام واحدهای توزیع و مصرف محصول ارسال کند؛ کالاها را از مؤسسات تجاری پس بگیرد؛ و کل سری محصولات متخلف را فراخوان و معدوم کند.
نتایج فراخوان و امحا باید قبل از ۲ آگوست ۲۰۲۵ به وزارتخانه گزارش شود. در عین حال، وزارتخانه همچنین رسید اظهارنامه محصول آرایشی با شماره ۰۰۰۶۶۹/۲۱/CBMP-HCM را طبق مفاد بند ب، ماده ۴۶، بخشنامه شماره ۰۶/۲۰۱۱/TT-BYT لغو میکند.
سازمان داروی ویتنام، وزارت بهداشت شهر هوشی مین را موظف کرد تا بر رعایت مقررات فراخوان و معدومسازی محصولات متخلف شرکت گاما نظارت و بازرسی کند و همزمان تخلفات در تولید و تجارت لوازم آرایشی این واحد را طبق قانون بررسی و رسیدگی نماید.
پیش از این، سازمان دارو نیز به دلیل نقض مقررات مربوط به مواد تشکیل دهنده و برچسب گذاری، تصمیم به تعلیق و فراخوانی بسیاری از محصولات آرایشی دیگر گرفته بود.
به طور خاص، ۷ محصول فراخوان شده وجود دارد که شامل موارد زیر است: ME LINE 01 Caucasian Skin، INNOAESTHTICS INNO-TDS Xeroskin-ID، کرم پاک کننده لکههای تیره INNOAESTHTICS INNO-DERMA 24H، لایه بردار قرمزی INNOAESTHTICS INNO-EXFO، INNOAESTHTICS INNO-EXFO TCAGE، INNOAESTHTICS INNO-EXFO Skin Recovery و ME LINE 02 Caucasian Skin Night.
این محصولات توسط شرکت داروسازی جهانی دونگ نام لیمیتد معرفی و توزیع شدهاند. این وزارتخانه از این شرکت درخواست کرد که تمام محصولات فروخته شده در بازار را جمعآوری کند و بررسی پرونده جدید اطلاعیه آرایشی این شرکت را به طور موقت به مدت 6 ماه به حالت تعلیق درآورد. پروندههای ارائه شده قبل از تصمیم تعلیق نیز دیگر معتبر نیستند.
علاوه بر این، دو محصول دیگر، آکوافرش سافت مینت و آکوافرش کلیر مینت، که توسط شرکت فات آنه مین لیمیتد منتشر شده بودند، نیز به دلیل نقض مقررات مربوط به برچسبگذاری لوازم آرایشی، از گردش مالی خود معلق شدند. سازمان دارو از وزارت بهداشت درخواست کرد تا روند جمعآوری این محصولات را از نزدیک رصد کند، تخلفات را به طور دقیق رسیدگی کند و گزارشها را برای سنتز و نظارت به وزارتخانه ارسال کند.
این اقدام قاطع با هدف تقویت کنترل کیفیت لوازم آرایشی و بهداشتی در بازار و تضمین ایمنی مصرفکنندگان انجام میشود. سازمان دارو توصیه میکند که سازمانها و افراد به استفاده، توزیع یا تجارت محصولات تعلیقشده ادامه ندهند.
مصرفکنندگان باید بهطور فعال با مسئولین در جمعآوری و معدومسازی لوازم آرایشی بیکیفیت همکاری کنند و به حفاظت از سلامت عمومی و محیط زیست کمک کنند.
منبع: https://baodautu.vn/sua-rua-mat-gammaphil-125ml-bi-thu-hoi-do-khong-dung-thanh-phan-theo-cong-bo-d329284.html
































































































![گذار دونگ نای OCOP: [ماده 3] پیوند گردشگری با مصرف محصولات OCOP](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/11/10/1762739199309_1324-2740-7_n-162543_981.jpeg)













نظر (0)