パキスタンは、ロシュ社の抗がん剤「アバスチン」の投与を受けた糖尿病患者12人が失明した事件を受け、販売業者2社を捜査している。アバスチンはベトナムでも承認されている。
ベトナムでは、9月27日現在、ベトナム医薬品管理局( 保健省)は、アバスチン使用後に患者の視力喪失に関連するアバスチンの望ましくない影響を反映する報告を受けていない。
ベトナム医薬品管理局は、F・ホフマン・ラ・ロシュ社の代表事務所からこの事件に関する報告を受けた。
具体的には、パキスタンで、違法な供給業者であるGenius Pharmaceutical Serviceから供給された注射剤を使用した後、約12人の患者が視力を失いました。この薬剤は「Inj. Avastin 1.25mg/0.05ml」とラベル表示されており、ロシュ社製品であるという誤った認識を引き起こしました。
ロシュ社のアバスチンは眼科用途として承認されていません。Genius Pharmaceutical Serviceは、1.25 mg/0.5 mlの用量を不衛生かつ未承認の条件下で供給、希釈、再包装しました。
パキスタン当局は汚染の原因を調査中です。原因としては、不適切な滅菌、汚染されたバイアル、未滅菌の注射器、薬剤調剤時の標準作業手順からの逸脱などが考えられます。
同時に、パキスタン政府はロシュ社のアバスチン100mg/ml(H352B11、B7266B07、B7266B20)3バッチとジーニアス・ファーマシューティカル・サービス社が供給するすべての医薬品の回収を要請した。
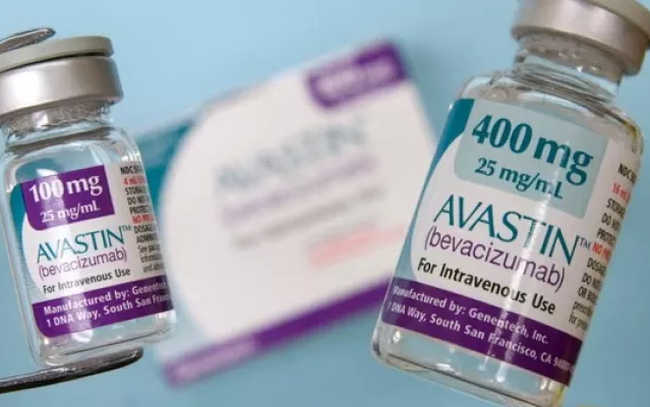
(イラスト:24 News HD)。
ベトナムでは、アバスチン(有効成分:ベバシズマブ)は4件の流通登録証を取得しており、いずれも現在も有効です。以下を含みます。
ベバシズマブ 100mg/4ml(1バイアル×4ml入り箱、登録番号:400410250123(QLSP-1118-18)、製造元:Roche Diagnostics GmbH、ドイツ)。
ベバシズマブ 400mg/16ml(1バイアル×16ml入り箱:登録番号:400410250223(QLSP-1119-18);製造元:Roche Diagnostics GmbH、ドイツ)。
ベバシズマブ 100mg/4ml(1バイアル×16ml入り箱、登録番号:QLSP-1010-17、製造元:F. Hoffmann-La Roche Ltd.、スイス)。
ベバシズマブ 400mg/16ml (1 バイアル x 16ml 入り箱、登録番号: QLSP-1011-17、製造元: F. Hoffmann-La Roche Ltd.、スイス)。
アバスチンはベトナムにおいて、転移性大腸がん、進行性、転移性または再発性の非小細胞肺がん、進行性および/または転移性の腎細胞がん、神経膠芽腫/悪性神経膠腫(WHOステージIV)、上皮性卵巣がん、卵管がん、原発性腹膜がんなどの特定のがんの治療薬として認可されています。
一般的な警告に加えて、FDA 承認のパッケージ挿入物には、「硝子体内に使用しないでください」という警告が含まれています。
具体的には、この薬剤は視覚障害を引き起こす可能性があり、がん患者への静脈内注入を目的としたバイアルからのアバスチン混合物の未承認の投与経路である硝子体内注射後に、重篤な眼の有害事象の個別症例および集団が報告されています。
これらの反応には、眼内感染症、眼内炎、ぶどう膜炎、網膜剥離、網膜色素上皮裂孔、緑内障、眼内出血などがあります。これらの事象の中には、永久的な失明を含む、さまざまな程度の視野欠損を引き起こすものもあります。
[広告2]
ソース


































































































コメント (0)