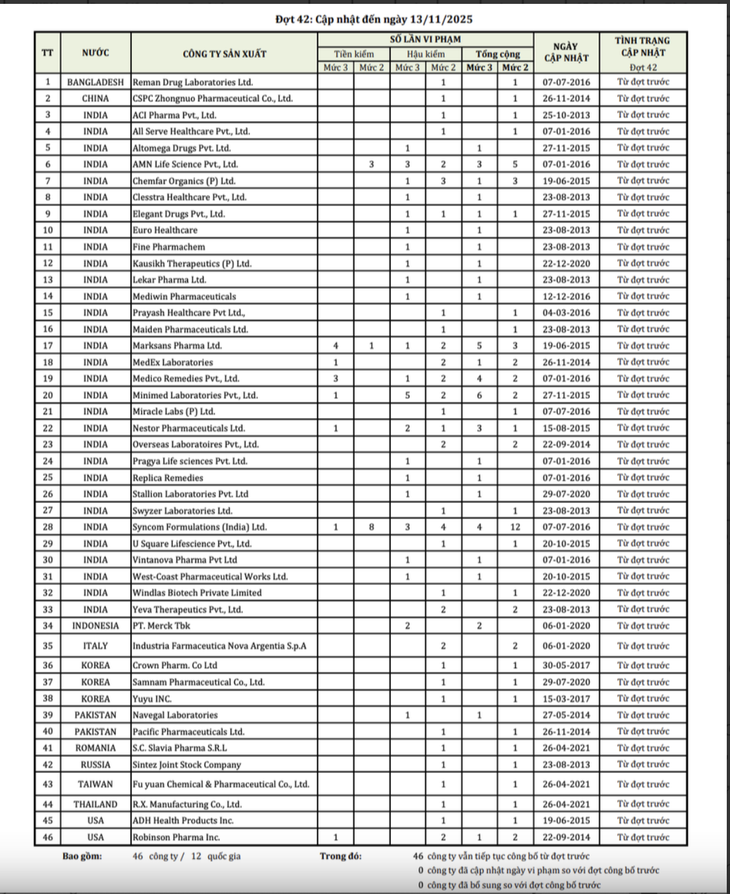
2025년 11월 13일 기준, 품질 규정을 위반한 약물을 보유한 46개 외국 제약 회사 목록 업데이트 - 사진: 미국 식품의약국(FDA)
12개국 46개 기업 모두 여러 번 재발한 사례였으며, 가장 많은 기업은 최대 12회까지 재발한 기업이었습니다.
베트남 약품 관리국은 방금 보건부의 규정을 이행하기 위해 각 성, 시의 보건부 와 약품 수입 회사에 문서를 보냈습니다. 이 규정은 품질이 낮은 약품을 제조하는 시설의 이름을 공표, 업데이트, 목록에서 삭제하는 내용을 담고 있습니다.
이에 따라, 식약처는 유통 중인 의약품의 품질 모니터링 결과, 위반 의약품이 있는 시설과 수입 의약품 100%의 품질 검사를 위한 샘플 채취 대상에서 제외될 수 있는 외국 의약품 제조 시설 등을 검토한 결과를 바탕으로, 위반 의약품이 있는 외국 기업 목록을 발표합니다.
따라서 이 목록에서 인도 기업은 여전히 가장 많은 위반 기업을 보유한 국가입니다. 2013년부터 2015년까지 나타난 여러 기업들은 현재까지 사전 검사 목록에 남아 있습니다.
인도의 대규모 집단 외에도 방글라데시, 중국, 인도네시아, 한국, 파키스탄, 미국, 이탈리아, 루마니아의 많은 기업도 계속해서 특별 감시를 받고 있습니다.
방글라데시의 리만 드럭 연구소, 중국의 CSPC 중누오, 인도네시아의 PT. 머크 Tbk, 한국의 크라운 파마와 유유는 모두 이전 배치에서 유죄 판결을 받았지만, 아직 사전 검사 해제 요건을 충족하지 못했습니다.
이 목록에는 ADH Health Products와 Robinson Pharma 등 2개 미국 기업이 포함되어 있으며, 이들 기업은 검사 전과 검사 후 모두 품질 위반 사항이 있습니다.
이 목록에 있는 회사는 수입 약물 배치의 100%에 대해 품질 테스트 샘플링을 실시해야 합니다(사전 검사).
식품의약품안전처는 위반 사항 목록 외에도 사전 검사 기간을 마친 후 16개국 98개 회사가 모니터링 목록에서 제외되었으며 새로운 위반 사항은 발생하지 않았다고 밝혔습니다.
베트남 약품감독관리국은 각 성, 시, 보건부 산하의 약품관리, 검사, 시험 부서에 관리 구역 내 유통되는 수입 약품에 대한 품질 검사 규정 준수 여부를 검사하고 감독하도록 지시하고, 현행 규정을 위반하는 기관/개인을 처리하도록 요구합니다.
출처: https://tuoitre.vn/danh-sach-46-cong-ty-duoc-nuoc-ngoai-co-thuoc-vi-pham-chat-luong-20251203160328166.htm



![[사진] 토람 사무총장, 러시아 연방 대통령 산하 공공행정 및 국민경제 아카데미 원장 접견](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F12%2F08%2F1765200203892_a1-bnd-0933-4198-jpg.webp&w=3840&q=75)











































































































댓글 (0)