Het nieuwe antibioticum werd ontdekt toen onderzoekers de werking van een oud medicijn bestudeerden. Daarbij stuitten ze op een tot dan toe onbekende stof.
De stof heeft het vermogen om ‘moeilijke’ bacteriestammen te doden, zoals meticilline-resistente Staphylococcus aureus (MRSA) en Enterococcus faecium, die ernstige infecties in ziekenhuizen veroorzaken en steeds moeilijker te behandelen zijn met de huidige medicijnen.
Het bijzondere is dat deze nieuwe verbinding is gemaakt van een bacteriesoort die in de bodem leeft. Hoewel van natuurlijke oorsprong, bezit deze verbinding uitstekende antibacteriële eigenschappen en is vele malen effectiever dan het oorspronkelijke antibioticum waar aanvankelijk onderzoek naar werd gedaan.
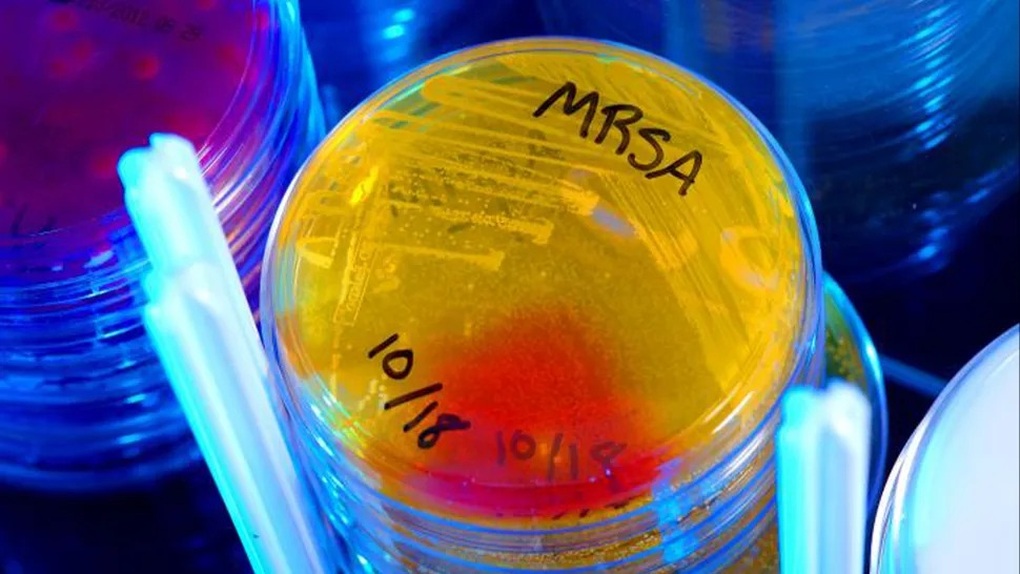
MRSA, een superbacterie die resistent is tegen medicijnen, infecteert vaak mensen die in het ziekenhuis worden verzorgd (foto: Melissa Dankel).
Van fundamenteel onderzoek tot ondergrondse ‘goudmijn’
Het onderzoeksteam, onder leiding van de wetenschappers Lona Alkhalaf en Greg Challis, begon hun werk met als doel het productiemechanisme van een bekend antibioticum genaamd methyleenomycine A te begrijpen.
Dit antibioticum wordt geproduceerd door de bodembacterie Streptomyces coelicolor. Ze waren niet op zoek naar nieuwe antibiotica, maar wilden begrijpen hoe bacteriën medicijnen maken.
Micro-organismen, waaronder bacteriën en schimmels, zijn in staat duizenden complexe verbindingen te produceren. Veel van deze verbindingen zijn inmiddels geneesmiddelen voor de mens geworden, zoals antibiotica, antikankermedicijnen en antiparasitaire middelen.
Door te begrijpen hoe deze verbindingen in de natuur ontstaan, kunnen wetenschappers nieuwe medicijnen ontwikkelen die effectiever zijn en minder bijwerkingen hebben.
In bacteriën worden biologische verbindingen vaak aangemaakt door specifieke groepen genen, zogenaamde biosynthetische genclusters. Het team schakelde een aantal van deze genen uit om te zien hoe de productie van methyleenomycine A verstoord werd.
Toen de reactie halverwege stopte, begonnen er tussenproducten te ontstaan, waaronder twee verbindingen die nog nooit eerder waren gerapporteerd.
Eén van de twee nieuwe verbindingen, genaamd pre-methyleenomycine C-lacton, toonde een zeer sterke antibacteriële activiteit bij tests tegen grampositieve bacteriestammen.
Deze stof doodt in het bijzonder effectief MRSA en Enterococcus faecium: twee soorten bacteriën die zeer moeilijk te bestrijden zijn omdat ze resistent zijn tegen veel gangbare medicijnen.
Uitstekende activiteit en anti-drug resistentie signatuur
Pre-methyleenomycine C-lacton is niet alleen ongeveer 100 keer krachtiger dan methyleenomycine A in het doden van bacteriën, maar het heeft ook nog een ander opmerkelijk voordeel.
Tijdens de proef van 28 dagen ontwikkelden de bacteriën geen resistentie tegen het nieuwe medicijn.
In de test werden Enterococcus faecium-bacteriën continu blootgesteld aan de nieuwe stof in toenemende doses. Dit zijn de ideale omstandigheden voor de bacteriën om te leren resistent te worden tegen het medicijn.
De resultaten lieten echter zien dat de minimale remmende concentratie gedurende de test onveranderd bleef. Dit betekent dat de verbinding zijn antibacteriële werking behield zonder dat de bacteriën "resistent" werden.
Dit is een belangrijke stap voorwaarts, omdat antibioticaresistentie veel infecties moeilijker te behandelen maakt dan ooit tevoren. Wanneer er een nieuw medicijn beschikbaar is waartegen bacteriën minder snel resistentie ontwikkelen, is dat een goed teken voor de geneeskunde.
Wetenschappers blijven echter voorzichtig. Er is een groot verschil tussen een stof die bacteriën in het laboratorium doodt en een medicijn dat daadwerkelijk in het veld wordt gebruikt, zegt chemicus Stephen Cochrane van Queen's University Belfast, die niet bij het onderzoek betrokken was.
"Een medicijn dat voor menselijk gebruik wordt goedgekeurd, moet aan veel criteria voldoen. Zo moet het niet-giftig zijn, stabiel in het lichaam en duidelijke klinische effecten hebben", aldus de onderzoeker.
Nieuwe wegen openen in de behandeling van medicijnresistente bacteriën
Nadat het team de mogelijkheden van pre-methyleenomycine C-lacton had ontdekt, wilde het de verbinding verder ontwikkelen tot een medicijn.
Ze werken nu samen met chemicus David Lupton van de Monash University in Australië om een manier te vinden om de verbinding in het laboratorium te synthetiseren in plaats van afhankelijk te zijn van bacteriën.
Als dat lukt, kunnen ze de stof in grote hoeveelheden produceren. Daarmee kan verder onderzoek worden gedaan naar de werking ervan en de effecten ervan op menselijke cellen.
Dit biedt ook de mogelijkheid om de chemische structuur van de stof aan te passen en zo varianten te creëren die krachtiger zijn of minder bijwerkingen hebben.
De volgende stap, zeggen de onderzoekers, is het identificeren van het biologische doelwit van de verbinding in bacteriën en analyseren hoe kleine veranderingen in de moleculaire structuur de antibacteriële effectiviteit kunnen verhogen of verlagen.
Die kennis vormt de basis voor de ontwikkeling van meer antibiotica binnen dezelfde groep. Zo krijgt de geneeskunde nieuwe wapens in de strijd tegen resistente bacteriën.
Hoewel er nog veel werk te verzetten is, suggereert de ontdekking dat de natuur nog veel geheimen te ontdekken heeft. In een tijd waarin veel medicijnen hun effectiviteit verliezen, is een nieuwe, effectieve en resistente stof wellicht precies waar de medische wereld op heeft gewacht.
Bron: https://dantri.com.vn/khoa-hoc/phat-hien-khang-sinh-manh-gap-100-lan-mang-hy-vong-moi-cho-y-hoc-20251110120120821.htm






![[Foto] Chu Noodles - de essentie van rijst en zonneschijn](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/11/1762846220477_ndo_tl_7-jpg.webp)
![[Foto] Premier Pham Minh Chinh leidt een vergadering over huisvestingsbeleid en de vastgoedmarkt.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/11/1762838719858_dsc-2107-jpg.webp)


























































































![Transformatie van Dong Nai OCOP: [Artikel 4] Het bereiken van nationale standaardproducten](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/11/11/1762825820379_4702-cac-san-pham-trai-cay-chung-nhan-ocop-nongnghiep-174649.jpeg)


![Dong Nai OCOP-transitie: [Artikel 3] Toerisme koppelen aan OCOP-productconsumptie](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/11/10/1762739199309_1324-2740-7_n-162543_981.jpeg)






Reactie (0)