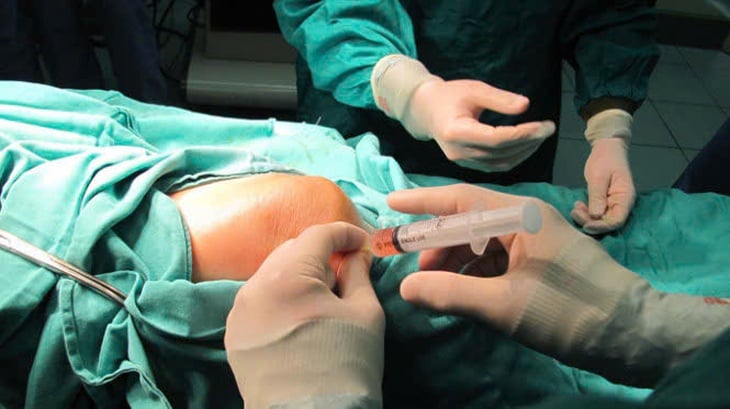
La thérapie cellulaire soulève des défis majeurs en matière de gestion, de science et d'éthique de la recherche. – Photo : Fournie par l’hôpital
Le matin du 6 octobre, à l'Institut Pasteur de Hô Chi Minh-Ville, le Département des sciences, des technologies et de la formation du ministère de la Santé a organisé un atelier sur l'élaboration de normes nationales (TCVN) pour les cellules et les produits de cellules souches utilisés dans la recherche.
Cet événement réunit des dirigeants, des scientifiques et des experts de premier plan issus d'instituts de recherche, d'universités et d'entreprises dans les domaines de la biotechnologie et de la médecine ; afin de discuter et de contribuer à la mise en place d'un cadre juridique, technique et qualitatif pour la recherche et l'application de la thérapie cellulaire au Vietnam.
Les gens dépensent des sommes considérables pour utiliser des « cellules portables » de qualité inconnue.
Lors de l'atelier, M. Nguyen Ngo Quang, directeur du Département des sciences, des technologies et de la formation du ministère de la Santé , a déclaré que la technologie cellulaire et les produits cellulaires dans le domaine médical sont identifiés comme des technologies stratégiques, prioritaires pour le développement dans la période à venir.
Le ministère de la Santé a fait rapport au Secrétariat et ce contenu a été inclus dans la décision du Premier ministre, afin d'encourager la participation des scientifiques, des installations de production et des investisseurs.
Au Vietnam, le domaine des cellules et des produits cellulaires est encore très récent et ne dispose d'aucune filière officielle. De nombreux scientifiques, infrastructures et organismes ont investi massivement, se sont conformés à la réglementation et se sont attachés à garantir la qualité des cellules et des produits cellulaires dans la recherche et les applications.
Cependant, ces derniers temps, le développement du traitement cellulaire est devenu incontrôlé. De nombreux établissements médicaux, cliniques et salons de beauté (officiels et non officiels) ont profité de cette tendance pour appliquer des cellules à leurs clients sans contrôle, entraînant de nombreuses conséquences néfastes pour la santé.
Un problème majeur réside dans l'importation illégale au Vietnam de produits appelés « cellules souches », sans aucun document de contrôle qualité, alors même qu'ils sont largement présentés comme des traitements pour de nombreuses maladies. Les consommateurs sont ainsi contraints de dépenser des sommes considérables pour des produits d'origine et de qualité inconnues.
Cette situation crée une concurrence déloyale envers les établissements médicaux et les scientifiques qui ont investi de manière appropriée dans la technologie, les équipements, les processus de contrôle de la qualité et les normes publiées pour leurs installations.
En 2025, le ministère de la Santé publiera des normes nationales sur les cellules et les produits cellulaires.
M. Quang a ajouté qu'en plus des dispositions de la loi sur l'examen et le traitement médicaux et des circulaires et décrets pris en application de cette loi, la question du contrôle de la qualité des cellules et des produits cellulaires avant leur utilisation sur l'homme est extrêmement importante.
Pour contrôler la qualité des cellules et des produits cellulaires, ils doivent se conformer à 8 ensembles de normes très détaillés, depuis la réception des échantillons, la signature des contrats jusqu'à la réalisation de tests spécialisés et la communication des résultats.
En 2025, le ministère de la Santé publiera des normes nationales (TCVN) relatives aux cellules et aux produits cellulaires, initialement destinées à la recherche et aux applications cliniques. Dans un second temps, ces normes seront mises en œuvre dans la pratique thérapeutique.
« La technologie cellulaire et les produits cellulaires dans le domaine médical constituent la stratégie prioritaire du ministère de la Santé jusqu'en 2035 », a conclu M. Quang.
Un représentant de l'Institut Pasteur à Hô Chi Minh-Ville a déclaré que, pour garantir l'objectivité avant qu'un produit cellulaire ne soit soumis à des essais cliniques, une unité de test indépendante est nécessaire pour évaluer sa qualité selon des critères stricts.
L’Institut recommande au ministère de la Santé de fournir des orientations sur les tests des cellules utilisées dans la recherche, en sélectionnant les critères les plus importants d’identification, d’efficacité et de sécurité pour une application uniforme.

Vice-ministre de la Santé, Nguyen Tri Thuc - Photo : Fournie par l'Institut Pasteur de Hô Chi Minh-Ville
Dans son discours, le vice-ministre de la Santé, Nguyen Tri Thuc, a déclaré qu'il s'agissait d'un événement très spécial, visant à recueillir les rapports et les commentaires des scientifiques, des experts, ainsi que des établissements de production et des praticiens cliniques.
Le vice-ministre a affirmé que le premier ensemble de normes joue un rôle important, servant de base à l'ensemble du processus ultérieur, visant à concrétiser les résolutions du Politburo sur le développement scientifique et technologique et les soins de santé publique, tout en répondant aux exigences de la loi sur les normes et la qualité, qui entrera en vigueur en janvier 2026.
« L’objectif principal de la création du TCVN est d’établir un système de normes nationales au service de la recherche scientifique, en vue d’applications thérapeutiques, avec pour but ultime la protection de la santé publique. »
« Parallèlement, cela contribue à standardiser les processus de recherche et les protocoles de traitement, évitant ainsi les risques regrettables qui pourraient survenir en cas de déploiement à grande échelle sans direction unifiée du ministère de la Santé », a souligné le vice-ministre Nguyen Tri Thuc.
Source : https://tuoitre.vn/nhuc-nhoi-thuc-trang-dung-te-bao-troi-noi-bo-y-te-se-ban-hanh-bo-tieu-chuan-trong-nam-2025-20251006115309451.htm









































































































Comment (0)