Atualmente, a maioria dos ensaios clínicos no Vietnã está focada no desenvolvimento de novos produtos, como medicamentos, vacinas, equipamentos médicos e novas técnicas de tratamento. Em particular, nos últimos anos, houve um aumento nas pesquisas sobre terapia celular e terapia gênica.
Os ensaios clínicos exigem aprovação e avaliação rigorosas antes da implementação, pois o processo de teste, os novos produtos e as técnicas podem representar riscos para os voluntários que participam do estudo.
No entanto, na realidade, ao longo dos anos houve estudos aprovados por ministérios e agências que não o Ministério da Saúde , que realizaram pesquisas com seres humanos, mas não foram aprovados pelo Comitê de Ética em Pesquisa Biomédica.
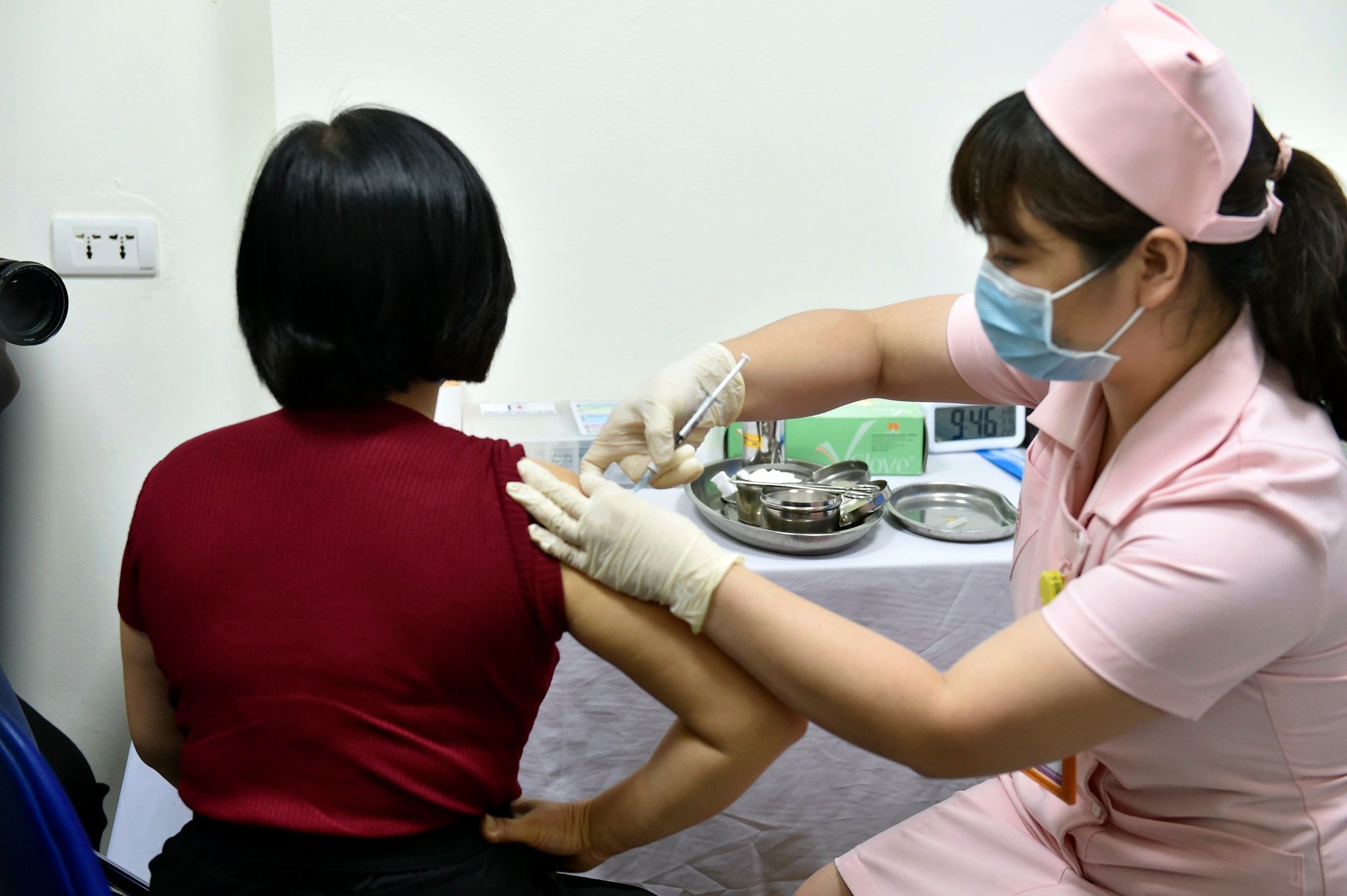
Aplicação das injeções do ensaio clínico da vacina Covivac contra a Covid-19 na Universidade Médica de Hanói , março de 2021.
O Ministério da Saúde está solicitando contribuições sobre uma minuta de circular que regulamenta a gestão de atividades científicas e tecnológicas sob sua responsabilidade. A minuta propõe que projetos de pesquisa financiados por fontes não orçamentárias ou gerenciados por outros ministérios e órgãos, mas que envolvam estudos com seres humanos, só poderão ser conduzidos após aprovação do Conselho de Ética em Pesquisa Biomédica e aprovação formal do Ministério da Saúde. Simultaneamente, a minuta enfatiza o papel dos conselhos locais na aprovação de propostas de pesquisa, na agilização dos prazos de aprovação no Ministério da Saúde e na garantia do progresso das pesquisas.
No Vietnã, são realizados aproximadamente 100 ensaios clínicos anualmente, criando condições favoráveis para o acesso nacional a novas tecnologias, produtos e métodos de tratamento e assistência à saúde, especialmente para doenças complexas como câncer e doenças cardiovasculares. Quando novos produtos e técnicas são aprovados, o Vietnã também estará entre os primeiros a ter acesso a eles, incluindo medicamentos e vacinas. No entanto, antes da aprovação oficial, o processo de ensaio clínico pode acarretar riscos à saúde e à vida dos voluntários; portanto, a aprovação e o monitoramento rigorosos ao longo de todo o processo de implementação são cruciais.
De acordo com a legislação vigente, o Ministério da Saúde é responsável pela gestão, orientação e organização da implementação de pesquisas biomédicas em seres humanos. Antes de iniciar atividades científicas e tecnológicas que envolvam pesquisa biomédica em seres humanos, a organização responsável deve obter aprovação do Comitê de Ética em Pesquisa Biomédica (conforme estipulado na Circular nº 04/2020/TT-BYT).
Link da fonte







![[Foto] Dois voos pousaram e decolaram com sucesso no Aeroporto de Long Thanh.](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F12%2F15%2F1765808718882_ndo_br_img-8897-resize-5807-jpg.webp&w=3840&q=75)


































































































Comentário (0)