V současné době se většina klinických studií ve Vietnamu zaměřuje na vývoj nových produktů, jako jsou léky, vakcíny, zdravotnické vybavení a nové léčebné techniky. Zejména v posledních letech probíhá výzkum buněčné terapie a genové terapie.
Klinické studie vyžadují před provedením přísné schvalování a hodnocení, protože testovací proces, nové produkty a techniky mohou představovat rizika pro dobrovolníky účastnící se studie.
Ve skutečnosti však v průběhu let existovaly studie schválené jinými ministerstvy a agenturami než ministerstvem zdravotnictví , které prováděly výzkum na lidech, ale nebyly schváleny etickou komisí pro biomedicínský výzkum.
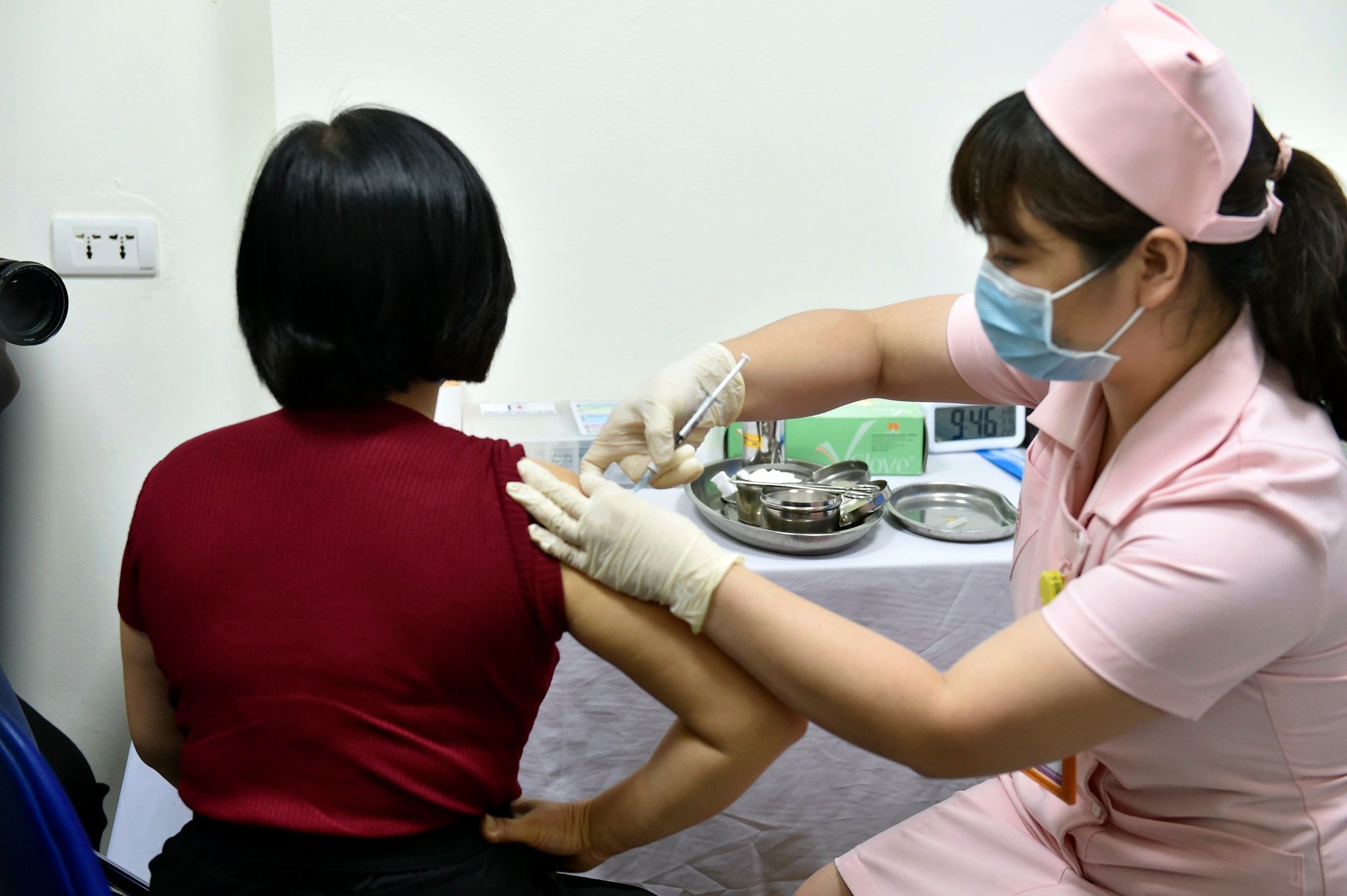
Zkušební injekce vakcíny Covivac proti Covid-19 na Lékařské univerzitě v Hanoji , březen 2021
Ministerstvo zdravotnictví žádá o zpětnou vazbu k návrhu oběžníku upravujícího řízení vědeckých a technologických úkolů v jeho působnosti. Návrh navrhuje, aby výzkumné projekty financované z mimorozpočtových zdrojů nebo řízené jinými ministerstvy a agenturami, ale zahrnující studie na lidech, mohly být realizovány pouze po schválení Radou pro etiku biomedicínského výzkumu a formálním schválení Ministerstvem zdravotnictví. Návrh zároveň zdůrazňuje roli rad na místní úrovni při schvalování výzkumných návrhů, zefektivnění lhůt schvalování na Ministerstvu zdravotnictví a zajištění pokroku ve výzkumu.
Ve Vietnamu se každoročně provádí přibližně 100 klinických studií, což vytváří příznivé podmínky pro domácí přístup k novým technologiím, produktům a metodám v léčbě a zdravotní péči, zejména u náročných onemocnění, jako je rakovina a kardiovaskulární onemocnění. Jakmile budou schváleny nové produkty a techniky, bude Vietnam také mezi prvními, kdo k nim bude mít přístup, včetně léků a vakcín. Před oficiálním schválením však může proces klinických studií nést zdravotní a životní rizika pro dobrovolníky; proto je zásadní důsledné schvalování a monitorování v průběhu celého procesu implementace.
Podle současných předpisů je Ministerstvo zdravotnictví odpovědné za řízení, vedení a organizaci provádění biomedicínského výzkumu na lidech. Před zahájením vědeckých a technologických úkolů zahrnujících biomedicínský výzkum na lidech musí vedoucí organizace získat souhlas Etické komise pro biomedicínský výzkum (jak je stanoveno v oběžníku č. 04/2020/TT-BYT).
Zdrojový odkaz
















































































































Komentář (0)