Eine Gruppe von Wissenschaftlern in Ho-Chi-Minh-Stadt hat eine Stammzellschicht entwickelt, die als „biologisches Pflaster“ zur Wiederherstellung eines infarktbedingten Herzmuskels dienen soll, und diese erfolgreich an Mäusen getestet.
Die Forschung wurde von einer Gruppe von Wissenschaftlern des Ho Chi Minh City Biotechnology Center durchgeführt und im April abgeschlossen. Die Arbeit eröffnet eine neue Forschungsrichtung in der Behandlung von Herzinfarkten mit Stammzellen.
Dr. Pham Le Buu Truc (41 Jahre), Projektleiter, sagte, dass Herz-Kreislauf-Erkrankungen als „stille Killer“ gelten, da die Sterblichkeitsrate derzeit die höchste unter den nicht übertragbaren Ursachen ist, höher als bei Krebs, Diabetes usw. Aktuelle Behandlungsmethoden helfen dabei, die Symptome zu lindern und das Fortschreiten der Herzinsuffizienz zu verlangsamen, können jedoch nicht dazu beitragen, den geschädigten Herzmuskel zu regenerieren oder vollständig wiederherzustellen.
Das Forschungsteam testete die Transplantation von Stammzellschichten in die geschädigte Herzwand, um deren Funktion zu erhalten. Die Stammzellschichten wirken wie ein „biologisches Pflaster“ im geschädigten Bereich, reduzieren die Fibrose, tragen zum Schutz der Herzmuskelwand bei und ermöglichen die Wiederherstellung der Herzmuskelzellen.
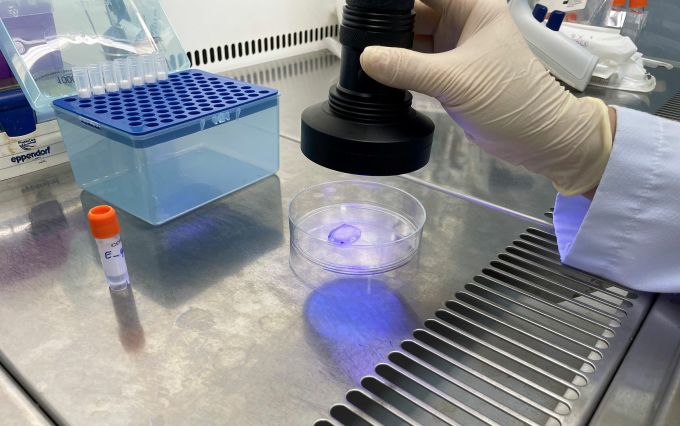
Das biologische Pflaster liegt in Gelform vor und muss UV-Licht ausgesetzt werden, um auszuhärten und sich mit der Herzwand zu verbinden. Foto: Ha An
Zur Herstellung des „biologischen Pflasters“ wählte, isolierte und kultivierte das Team mesenchymale Stammzellen aus menschlichem Nabelschnurgewebe. Diese Art von Säuglingsstammzellen ist jung, gesund, leicht zu gewinnen, sehr verträglich und verursacht kaum eine Immunabstoßung. Gleichzeitig entwickelte das Team ein spezielles Gel und nutzte Lichttechnologie, um eine Verbindung zwischen Stammzellen und Gerüst herzustellen. Dies erleichtert die Formung der Zellschicht beim Einführen in den Körper.
Dieses „biologische Pflaster“ aus Stammzellen funktioniert, wenn es in die Herzwand implantiert wird. Es stellt ischämisches Herzgewebe oder abgestorbene Zellbereiche wieder her und verbessert so die Funktionsfähigkeit des Herzens.
Zur Verifizierung testete die Gruppe weiße Mäuse. Die Mäuse wurden operiert und ihre Koronararterien wurden unterbunden, um ein Modell eines Herzinfarkts zu erstellen, der zu Herzversagen führt. Nach 14 Tagen wählte die Gruppe das Herzinsuffizienz-Mausmodell anhand des per Ultraschall ermittelten linksventrikulären Gesamtblutfraktionsindex (ein Index zur Beurteilung der linksventrikulären Funktion) aus, der auf 20–30 % gesunken war. In einer zweiten Operation transplantierte die Gruppe den „biologischen Patch“, platzierte die Stammzellschicht auf dem infarktbetroffenen Herzbereich und überwachte zwei bis drei Wochen lang die morphologische Entwicklung, das Gewicht und andere biologische Indikatoren, um die Genesungsfähigkeit zu beurteilen.

Dr. Pham Le Buu Truc, Autor der Studie zur Entwicklung eines biologischen Pflasters zur Behandlung von Herzkrankheiten. Foto: Ha An
Durch echokardiographische Überwachung stellte die Gruppe nach der Transplantation eine Verbesserung der linksventrikulären Kontraktionsfunktion im Vergleich zur Kontrollgruppe fest und führte eine Herzoperation an den Mäusen durch. Dr. Truc und seine Kollegen analysierten die histologischen Merkmale des Fibrosegrads in der Herzwand, den Prozess der Verknüpfung des „biologischen Patches“ mit Stammzellgewebe mit dem Herzmuskelgewebe der Maus, die Genexpression...
Infolgedessen reduzierte sich bei der Gruppe der mit der TB2-Zellschicht transplantierten Mäuse der Anteil der Herzfibrose auf 2,4 % – der beste Wert aller getesteten Mäusegruppen. Zudem zeigte die Stammzellschicht keine Immunabstoßung. „Dieses Ergebnis ist eine wichtige Grundlage für die nächsten Schritte der Tests am Menschen“, sagte die Ärztin mit über 15 Jahren Erfahrung in der Stammzellforschung zur Behandlung von Herz-Kreislauf-Erkrankungen.
Bei klinischen Studien am Menschen treten bei der offenen Operation zur Implantation der Stammzellschicht in die Herzwand viele Probleme auf, darunter das Risiko eines zu großen Eingriffs. Daher schlug Dr. Truc vor, ein Gel mit Stammzellen in die Herzbeutelhöhle zu injizieren. Anschließend wird ein kompaktes Leuchtgerät (das die Verfestigung und Verdichtung des Gels unterstützt) in den geschädigten Bereich des Herzmuskels eingeführt, um vor Ort einen „biologischen Patch“ aus Stammzellen zu erzeugen, der das geschädigte Herzgewebe bedeckt. Dies gilt als minimalinvasive Methode, die das Komplikationsrisiko reduziert und den Patienten viele Behandlungsvorteile bringen kann.
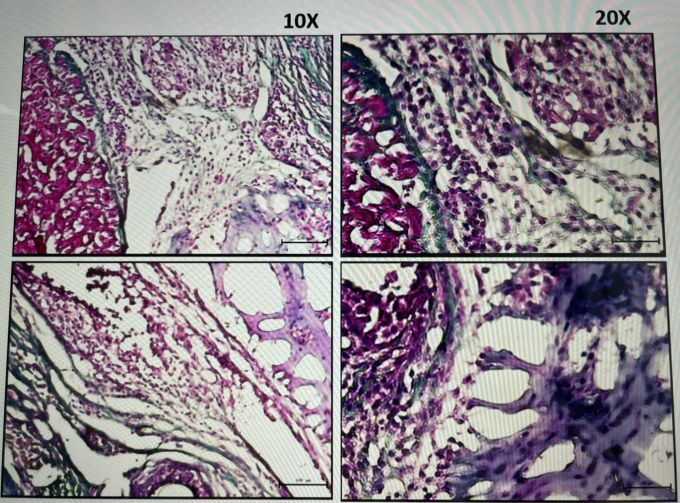
Vergrößerte Abbildung der Verbindung zwischen Stammzellschicht und Herzmuskel in der TB2-Probe. Foto: NVCC
Dr. Bui Quoc Thang (Abteilung für Reanimation – Kinderherzchirurgie, Cho Ray Krankenhaus) bewertete die Studienergebnisse als hilfreich für neue Ansätze zur Behandlung von Herz-Kreislauf-Erkrankungen, insbesondere Herzinfarkten. Das Transplantat trägt zur Reduzierung des Fibroseprozesses bei und verbessert dadurch die Kontraktionsfunktion der linken Herzkammer. Dies zeigt, wie wirksam es die Herzmuskelzellen bei ischämischen Erkrankungen schützt. Dies kann in Kombination mit gängigen Behandlungsmethoden wie Medikamenten, Stentimplantation oder Koronararterien-Bypass-Operationen angewendet werden, um die Wirksamkeit der aktuellen Methoden zu erhöhen.
Dr. Thang erklärte jedoch, dass für die Anwendung am Menschen weitere präklinische Studien erforderlich seien, um den Mechanismus der Fibrosereduktion und des Schutzes der Myokardzellen im ischämischen Zustand der Zellschicht zu klären. Dies würde den Ärzten helfen, die wissenschaftliche Grundlage für die nächsten Schritte der klinischen Studien zu stärken. Darüber hinaus erfordert die Durchführung der Forschung am Menschen die Genehmigung des Gesundheitsministeriums und einen enormen Ressourceneinsatz. Der Grund dafür ist, dass klinische Studien sehr teuer sind und ein Team von klinischen Experten benötigt wird, um die Durchführung von Forschung zu verstehen. „Wenn die Forschung am Menschen erfolgreich ist, wird der Nutzen für die Wissenschaft, die Patienten und sogar der wirtschaftliche Nutzen die Investition rechtfertigen“, sagte Herr Thang.
Ha An
[Anzeige_2]
Quellenlink

























![[Foto] Vorsitzender der Nationalversammlung nimmt am Seminar „Aufbau und Betrieb eines internationalen Finanzzentrums und Empfehlungen für Vietnam“ teil](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/7/28/76393436936e457db31ec84433289f72)













































































Kommentar (0)