Власти Пакистана объявили о временной приостановке поставок препарата для лечения рака (Авастин), распространяемого швейцарской фармацевтической компанией Roche, для проведения исследований после того, как 12 пациентов ослепли после инъекции этого препарата.
В связи с этой информацией Управление по контролю за лекарственными средствами Вьетнама ( Министерство здравоохранения ) только что 27 сентября объявило, что представительство компании F. Hoffmann La Roche Ltd. опубликовало официальное сообщение, содержащее обновленную информацию о расследовании, связанном с вышеуказанным препаратом Авастин .
Во Вьетнаме Авастин имеет 4 действующих свидетельства о регистрации обращения, а именно:
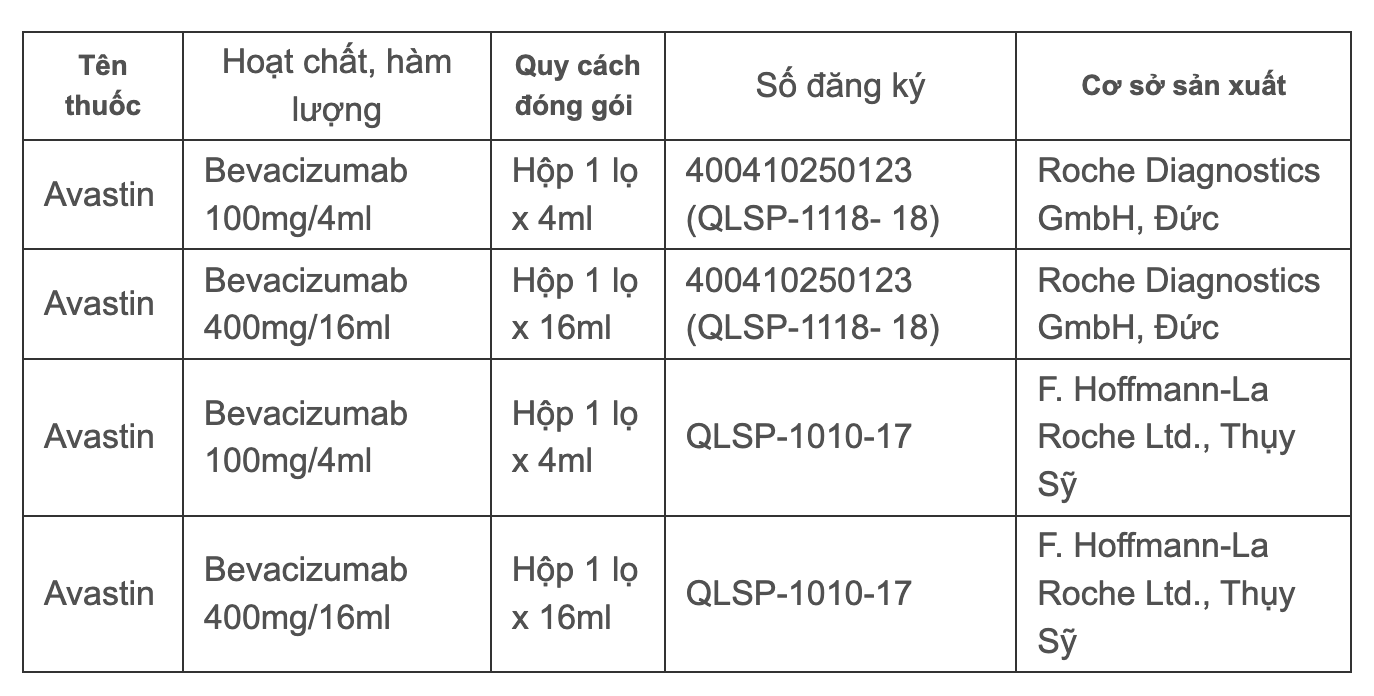
4 действительных регистрационных удостоверения на Авастин
По данным Управления по контролю за лекарственными средствами Вьетнама, препарату Авастин выдано свидетельство о регистрации в обращении во Вьетнаме по следующим показаниям для лечения: метастатический колоректальный рак, распространенный, метастатический или рецидивирующий немелкоклеточный рак легких, распространенный и/или метастатический почечно-клеточный рак, глиобластома/злокачественная глиома (стадия IV), эпителиальный рак яичников, маточных труб и первичный рак брюшины.
В дополнение к общим предупреждениям, одобренная FDA инструкция по применению также предупреждает, что «препарат не следует использовать для интравитреальных инъекций». В частности: препарат может вызывать нарушения зрения. Были зарегистрированы отдельные случаи и группы серьезных нежелательных явлений со стороны глаз после интравитреальных инъекций (неодобренный способ введения) смесей Авастина из флаконов, предназначенных для внутривенного вливания онкологическим больным.
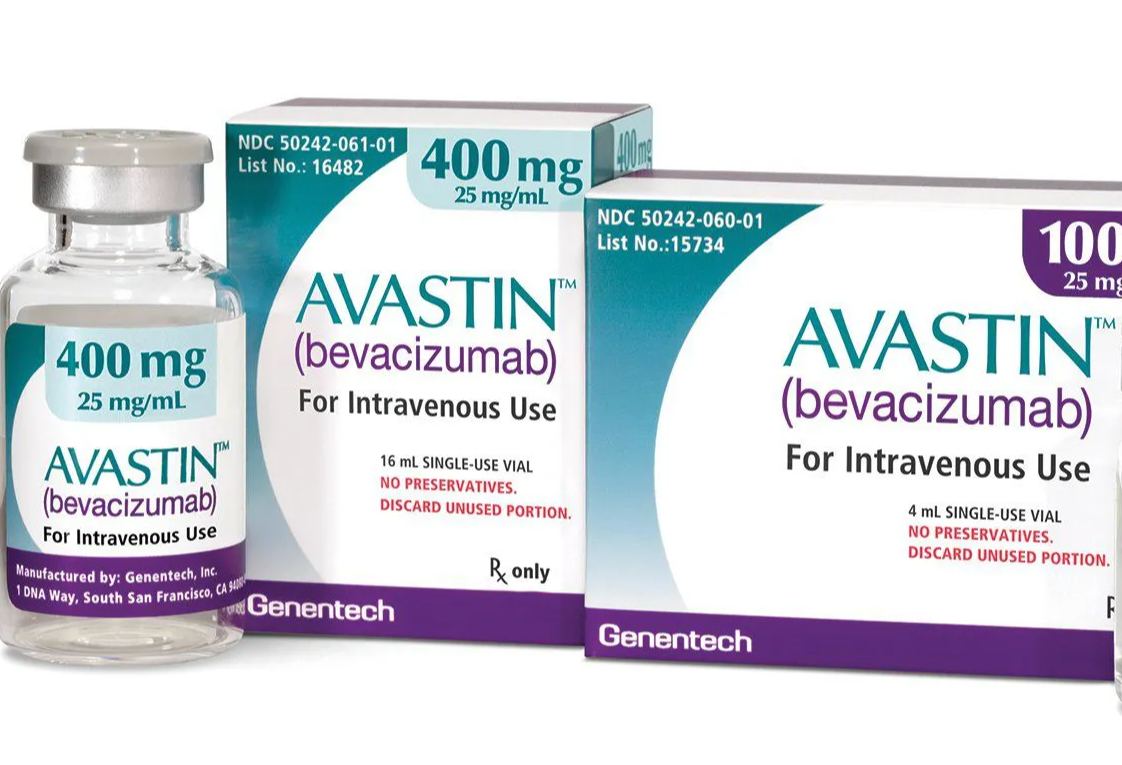
Авастин применяется при лечении рака.
К таким реакциям относятся: внутриглазная инфекция, эндофтальмит, такой как стерильный эндофтальмит, увеит и витрит, ретинальная полосатость, разрыв пигментного эпителия сетчатки, повышенное внутриглазное давление, внутриглазное кровоизлияние, такое как кровоизлияние в стекловидное тело или кровоизлияние в сетчатку, и конъюнктивальное кровоизлияние. Некоторые из этих событий привели к различной степени потери зрения, включая постоянную слепоту.
Представитель Управления по контролю за лекарственными средствами Вьетнама сообщил, что по состоянию на 27 сентября агентство не получало никаких сообщений, отражающих нежелательные эффекты Авастина, связанные с потерей зрения у пациентов после приема Авастина.
Согласно отчету представительства компании F. Hoffmann La Roche Ltd. в официальном сообщении № RA/02/09/2023, содержащем обновленную информацию о расследовании, связанном с препаратом Авастин, направленном в Управление по контролю за лекарственными средствами Пакистана, около 12 пациентов потеряли зрение после использования инъекций, предоставленных нелегальным поставщиком Genius Pharmaceutical Service. Согласно этому отчету, препарат маркируется как «Инъекции Авастина 1,25 мг/0,05 мл», что создает ложное впечатление, что это продукт компании Roche.
Препарат Авастин компании Roche не одобрен для применения при каких-либо офтальмологических показаниях. Компания Genius Pharmaceutical Service осуществила поставку/разбавление/переупаковку препарата в дозировке 1,25 мг/0,5 мл в антисанитарных и несанкционированных условиях.
Источник




![[Фото] Делегация из 100 журналистов из Ассоциации журналистов Вьетнама посещает солдат и жителей острова Труонгша.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/30/0984a986227d4e988177f560d2e1563e)
![[Фото] Журналисты были тронуты до слез на панихиде по солдатам, погибшим в Гак Ма](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/30/9454613a55c54c16bf8c0efa51883456)





















![[Фото] Премьер-министр Фам Минь Чинь посещает мероприятие «Цифровая трансформация банковской отрасли к 2025 году»](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/29/0e34cc7261d74e26b7f87cadff763eae)
































































Комментарий (0)