أعلنت السلطات في باكستان تعليقا مؤقتا لدواء علاج السرطان (أفاستين) الذي توزعه شركة الأدوية السويسرية روش للتحقيق بعد إصابة 12 مريضا بالعمى بعد حقنهم بالدواء.
وفيما يتعلق بهذه المعلومات، أعلنت إدارة الأدوية في فيتنام ( وزارة الصحة ) للتو في 27 سبتمبر أن المكتب التمثيلي لشركة F. Hoffmann La Roche Ltd. أصدر إرسالًا رسميًا يتضمن معلومات محدثة عن التحقيق المتعلق بالدواء المذكور أعلاه Avastin .
في فيتنام، يمتلك Avastin 4 شهادات تسجيل تداول صالحة، وهي على وجه التحديد:
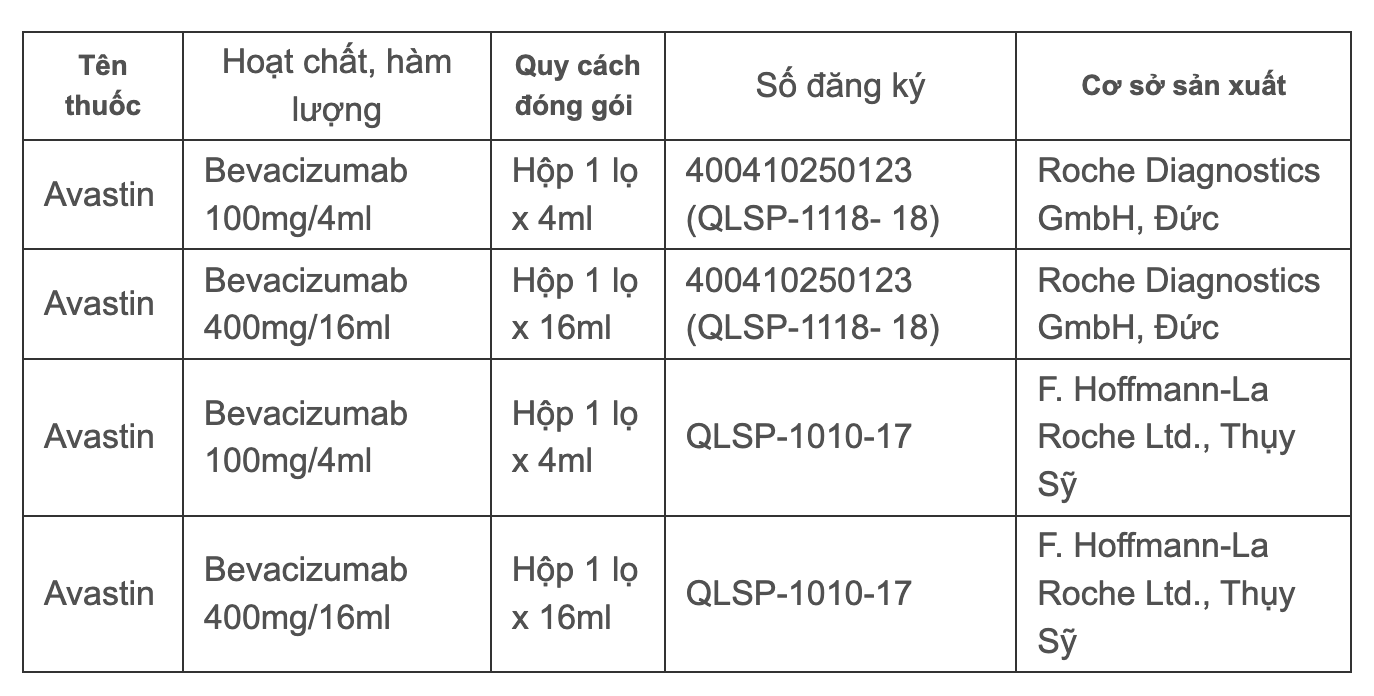
4 شهادات تسجيل صالحة لـ Avastin
وفقًا لإدارة الأدوية في فيتنام، تم منح أفاستين شهادة تسجيل تداول في فيتنام مع مؤشرات العلاج التالية: سرطان القولون والمستقيم النقيلي، سرطان الرئة غير صغير الخلايا المتقدم أو النقيلي أو المتكرر، سرطان الخلايا الكلوية المتقدم و/أو النقيلي، الورم الأرومي الدبقي/الورم الدبقي الخبيث (المرحلة الرابعة)، سرطان المبيض الظهاري، وسرطان قناة فالوب وسرطان الصفاق الأولي.
بالإضافة إلى التحذيرات العامة، تُحذّر النشرة الداخلية المُعتمدة من قِبل إدارة الغذاء والدواء الأمريكية (FDA) من أنه "لا يُستخدَم للحقن داخل الجسم الزجاجي". تحديدًا: قد يُسبّب الدواء اضطرابات بصرية. سُجِّلت حالات فردية ومجموعات من الآثار الجانبية الخطيرة في العين بعد الحقن داخل الجسم الزجاجي، وهو طريق غير مُعتمد للإعطاء، باستخدام خلائط أفاستين من قوارير مُخصَّصة للتسريب الوريدي لمرضى السرطان.
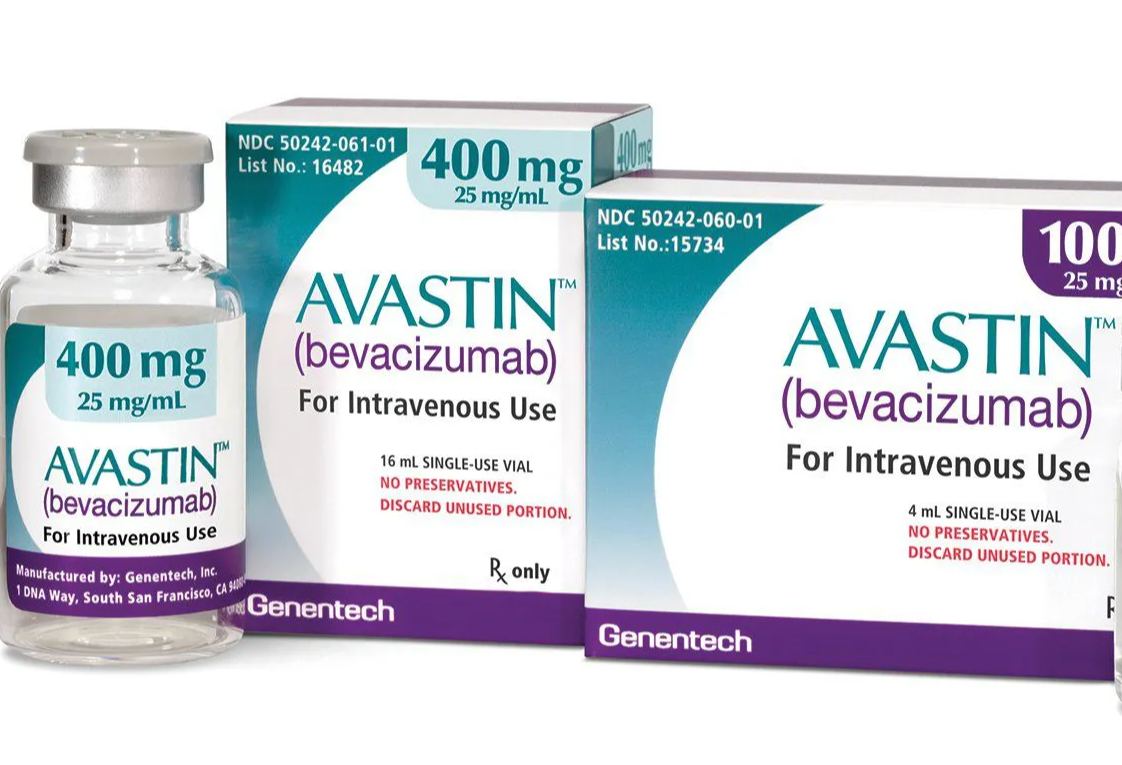
يستخدم دواء افاستين في علاج السرطان.
تشمل هذه التفاعلات: العدوى داخل العين، التهاب باطن العين، مثل التهاب باطن العين المعقم، التهاب العنبية والتهاب الزجاجية، تليف الشبكية، تمزق الظهارة الصبغية الشبكية، زيادة الضغط داخل العين، نزيف داخل العين مثل نزيف الجسم الزجاجي أو نزيف الشبكية، ونزيف الملتحمة. وقد أدت العديد من هذه الأحداث إلى درجات متفاوتة من فقدان البصر، بما في ذلك العمى الدائم.
وقال ممثل إدارة الغذاء والدواء في فيتنام إنه حتى 27 سبتمبر/أيلول، لم تتلق الوكالة أي تقارير تعكس آثارًا غير مرغوب فيها لدواء أفاستين تتعلق بفقدان المرضى للبصر بعد استخدام أفاستين.
وفقًا لتقرير المكتب التمثيلي لشركة F. Hoffmann La Roche Ltd. في الإرسالية الرسمية رقم RA/02/09/2023 التي تتضمن معلومات محدثة عن التحقيق المتعلق بدواء أفاستين، والمعلومات المرسلة إلى إدارة الأدوية الباكستانية، فقد حوالي 12 مريضًا بصرهم بعد استخدام الحقن المقدمة من قبل المورد غير القانوني Genius Pharmaceutical Service. وفقًا لهذا التقرير، تم تسمية الدواء "Inj. Avastin 1.25 mg/0.05 ml" مما أدى إلى إعطاء تصور مضلل بأنه منتج من شركة Roche.
لم تتم الموافقة على استخدام دواء أفاستين من إنتاج شركة روش في أي من مؤشرات طب العيون. قامت شركة Genius Pharmaceutical Service بتوريد/تخفيف/إعادة تعبئة الدواء بجرعة 1.25 ملجم/0.5 مل في ظل ظروف غير صحية وغير معتمدة.
[إعلان 2]
مصدر


![[صورة] أفضل اللاعبين يتجمعون في بطولة تنس الطاولة الوطنية لصحيفة نهان دان 2025](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/23/9ad5f6f4faf146b08335e5c446edb107)

![[صورة] نجح الثنائي آن هوانغ ودين دوك في الدفاع عن لقب بطولة زوجي الرجال في بطولة تنس الطاولة الوطنية لصحيفة نهان دان](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/23/d6ab3bcac02c49928b38c729d795cac6)























































































تعليق (0)