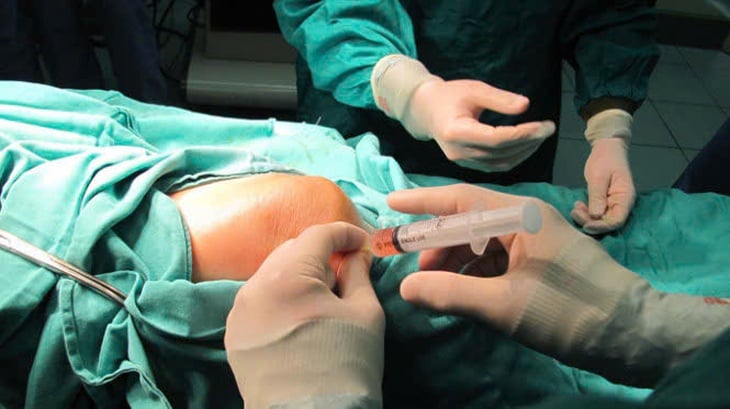
يشكل العلاج بالخلايا تحديات كبيرة في الإدارة والعلم وأخلاقيات البحث - الصورة: مقدمة من المستشفى
في صباح يوم 6 أكتوبر، نظمت إدارة العلوم والتكنولوجيا والتدريب بوزارة الصحة في معهد باستور في مدينة هوشي منه ورشة عمل حول تطوير المعايير الوطنية (TCVN) للخلايا ومنتجات الخلايا الجذعية المستخدمة في البحث.
يجمع الحدث بين كبار المديرين والعلماء والخبراء من معاهد البحوث والجامعات والشركات في مجالات التكنولوجيا الحيوية والطب؛ لمناقشة والمساهمة بالأفكار لبناء ممر قانوني وتقني وعالي الجودة للبحث وتطبيق العلاج الخلوي في فيتنام.
ينفق الناس مبالغ كبيرة من المال لاستخدام "خلايا محمولة يدويًا" ذات جودة غير معروفة.
وفي الورشة، قال السيد نجوين نجو كوانج - مدير إدارة العلوم والتكنولوجيا والتدريب بوزارة الصحة - إن تكنولوجيا الخلايا ومنتجات الخلايا في المجال الطبي تم تحديدها كتقنيات استراتيجية ذات أولوية للتطوير في الفترة المقبلة.
وقد أبلغت وزارة الصحة الأمانة العامة وتم تضمين هذا المحتوى في قرار رئيس الوزراء، لتشجيع مشاركة العلماء ومرافق الإنتاج والمستثمرين.
في فيتنام، لا يزال مجال الخلايا ومنتجاتها جديدًا، ولم يُنشأ تخصص رسمي بعد. وقد استثمر العديد من العلماء والمراكز والوحدات بجدية، والتزموا باللوائح، وركزوا على ضمان جودة الخلايا ومنتجاتها في البحث والتطبيق.
مع ذلك، في الآونة الأخيرة، افتقر تطور مجال الخلايا إلى الرقابة. فقد استغلت العديد من المرافق الطبية والعيادات وصالونات التجميل (الرسمية وغير الرسمية) هذا التوجه لتطبيق الخلايا على الزبائن دون رقابة، مما تسبب في عواقب صحية عديدة.
من القضايا الملحة أن منتجات تُسمى "الخلايا الجذعية" تُستورد إلى فيتنام يدويًا، دون وثائق مراقبة الجودة، ومع ذلك يُروّج لها على نطاق واسع لعلاج العديد من الأمراض. يضطر الناس إلى إنفاق مبالغ طائلة على منتجات مجهولة المصدر والجودة.
ويؤدي هذا الوضع إلى خلق منافسة غير عادلة مع المرافق الطبية والعلماء الذين استثمروا بشكل سليم في التكنولوجيا والمعدات وعمليات مراقبة الجودة والمعايير المنشورة للمرافق.
في عام 2025، ستصدر وزارة الصحة المعايير الوطنية الخاصة بالخلايا ومنتجات الخلايا.
وأضاف السيد كوانغ أنه بالإضافة إلى اللوائح الواردة في قانون الفحص الطبي والعلاج والتعميمات والمراسيم بموجب القانون، فإن قضية مراقبة جودة الخلايا ومنتجات الخلايا قبل استخدامها على البشر مهمة للغاية.
ولضمان التحكم في جودة الخلايا ومنتجات الخلايا، يتعين عليهم المرور عبر 8 مجموعات مفصلة للغاية من المعايير، بدءاً من تلقي العينات، وتوقيع العقود، إلى إجراء الاختبارات المتخصصة وإرجاع النتائج.
في عام ٢٠٢٥، ستُصدر وزارة الصحة معايير وطنية (TCVN) للخلايا ومنتجاتها، تُطبّق مبدئيًا في الأبحاث والتطبيقات السريرية. وفي المرحلة التالية، سيتم تطبيق هذه المعايير في ممارسات العلاج.
واختتم السيد كوانج قائلاً: "إن تكنولوجيا الخلايا ومنتجات الخلايا في المجال الطبي تشكل الاستراتيجية ذات الأولوية لوزارة الصحة من الآن وحتى عام 2035".
وقال ممثل معهد باستور في مدينة هوشي منه إنه لضمان الموضوعية قبل وضع منتج خلوي في التجارب السريرية، هناك حاجة إلى وحدة اختبار مستقلة لتقييم الجودة وفقًا لمعايير صارمة.
ويوصي المعهد وزارة الصحة بتقديم إرشادات بشأن اختبار الخلايا المستخدمة في الأبحاث، واختيار المعايير الأكثر أهمية للتعريف والفعالية والسلامة للتطبيق الموحد.

نائب وزير الصحة نجوين تري ثوك - الصورة: مقدمة من معهد باستور في مدينة هوشي منه
وفي كلمته، قال نائب وزير الصحة نجوين تري ثوك إن هذا حدث خاص للغاية، ويهدف إلى الاستماع إلى التقارير والتعليقات من العلماء والخبراء، وكذلك من مرافق الإنتاج والممارسات السريرية.
وأكد نائب الوزير أن المجموعة الأولى من المعايير تلعب دورًا مهمًا، حيث تشكل الأساس للعملية التالية بأكملها، بهدف تجسيد قرارات المكتب السياسي بشأن تطوير العلوم والتكنولوجيا ورعاية صحة الشعب، مع تلبية متطلبات قانون المعايير والجودة، والذي سيدخل حيز التنفيذ اعتبارًا من يناير 2026.
"الهدف الأساسي من بناء TCVN هو إنشاء نظام معايير وطني لخدمة البحث العلمي، والتحرك نحو التطبيق في العلاج بهدف حماية صحة الناس في نهاية المطاف.
وفي الوقت نفسه، يساعد ذلك على توحيد عمليات البحث وأنظمة العلاج، وتجنب المخاطر المؤلمة التي قد تحدث عند نشرها على نطاق واسع دون توجيه موحد من وزارة الصحة"، كما أكد نائب الوزير نجوين تري ثوك.
المصدر: https://tuoitre.vn/nhuc-nhoi-thuc-trang-dung-te-bao-troi-noi-bo-y-te-se-ban-hanh-bo-tieu-chuan-trong-nam-2025-20251006115309451.htm





































































































تعليق (0)