
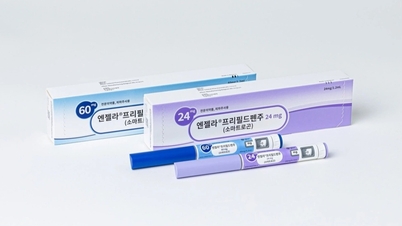
Retirada a nivel nacional de la solución de higiene femenina Ori Women Pluss
En concreto, según el despacho oficial del Departamento de Salud de Nghe An, los resultados de las pruebas mostraron que el lote de solución de higiene femenina Ori Women Pluss (caja de 1 botella de 120 ml, número de lote: 160324, fecha de fabricación: 16 de marzo de 2024, fecha de caducidad: 16 de marzo de 2027) producido por SJK Pharmaceutical and Cosmetic Biotechnology Company Limited (Hanoi), Bao Minh Chau Herbal Medicine and Medical Equipment Joint Stock Company (Hai Phong) es responsable de llevarlo al mercado, no cumplió con los estándares para los indicadores de límite microbiano.
La muestra de prueba se tomó en el mostrador de la sucursal farmacéutica de Que Phong ( Nghe An ). La Administración de Medicamentos solicitó la suspensión de la circulación, el retiro y la destrucción de todo el lote de este producto.
Los departamentos de salud provinciales y municipales son responsables de notificar a las empresas y usuarios para que dejen de consumir el producto inmediatamente, monitorear los retiros del mercado y manejar las infracciones.
Las dos empresas implicadas deben organizar urgentemente el retiro y la destrucción e informar los resultados al departamento antes del 4 de octubre.
Además, el Centro de Pruebas de Medicamentos, Cosméticos y Alimentos (Departamento de Salud de Can Tho ) también informó que el lote de producto LD Perfume Oil (caja de 1 botella de 12 ml, número de lote: LD043979, fecha de vencimiento: 36 meses después de la apertura) introducido en el mercado por LD Group Trading and Production Company Limited (Can Tho) no cumplió con los estándares de calidad en términos de indicadores sensoriales y violó las regulaciones de etiquetado (falta de información sobre la fecha de producción y el número de lote).
El Departamento de Administración de Medicamentos solicitó la suspensión de la circulación y el retiro a nivel nacional de este lote de producto. LD Group Company debe retirar, destruir y revisar las etiquetas de otros lotes para corregir errores similares e informar al departamento antes del 19 de septiembre.
La Administración de Medicamentos de Vietnam solicita a los departamentos de salud locales que supervisen de cerca la retirada y destrucción de establecimientos comerciales, y que, al mismo tiempo, verifiquen el cumplimiento de las normas sobre la gestión de cosméticos en la producción y las actividades comerciales. En caso de detectar infracciones, estas deben gestionarse estrictamente de acuerdo con la normativa vigente.
Se recomienda a los consumidores verificar cuidadosamente la información del producto, dejar de usar inmediatamente los lotes de cosméticos que han sido suspendidos de circulación e informar rápidamente a las autoridades cuando descubran productos sospechosos de ser inseguros.
La empresa retiró voluntariamente del mercado 4 productos CELL29
Además, el Departamento de Administración de Medicamentos también anunció la retirada de 4 números de recibo de declaración de productos cosméticos solicitados por NEXTGEN INTERNATIONAL JSC (HCMC) para detener la actividad comercial, incluidos:
1. BÁLSAMO REPASIVO PARA IMPERFECCIONES CELL29
2. CREMA DE POTENCIA CELL29 LUONLIGHT
3. REFUERZO CELL29 ILLUNA-EX
4. TÓNICO CELL29 GEN-3
Los cuatro productos mencionados anteriormente son fabricados por HWCOSCOCO CO., LTD (Corea) y cuentan con licencia para su circulación por parte de la Administración de Medicamentos de Vietnam desde febrero de 2025.
Fuente: https://tuoitre.vn/lai-phat-hien-lo-dung-dich-ve-sinh-phu-nu-vi-pham-quy-dinh-ve-chat-luong-2025091014542769.htm
































![[Foto] El periódico Nhan Dan muestra y solicita comentarios sobre los borradores de documentos del XIV Congreso Nacional del Partido.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/10/26/1761470328996_ndo_br_bao-long-171-8916-jpg.webp)








































































Kommentar (0)