Produkt jest dystrybuowany przez GAMMA Pharmaceutical - Cosmetic Production Company Limited, po odkryciu, że w jego składnikach znajdują się niezadeklarowane substancje.
Według informacji przekazanych przez władze, wycofana partia produktu ma numer GMPA010524, została wyprodukowana 2 maja 2024 r., a data ważności upływa 2 maja 2027 r., a numer potwierdzenia wydania to 000669/21/CBMP-HCM.
 |
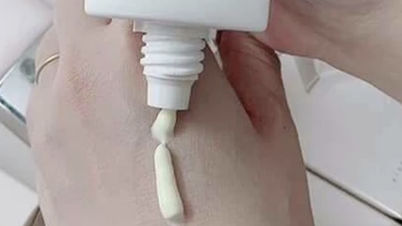
| Zdjęcie ilustracyjne. |
Produkt należy do GAMMA Pharmaceutical - Cosmetic Production Company Limited (dawniej GAMMA Private Enterprise for Cosmetic Chemical Production) z siedzibą pod adresem 18 Nguyen Hau Street, Tan Thanh Ward, Tan Phu District, Ho Chi Minh City i adresem produkcyjnym w Group 1, Phu Hiep Hamlet, Phu Hoa Dong Commune, Cu Chi District, Ho Chi Minh City.
Wyniki badań próbek produktu, przeprowadzonych przez Centrum Testowania Leków, Kosmetyków i Żywności Departamentu Zdrowia Prowincji Yen Bai zgodnie z certyfikatem badań nr 25L-020MP z dnia 17 czerwca, wykazały, że produkt zawiera dwa powszechnie stosowane konserwanty w kosmetykach: metyloparaben i propyloparaben.
Jednakże te dwie substancje nie zostały uwzględnione w składzie produktu przedstawionym władzom, co stanowi poważne naruszenie przepisów dotyczących deklarowania składników kosmetycznych.
W odpowiedzi na powyższe naruszenia, Agencja ds. Żywności i Leków (FDA) zażądała wstrzymania obrotu i pilnego wycofania partii produktu w całym kraju. Jednocześnie zaapelowała do firm i użytkowników kosmetyków o natychmiastowe zaprzestanie sprzedaży i stosowania tej partii płynu do mycia twarzy oraz o zwrot produktu dostawcy.
Departament zwrócił się również do departamentów zdrowia prowincji i miast centralnie zarządzanych o powiadomienie przedsiębiorców i użytkowników kosmetyków na swoim terenie o decyzji o zawieszeniu, a także o jednoczesne przeprowadzenie kontroli i nadzorowanie procesu wycofywania i niszczenia produktów oraz o ścisłe postępowanie z podmiotami naruszającymi przepisy, zgodnie z obowiązującymi przepisami.
W przypadku firmy GAMMA Company, Agencja ds. Żywności i Leków wymaga od niej wysłania zawiadomienia o wycofaniu produktu do wszystkich jednostek dystrybuujących i wykorzystujących produkt, odebrania towarów z placówek handlowych oraz wycofania i zniszczenia całej partii produktów naruszających przepisy.
Wyniki wycofania i zniszczenia produktu muszą zostać zgłoszone do Departamentu przed 2 sierpnia 2025 r. Jednocześnie Departament unieważnia również numer odbioru deklaracji produktu kosmetycznego 000669/21/CBMP-HCM zgodnie z postanowieniami punktu b, artykułu 46, Okólnika nr 06/2011/TT-BYT.
Wietnamska Agencja ds. Żywności i Leków zleciła Departamentowi Zdrowia miasta Ho Chi Minh przeprowadzanie inspekcji i nadzorowanie przestrzegania zasad wycofywania z obrotu i niszczenia produktów firmy GAMMA naruszających przepisy, a jednocześnie analizowanie i rozpatrywanie naruszeń w zakresie produkcji i handlu kosmetykami tej jednostki zgodnie z prawem.
Wcześniej Agencja ds. Żywności i Leków podjęła również decyzję o zawieszeniu i wycofaniu wielu innych produktów kosmetycznych z powodu naruszeń przepisów dotyczących składników i etykietowania.
Dokładnie 7 wycofanych produktów, w tym: ME LINE 01 Caucasian Skin, INNOAESTHTICS INNO-TDS Xeroskin-ID, INNOAESTHTICS INNO-DERMA Dark Spot Eraser 24H Cream, INNOAESTHTICS INNO-EXFO Redness Peel, INNOAESTHTICS INNO-EXFO TCAGE, INNOAESTHTICS INNO-EXFO Skin Recovery i ME LINE 02 Caucasian Skin Night.
Produkty te zostały ogłoszone i dystrybuowane przez Dong Nam Global Pharmaceutical Company Limited. Departament zażądał od firmy wycofania wszystkich produktów wprowadzonych na rynek i czasowego zawieszenia przeglądu dokumentacji dotyczącej nowego produktu kosmetycznego tej firmy na okres 6 miesięcy. Dokumentacja złożona przed decyzją o zawieszeniu również straciła ważność.
Ponadto, dwa inne produkty, Aquafresh Soft Mint i Aquafresh Clear Mint, wydawane przez Phat Anh Minh Company Limited, również zostały zawieszone z powodu naruszenia przepisów dotyczących etykietowania kosmetyków. Agencja ds. Żywności i Leków (FDA) zwróciła się do Departamentu Zdrowia o ścisłe monitorowanie procesu wycofywania tych produktów, rygorystyczne postępowanie w przypadku naruszeń i przesyłanie raportów do Departamentu w celu ich syntezy i monitorowania.
Ten drastyczny krok ma na celu wzmocnienie kontroli jakości kosmetyków na rynku i zapewnienie bezpieczeństwa konsumentom. Agencja ds. Żywności i Leków (DMA) zaleca, aby organizacje i osoby prywatne zaprzestały używania, dystrybucji i handlu produktami objętymi zawieszeniem.
Konsumenci muszą aktywnie współpracować z władzami w zakresie wycofywania i niszczenia kosmetyków niezgodnych ze standardami, przyczyniając się w ten sposób do ochrony zdrowia publicznego i środowiska.
Źródło: https://baodautu.vn/sua-rua-mat-gammaphil-125ml-bi-thu-hoi-do-khong-dung-thanh-phan-theo-cong-bo-d329284.html
































































































![Przejście Dong Nai OCOP: [Artykuł 3] Powiązanie turystyki z konsumpcją produktów OCOP](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/11/10/1762739199309_1324-2740-7_n-162543_981.jpeg)













Komentarz (0)