हाल के वर्षों में, कैंसर के बारे में हमारी समझ में एक बड़ा बदलाव यह अहसास लेकर आया है कि सूक्ष्मजीव न केवल आंत में, बल्कि ट्यूमर के ऊतकों में भी पाए जाते हैं—जिनमें स्तन, प्रोस्टेट और फेफड़े जैसे ठोस ट्यूमर भी शामिल हैं। ये सूक्ष्मजीव समुदाय (जिन्हें सामूहिक रूप से इंट्राट्यूमरल माइक्रोबायोम या ट्यूमर-संबंधी माइक्रोबायोम कहा जाता है) कैंसर कोशिकाओं, प्रतिरक्षा कोशिकाओं और आसपास के वातावरण के साथ सीधे संपर्क करते हैं, जिससे ट्यूमर का जीव विज्ञान, उपचार प्रतिक्रिया और रोग का निदान प्रभावित होता है।
क्या ट्यूमर ऊतक में माइक्रोबायोटा आंत के माइक्रोबायोटा से भिन्न है?
पहले ट्यूमर ऊतक को एक "बाँझ क्षेत्र" माना जाता था, लेकिन हाल ही में हुए जीनोमिक और अनुक्रमण विश्लेषण से कई रिसेक्ट किए गए ट्यूमर नमूनों में सूक्ष्मजीवी डीएनए/आरएनए का पता चला है। ये सूक्ष्मजीव कैंसर कोशिकाओं, प्रतिरक्षा कोशिकाओं या आसपास के संयोजी ऊतक में मौजूद हो सकते हैं। सूक्ष्मजीवों की संरचना और घनत्व ट्यूमर के प्रकार और रोगियों के अनुसार अलग-अलग होते हैं—उदाहरण के लिए, स्तन ट्यूमर में कुछ अन्य ट्यूमर की तुलना में अपेक्षाकृत अधिक सूक्ष्मजीवी विविधता होती है—और उनका स्थान (कोशिकीय बनाम बाह्यकोशिकीय) यह निर्धारित करता है कि वे रोगग्रस्त ऊतक को कैसे प्रभावित करते हैं।
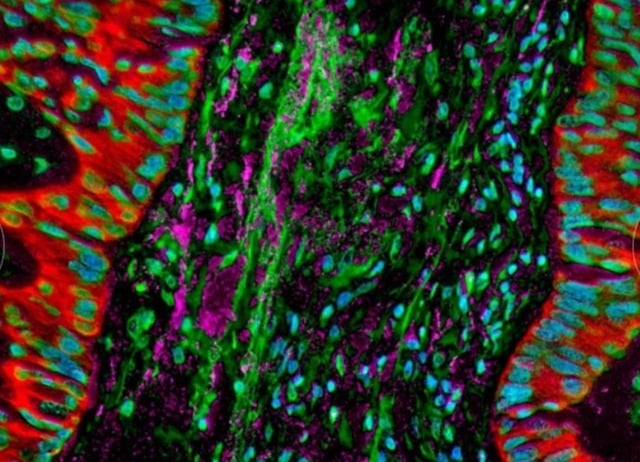
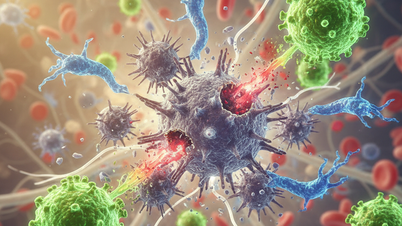
सूक्ष्म चित्रों से पता चलता है कि फेफड़े के कैंसर कोशिकाओं में बैक्टीरिया रहते हैं, जो शरीर की प्रतिरक्षा प्रतिक्रिया को बदल देते हैं।
स्तन, प्रोस्टेट और फेफड़ों के ऊतकों में बैक्टीरिया और वायरस की भूमिका
स्थानीय माइक्रोबायोटा प्रतिरक्षा वातावरण को दमनकारी या सक्रियकारी दोनों तरह से नियंत्रित कर सकते हैं। कुछ सूक्ष्मजीव दीर्घकालिक सूजन संबंधी संकेतों (जैसे, पैटर्न पहचान रिसेप्टर्स जैसे टीएलआर) को सक्रिय करते हैं, जिससे प्रो-इंफ्लेमेटरी साइटोकिन्स में वृद्धि होती है, जो दमनकारी प्रतिरक्षा कोशिकाओं (एम2 मैक्रोफेज, टीरेग) को आकर्षित करते हैं - जिससे ट्यूमर को प्रतिरक्षा से बचने में मदद मिलती है। इसके विपरीत, कुछ बैक्टीरिया या वायरस कोशिकीय प्रतिरक्षा को उत्तेजित कर सकते हैं (एंटीजन प्रस्तुति में वृद्धि, सीडी8+ टी कोशिका सक्रियण) और इम्यूनोथेरेपी की प्रभावशीलता में योगदान दे सकते हैं। इस प्रकार, एक ही माइक्रोबायोटा संदर्भ के आधार पर "मित्र" या "शत्रु" हो सकता है।
कुछ बैक्टीरिया ऐसे विषाक्त पदार्थ या यौगिक उत्पन्न करते हैं जो डीएनए को नुकसान पहुँचाते हैं, उत्परिवर्तन उत्पन्न करते हैं और कैंसर के विकास को बढ़ावा देते हैं। इसके विपरीत, अन्य सूक्ष्मजीव चयापचय को प्रेरित कर सकते हैं जो ट्यूमर कोशिकाओं की वृद्धि को कम करता है। स्तन ऊतक में, अध्ययनों ने सूजन और चयापचय पथों में शामिल बैक्टीरिया की उपस्थिति का दस्तावेजीकरण किया है; प्रोस्टेट में, सूक्ष्मजीवी परिवर्तन रोग की प्रगति और एंटी-एंड्रोजन थेरेपी की प्रतिक्रिया से जुड़े होते हैं; और फेफड़ों में, अंतर्जात माइक्रोबायोम धूम्रपान से प्रेरित सूजन के साथ परस्पर क्रिया कर सकता है और सूक्ष्म वातावरण को संशोधित कर सकता है जिससे ट्यूमर इम्यूनोथेरेपी के प्रति कम प्रतिक्रियाशील हो जाते हैं।
इंट्राट्यूमरल माइक्रोबायोम की उपस्थिति या संरचना कीमोथेरेपी, रेडियोथेरेपी और विशेष रूप से इम्यूनोथेरेपी की प्रभावकारिता को बदल सकती है। इन प्रक्रियाओं में सूक्ष्म वातावरण (पीएच, पोषण) में परिवर्तन, स्थानीय दवा निष्क्रियता (कुछ बैक्टीरिया में दवा-अपघटनकारी एंजाइम होते हैं), या एंटीजन प्रस्तुति और प्रतिरक्षा कोशिका घुसपैठ का मॉड्यूलेशन शामिल हैं। कई अध्ययनों से पता चला है कि ट्यूमर माइक्रोबायोटा में अंतर प्रतिरक्षा जांच बिंदु अवरोधकों (आईसीआई) के प्रति प्रतिक्रिया या प्रतिरोध से जुड़ा है।
ट्यूमर ऊतक में स्थानीय माइक्रोबायोम संशोधन - मौजूदा और जांचात्मक रणनीतियाँ
ट्यूमर माइक्रोबायोम में सीधे हस्तक्षेप करने का विचार उपचार के नए रास्ते खोल रहा है। कुछ उपाय जो विकसित किए गए हैं या विकसित किए जा रहे हैं, उनमें शामिल हैं:
कुछ प्रायोगिक मॉडलों में, ट्यूमर में "खराब" प्रजातियों को खत्म करने के लिए एंटीबायोटिक दवाओं के इस्तेमाल से दवाओं के प्रति ऊतकों की प्रतिक्रिया बदल गई है। हालाँकि, प्रणालीगत एंटीबायोटिक दवाओं के व्यापक प्रभाव होते हैं (और प्रतिरक्षा के लिए आवश्यक आंत माइक्रोबायोम को प्रभावित कर सकते हैं), इसलिए स्थानीय एंटीबायोटिक दवाओं का उपयोग या लक्षित प्रजातियों के लिए चुनिंदा एंटीबायोटिक दवाओं का विकास प्राथमिकता है।
विचार यह है कि ट्यूमर के ऊतकों में ऐसे इंजीनियर्ड बैक्टीरिया डाले जाएँ जो प्रतिरक्षा-उत्तेजक साइटोकिन्स, pH बदलने वाले मेटाबॉलिक एंजाइम, या प्रतिरक्षा-दमनकारी दवाओं को तोड़ने वाले एंजाइम स्रावित करते हैं। स्थानीय स्तर पर दवाएँ पहुँचाने के लिए कमज़ोर बैक्टीरिया का उपयोग करने वाले कुछ पूर्व-नैदानिक परीक्षणों ने आशाजनक परिणाम दिखाए हैं।
ऑन्कोलिटिक वायरस का अध्ययन कैंसर कोशिकाओं को सीधे मारने और साथ ही ट्यूमर-रोधी प्रतिरक्षा को उत्तेजित करने के लिए किया गया है। ऑन्कोलिटिक वायरस को माइक्रोबायोम एडिटिंग के साथ मिलाने से स्थानीय टी कोशिका सक्रियण में वृद्धि हो सकती है और प्रणालीगत प्रतिक्रियाओं का विस्तार हो सकता है।
यद्यपि यहां विषय स्थानीय सूक्ष्म जीव विज्ञान है, लेकिन यह ध्यान रखना महत्वपूर्ण है कि आंत-ट्यूमर अक्ष मौजूद है: आंत माइक्रोबायोम में परिवर्तन (उदाहरण के लिए, आहार, प्रोबायोटिक्स, एफएमटी के माध्यम से) अप्रत्यक्ष रूप से इंट्राट्यूमरल माइक्रोबायोम और प्रणालीगत प्रतिरक्षा को बदल सकता है, जिससे फेफड़े, स्तन या प्रोस्टेट में ट्यूमर ऊतक प्रभावित हो सकता है।

वैज्ञानिक ट्यूमर ऊतक में सूक्ष्मजीवी डीएनए का विश्लेषण कर रहे हैं ताकि ऐसी प्रजातियों का पता लगाया जा सके जो कैंसर उपचार की प्रभावशीलता को प्रभावित करती हैं।
नैदानिक चुनौतियाँ और विचार
- "कारण" और "प्रभाव" के बीच अंतर: कई वर्तमान अध्ययन अभी भी सहसंबंधों का वर्णन करते हैं, लेकिन सूक्ष्म जीव विज्ञान और ट्यूमर प्रगति के बीच किसी कारण संबंध की पुष्टि नहीं की है।
- तकनीकी मानकीकरण: नमूनाकरण, डीएनए/आरएनए पृथक्करण, बहिर्जात संदूषण से बचाव, तथा जैवसूचना विश्लेषण, सभी के लिए विश्वसनीय परिणामों के लिए मानकीकरण की आवश्यकता होती है।
- रोगियों के बीच उच्च परिवर्तनशीलता: माइक्रोबायोम व्यक्ति-आधारित है; हस्तक्षेप को व्यक्तिगत बनाने की आवश्यकता है।
- सुरक्षा: ट्यूमर ऊतक में जीवित बैक्टीरिया या वायरस डालने से संक्रमण या प्रतिरक्षा प्रतिक्रिया का खतरा रहता है; इन उपचारों के लिए कठोर परीक्षण की आवश्यकता होती है।
ट्यूमर-संबंधी माइक्रोबायोम का अध्ययन ऑन्कोलॉजी में जीव विज्ञान की एक नई परत खोलता है: स्थानीय माइक्रोबायोम कैंसर को बढ़ावा देने वाला और प्रतिरक्षा मॉड्यूलेशन तथा ट्यूमर तक लक्षित दवा पहुँचाने का एक उपकरण दोनों हो सकता है। अनुक्रमण, ऊतक विज्ञान, बायोमिमिक्री और माइक्रोबायोम-इंजीनियरिंग तकनीकों में प्रगति के साथ, निकट भविष्य में ऐसी चिकित्सीय रणनीतियाँ सामने आएंगी जो स्थानीय माइक्रोबायोम को लक्षित या उनका दोहन करेंगी—जैव-अभियांत्रिकी बैक्टीरिया, चयनात्मक फेज से लेकर प्रतिरक्षा-सक्षम ऑन्कोलिटिक वायरस तक—मल्टीमॉडल थेरेपी का हिस्सा बन जाएँगी।
हालाँकि, नैदानिक रास्ता अभी भी लंबा है; परीक्षण का मानकीकरण, कारण-कार्य संबंध का प्रदर्शन, और सुरक्षा का आश्वासन, इन हस्तक्षेपों को व्यापक रूप से अपनाने से पहले आवश्यक शर्तें होंगी।
स्रोत: https://suckhoedoisong.vn/lieu-co-the-chua-ung-thu-bang-cach-dieu-chinh-vi-sinh-trong-mo-u-169251028135655078.htm







































































































टिप्पणी (0)