クローン猿は今も元気に生きている。
火曜日にネイチャー・コミュニケーションズ誌に掲載されたこの研究は、新たにクローン化されたアカゲザル「レトロ」について述べている。論文著者の一人であるファロン・ルー氏は、このサルは健康で順調に成長していると述べた。

レトロと名付けられたクローンアカゲザルは、現在も元気に生きている。写真:ネイチャー・コミュニケーションズ
「私たちは初めて健康なアカゲザルのクローンを作成しました。従来の受精卵に比べると効率は非常に低いものの、これは非常に大きな一歩であり、不可能と思われていました」と、中国科学院分子発生生物学国家重点実験室および遺伝学・発生生物学研究所の専門家、法龍陸氏は述べた。
霊長類はクローン作成が最も難しい種の一つです。科学者たちは長年、クローン細胞を正常な胚の細胞に置き換えることに成功していません。彼らは、この新技術を用いて、医学研究用に同一のアカゲザルを作り出すことを目指しています。
しかし、多くの研究者は、この新しい方法の成功率はまだ非常に低く、クローンをめぐる倫理的な疑問が生じていると警告している。
クローン化された最初の哺乳類は、体細胞核移植(SCNT)と呼ばれる技術を使用して1996年に作成された羊のドリーでした。
この成果以来、科学者らは豚、牛、馬、犬など多くの哺乳類のクローンを作成してきたが、これは通常、非常に少数の胚を代理動物に移植して生存可能な子孫を生み出すというプロセスである。
新しいクローン作成方法とは何ですか?
研究チームは、カニクイザル(Macaca fascicularis)に改良版のSCNT法を使用し、さらにその技術を改良してアカゲザル(Macaca mulatta)のクローンを作成した。

クローンサル「レトロ」、生後17ヶ月。写真:ネイチャー・コミュニケーションズ
何百回もの失敗を経て、研究者たちは内部細胞塊移植と呼ばれるプロセスを実行した。これはクローン化された内部細胞を非クローン胚に導入するものである。
これにより、クローンは正常に発育することができました。研究チームはその後、113個の再構成胚を用いてこの新技術を試験しました。そのうち11個は7匹の代理母動物に移植されましたが、生存したのは1匹だけでした。
「今後の私たちの主な焦点は、霊長類におけるSCNTの成功率を向上させる研究です」とファロン・ルー氏は語った。
実は、最初のクローンサルはレトロではなく、Zhong ZhongとHua Huaという名の、一組の同じ体を持つカニクイザルでした。この2匹は2018年に、上海にある中国科学院神経科学研究所の研究者によってSCNT法を用いて誕生しました。
チュンチュンとホアホアは現在6歳を超え、仲間の猿たちと幸せに健康に暮らしています。ルー氏によると、これまでのところ、研究者たちはクローン猿の寿命に潜在的な限界は見出せていないとのことです。
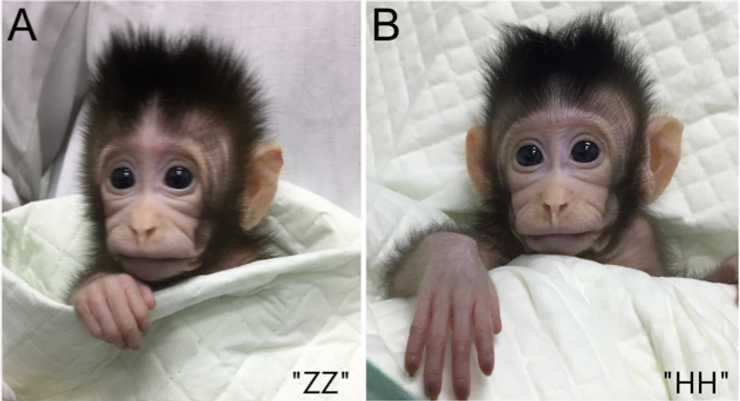
クローンマカクのZhong Zhong(ZZ)とHua Hua(HH)。写真:Liu et al Cell
倫理的な議論
科学研究におけるサルの使用は、動物福祉の観点から倫理的な問題で議論の的となっている。スペイン国立バイオテクノロジーセンターの科学者、ルイス・モントリウ氏は、この研究には関与していないが、当初の113個の胚のうち生存したのは1個だけであり、成功率は1%未満であると指摘した。
「まず、霊長類のクローンは可能です。そして、同様に重要な第二に、こうした実験は成功率が非常に低く、成功させるのが非常に困難です」とモントリュー氏は述べた。
同氏はさらに、この実験の成功率の低さは人間のクローン作成が不必要かつ物議を醸すものであることを示し、もし試みられたとしても「極めて困難で倫理的に正当化できない」ものになるだろうと述べた。
一方、英国王立動物虐待防止協会は、「クローン技術を動物に適用することについては、倫理的および福祉上の深刻な懸念がある。動物のクローン作成には、動物に苦痛や不快感を与える可能性のある手順が必要であり、失敗率や死亡率も高い」と述べた。
サルのクローンの重要性
さまざまな意見がある中、研究チームは、科学研究における非ヒト霊長類の使用に関する中国の法律とガイドラインに依然として従っていると述べた。
中国科学工学医学院の委員会が5月に発表した報告書によると、人間と多くの類似点を持つ霊長類の研究は、新型コロナウイルス感染症ワクチンの開発など、多くの医学的進歩につながる重要な役割を果たすだろうという。
研究チームは、マウスを用いた実験に限界があるため、クローンサルの成功は生物医学研究の加速につながる可能性があると述べた。エステバン氏はまた、遺伝的に同一のサルを作成することは、様々な用途で役立つ可能性があると考えている。
「この研究は、ヒト以外の霊長類でもクローン化が可能であることの証明であり、より効率的な新たな手法への道を開くものです。クローンサルは、野生のサルでは不可能な複雑な方法で遺伝子改変を行うことができます。これは、疾患モデル化や保全活動に多くの影響を与えるでしょう」とエステバン氏は述べた。
ホアイ・フオン氏(CNN、AFPによる)
[広告2]
ソース







![[写真] ファム・ミン・チン首相が、中部各省の洪水被害を克服するための解決策を議論する会議を主宰した。](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/10/29/1761716305524_dsc-7735-jpg.webp)































































![[インフォグラフィック] 2021年から2025年までの5年間のベトナムの社会経済状況:印象的な数字](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/10/29/1761730747150_anh-man-hinh-2025-10-29-luc-16-38-55.png)



![[ライブ] ハロン2025コンサート:「伝統の精神 - 未来を明るくする」](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/10/29/1761743605124_g-anh-sang-am-thanh-hoanh-trang-cua-chuong-trinh-mang-den-trai-nghiem-dang-nho-cho-du-khach-22450328-17617424836781829598445-93-0-733-1024-crop-1761742492749383512980.jpeg)






























コメント (0)