Le ministère de la Santé vient de publier la décision n° 1703/QD-BYT promulguant le « Plan de mise en œuvre du mois de pointe pour lutter contre et repousser la contrebande, la fraude commerciale, les produits contrefaits et la violation des droits de propriété intellectuelle » du 15 mai au 15 juin.
Inspecter, détecter et traiter les infractions de contrebande, de fraude commerciale et de contrefaçon dans le domaine médical.
Français Selon le ministère de la Santé, le Plan de mise en œuvre du mois de pointe de lutte et de prévention de la contrebande, de la fraude commerciale, des produits contrefaits et de la violation des droits de propriété intellectuelle a été publié dans le but de mettre en œuvre les instructions contenues dans les documents suivants : Dépêche officielle n° 41/CD-TTg du 17 avril 2025 sur le traitement des cas de production et de commerce de médicaments et d'aliments de protection de la santé contrefaits ;
Dépêche officielle n° 55/CD-TTg du 2 mai 2025 sur le renforcement de la coordination et le traitement strict des organisations et des individus impliqués dans la production et le commerce de faux médicaments, de faux lait et de faux aliments de protection de la santé ;
Télégramme n° 65/CD-TTg du 15 mai 2025 portant lancement d'une période de pointe pour lutter contre et repousser la contrebande, la fraude commerciale, les marchandises contrefaites et les atteintes aux droits de propriété intellectuelle ;
Directive n° 13/CT-TTg du 17 mai 2025 du Premier Ministre relative au renforcement de la lutte contre la contrebande, la fraude commerciale et les marchandises contrefaites dans la nouvelle situation.
Déployer un mois de pointe dans l'ensemble du secteur de la santé pour inspecter et contrôler la mise en œuvre des réglementations légales liées au commerce, à la production et aux activités commerciales des entreprises pharmaceutiques, d'aliments fonctionnels, de cosmétiques et d'équipements médicaux afin de combattre, prévenir, repousser et finalement mettre fin à la contrebande, à la fraude commerciale, à la production et à la circulation de produits contrefaits (pour les produits pharmaceutiques, cosmétiques, les aliments fonctionnels, la médecine traditionnelle et les équipements médicaux) ; protéger les droits et intérêts légitimes des personnes et des entreprises.
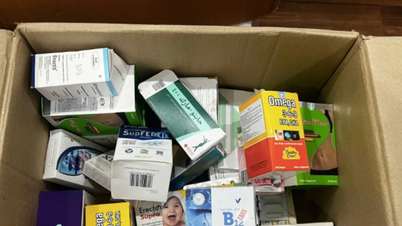
Dans le même temps, il faut détecter rapidement et traiter strictement les actes de fabrication et de commerce de produits pharmaceutiques, cosmétiques, aliments fonctionnels, médicaments traditionnels et équipements médicaux contrefaits, de contrebande et d’origine inconnue.
Dans le plan, le ministère de la Santé exige la mise en œuvre synchrone et drastique de l’inspection, de la détection et du traitement des violations de la contrebande, de la fraude commerciale et des produits contrefaits dans le domaine médical ; Renforcer l’efficacité de la gestion, créer des changements révolutionnaires dans le travail de prévention et de lutte contre la contrebande, la fraude commerciale et la contrefaçon de médicaments, de cosmétiques, d’aliments fonctionnels et d’équipements médicaux ;
Coordination étroite entre les agences fonctionnelles et les niveaux de gestion du niveau central au niveau local dans la lutte contre la contrefaçon de médicaments, de cosmétiques, d’aliments fonctionnels et d’équipements médicaux.
Assurer la régularité, la continuité et la continuité du travail de lutte contre la contrebande, la fraude commerciale et la contrefaçon dans le secteur de la santé.
Mettre en place 15 équipes d’inspection liées aux domaines des produits pharmaceutiques, des cosmétiques, de la médecine traditionnelle, du lait, des aliments fonctionnels et des équipements médicaux.
Dans le cadre de ce plan, le ministère de la Santé a également mis en place des équipes d’inspection dans les unités relevant du ministère de la Santé et des départements de la Santé des provinces et des villes, notamment :
La Drug Administration a créé cinq équipes d’inspection chargées de contrôler la mise en œuvre des réglementations légales sur les produits pharmaceutiques et cosmétiques dans les établissements produisant, exportant, important et vendant en gros des médicaments, des ingrédients pharmaceutiques et des cosmétiques ;
Le Département de médecine traditionnelle et de pharmacie a créé deux équipes d'inspection chargées de contrôler la mise en œuvre des réglementations légales sur les médicaments traditionnels, les herbes médicinales et les ingrédients médicinaux traditionnels dans les établissements de production, d'exportation, d'importation, de vente en gros et au détail et dans les cliniques utilisant la médecine traditionnelle ;
Le Département de la sécurité alimentaire a mis en place cinq équipes d’inspection chargées de contrôler la mise en œuvre des réglementations en matière de sécurité alimentaire dans les établissements qui produisent, exportent, importent et commercialisent des ingrédients alimentaires, du lait et des aliments fonctionnels ;
Le Département des infrastructures et des équipements médicaux a créé trois équipes d'inspection chargées de contrôler la mise en œuvre des réglementations légales sur les équipements médicaux dans les établissements qui fabriquent, exportent, importent et commercialisent des équipements médicaux.
Le personnel participant aux équipes d'inspection de chaque département est composé de fonctionnaires travaillant au département et de fonctionnaires d'autres unités qui sont réquisitionnés.
Le ministère de la Santé demande aux départements de la Santé des provinces et des villes gérées par le gouvernement central de conseiller au Comité populaire provincial de créer des équipes d'inspection pour la production, le commerce et les activités des produits pharmaceutiques, des cosmétiques, des aliments fonctionnels, des médicaments traditionnels et des équipements médicaux dans le cadre de leur gestion.
Les sujets d'inspection sont les entreprises de fabrication, d'exportation et d'importation ainsi que les ménages commerçant directement dans le domaine des produits pharmaceutiques, des cosmétiques, des aliments fonctionnels, des médicaments traditionnels et des équipements médicaux.
Le contenu de l'inspection porte sur les activités de production, d'exploitation, de conservation et de stockage : Mise en œuvre des lois et réglementations sur les produits pharmaceutiques et cosmétiques dans les établissements produisant, exportant, important et vendant en gros des médicaments, des ingrédients pharmaceutiques et des cosmétiques ;
Mise en œuvre des lois et réglementations sur les médecines traditionnelles, les herbes médicinales et les ingrédients médicinaux traditionnels dans les domaines de la production, de l’exportation, de l’importation, de la vente en gros, de la vente au détail et des cliniques de médecine traditionnelle ;
Mise en œuvre des lois et réglementations sur la sécurité alimentaire dans les établissements de production, d’exportation et d’importation et dans les entreprises commerciales qui commercialisent directement des ingrédients alimentaires, du lait et des aliments fonctionnels ;
Mise en œuvre des lois et règlements sur les équipements médicaux dans les établissements de fabrication, d'exportation, d'importation et de commercialisation d'équipements médicaux.
Activités publicitaires de la médecine traditionnelle et des aliments fonctionnels, y compris la vérification de la participation des scientifiques et des gestionnaires du secteur de la santé aux activités publicitaires. Par l’inspection, la correction et le traitement des publicités mensongères et des activités publicitaires excessives.
Le ministère de la Santé exige que les scientifiques et les gestionnaires du secteur de la santé signent un engagement à ne pas faire de publicité ni à introduire de fausses informations, des informations dénuées de fondement ou de fondement scientifique, ou exagérant les caractéristiques et les utilisations des produits.
Signez un engagement à ne pas exagérer les caractéristiques et les utilisations du produit
Le ministère de la Santé exige que les scientifiques et les responsables du secteur de la santé signent un engagement à ne pas faire de publicité ni à introduire de fausses informations, des informations dénuées de fondement ou de fondement scientifique, ou à exagérer les caractéristiques et les utilisations des produits sans vérifier soigneusement les documents juridiques relatifs aux produits ; être responsable devant la loi de toute publicité frauduleuse.
Renforcer le travail d’information et de communication : Promouvoir les activités d’information et de communication sur les risques et les méfaits de l’utilisation de faux médicaments et de faux aliments de protection de la santé d’origine inconnue.
Lancer un mouvement pour que les gens participent à la réponse au contrôle de la qualité des médicaments et des aliments : Propagande et explication des dangers de la contrebande, de la fraude commerciale, des produits contrefaits, des produits qui portent atteinte aux droits de propriété intellectuelle et de la violation du droit d'auteur.
Lancer un mouvement national pour dénoncer les produits contrefaits à travers les journaux et les réseaux sociaux. Bilan et évaluation de la période de pointe de mise en œuvre de la lutte, de la prévention, du refoulement et finalement de la fin de la contrebande, de la fraude commerciale, de la production et de la circulation des marchandises contrefaites.
Source : https://nhandan.vn/bo-y-te-ra-quan-kiem-tra-ve-duoc-my-pham-thuc-pham-chuc-nang-thiet-bi-y-te-post881483.html



![[Photo] Le Premier ministre Pham Minh Chinh préside la réunion spéciale du gouvernement sur l'élaboration des lois en mai](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/22/1c880aae96fd4e0894abc47a46fe19ba)

![[Photo] Le secrétaire général To Lam travaille avec la Commission centrale d'inspection](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/22/54820e91fd124c4cb691961718c4ee5d)















![[Photo] Le Premier ministre Pham Minh Chinh préside la réunion spéciale du gouvernement sur l'élaboration des lois en mai](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/5/22/1c880aae96fd4e0894abc47a46fe19ba)


![[Photo] Le secrétaire général To Lam travaille avec la Commission centrale d'inspection](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/5/22/54820e91fd124c4cb691961718c4ee5d)































































Comment (0)