Ces dernières années, un changement majeur dans notre compréhension du cancer a été la prise de conscience que les micro-organismes résident non seulement dans l'intestin, mais aussi dans les tissus tumoraux, notamment les tumeurs solides comme celles du sein, de la prostate et du poumon. Ces communautés microbiennes (appelées collectivement microbiome intratumoral ou microbiome associé à la tumeur) interagissent directement avec les cellules cancéreuses, les cellules immunitaires et le microenvironnement, influençant ainsi la biologie tumorale, la réponse au traitement et le pronostic.
Le microbiote des tissus tumoraux est-il différent du microbiote intestinal ?
On pensait auparavant que le tissu tumoral était une « zone stérile », mais des analyses génomiques et de séquençage récentes ont révélé la présence d'ADN et d'ARN microbiens dans de nombreux échantillons tumoraux réséqués. Ces microbes peuvent résider à l'intérieur des cellules cancéreuses, des cellules immunitaires ou être intégrés au tissu conjonctif environnant. La composition et la densité microbiennes varient selon le type de tumeur et le patient ; par exemple, les tumeurs du sein présentent une diversité microbienne relativement élevée comparée à d'autres tumeurs. Leur localisation (intracellulaire ou extracellulaire) détermine leur impact sur le tissu malade.
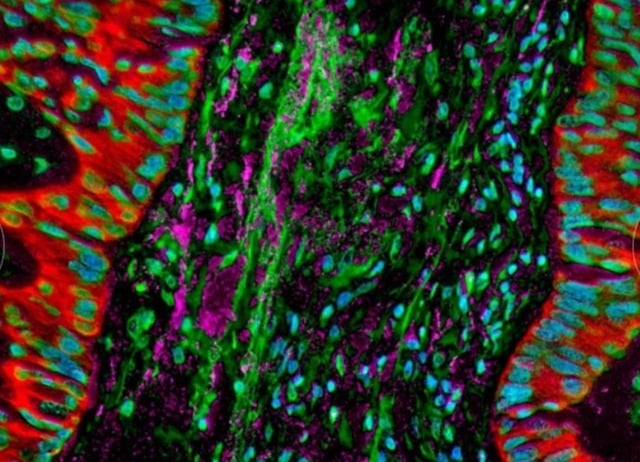
Des images microscopiques montrent des bactéries résidant dans les cellules cancéreuses du poumon, modifiant la réponse immunitaire de l'organisme.
Le rôle des bactéries et des virus dans les tissus du sein, de la prostate et du poumon
Le microbiote local peut moduler l'environnement immunitaire de façon suppressive ou activatrice. Certains microbes déclenchent des signaux inflammatoires chroniques (par exemple, via des récepteurs de reconnaissance de motifs comme les TLR), entraînant une augmentation des cytokines pro-inflammatoires. Ces dernières attirent des cellules immunitaires suppressives (macrophages M2, lymphocytes T régulateurs) et contribuent ainsi à l'échappement tumoral au système immunitaire. À l'inverse, certaines bactéries ou certains virus peuvent stimuler l'immunité cellulaire (présentation accrue d'antigènes, activation des lymphocytes T CD8+) et contribuer à l'efficacité de l'immunothérapie. Ainsi, un même microbiote peut être un allié ou un ennemi selon le contexte.
Certaines bactéries produisent des toxines ou des composés qui endommagent l'ADN, provoquant des mutations et favorisant la progression du cancer. À l'inverse, d'autres microbes peuvent induire un métabolisme qui réduit la croissance des cellules tumorales. Dans le tissu mammaire, des études ont mis en évidence la présence de bactéries impliquées dans les voies inflammatoires et métaboliques ; dans la prostate, des modifications microbiennes sont associées à la progression de la maladie et à la réponse à l'hormonothérapie anti-androgénique ; et dans le poumon, le microbiome endogène peut interagir avec l'inflammation induite par le tabagisme et modifier le microenvironnement, rendant ainsi les tumeurs moins sensibles à l'immunothérapie.
La présence et la composition du microbiome intratumoral peuvent modifier l'efficacité de la chimiothérapie, de la radiothérapie et, surtout, de l'immunothérapie. Parmi les mécanismes impliqués figurent des altérations du microenvironnement (pH, nutrition), l'inactivation locale des médicaments (certaines bactéries possèdent des enzymes de dégradation des médicaments) ou la modulation de la présentation des antigènes et de l'infiltration des cellules immunitaires. Plusieurs études ont montré que des différences dans le microbiote tumoral sont associées à la réponse ou à la résistance aux inhibiteurs de points de contrôle immunitaire (ICI).
Modification locale du microbiome dans les tissus tumoraux : stratégies existantes et expérimentales
L’idée d’intervenir directement sur le microbiome tumoral ouvre de nouvelles perspectives thérapeutiques. Parmi les approches développées ou en cours de développement, on peut citer :
Dans certains modèles expérimentaux, l'utilisation d'antibiotiques pour éliminer les espèces pathogènes des tumeurs a modifié la réponse tissulaire à ces médicaments. Cependant, les antibiotiques systémiques ont des effets étendus (et peuvent perturber le microbiote intestinal, essentiel à l'immunité) ; par conséquent, l'utilisation locale d'antibiotiques ou le développement d'antibiotiques sélectifs pour les espèces cibles constituent une priorité.
L'idée est d'introduire dans le tissu tumoral des bactéries modifiées qui sécrètent des cytokines stimulant le système immunitaire, des enzymes métaboliques modifiant le pH ou des enzymes dégradant les immunosuppresseurs. Certains essais précliniques utilisant des bactéries atténuées pour administrer des médicaments localement se sont révélés prometteurs.
Des virus oncolytiques ont été étudiés pour leur capacité à détruire directement les cellules cancéreuses et à stimuler simultanément l'immunité antitumorale. L'association de ces virus à la modification du microbiome pourrait renforcer l'activation locale des lymphocytes T et amplifier les réponses systémiques.
Bien que le sujet traité ici soit la microbiologie locale, il est important de noter qu'il existe un axe intestin-tumeur : les altérations du microbiome intestinal (par exemple, par le biais de l'alimentation, des probiotiques, de la FMT) peuvent indirectement modifier le microbiome intratumoral et l'immunité systémique, influençant ainsi le tissu tumoral du poumon, du sein ou de la prostate.

Des scientifiques analysent l'ADN microbien présent dans les tissus tumoraux afin de trouver les espèces qui influencent l'efficacité du traitement du cancer.
Défis et considérations cliniques
- Distinguer entre « cause » et « effet » : de nombreuses études actuelles décrivent encore des corrélations mais n'ont pas confirmé de relation causale entre la microbiologie et la progression tumorale.
- Standardisation technique : l’échantillonnage, l’isolement de l’ADN/ARN, la prévention de la contamination exogène et l’analyse bioinformatique nécessitent tous une standardisation pour obtenir des résultats fiables.
- Forte variabilité interindividuelle : le microbiome est propre à chaque individu ; les interventions doivent être individualisées.
- Sécurité : L’introduction de bactéries ou de virus vivants dans les tissus tumoraux comporte un risque d’infection ou de réaction immunitaire excessive ; ces thérapies nécessitent des tests rigoureux.
L'étude du microbiome associé aux tumeurs ouvre une nouvelle perspective en oncologie : le microbiome local peut à la fois favoriser le cancer et servir d'outil de modulation immunitaire et d'administration ciblée de médicaments aux tumeurs. Grâce aux progrès réalisés dans les domaines du séquençage, de l'histologie, du biomimétisme et des techniques d'ingénierie du microbiome, les stratégies thérapeutiques ciblant ou exploitant le microbiome local – des bactéries bio-ingénierées aux virus oncolytiques immunocompétents, en passant par les phages sélectifs – devraient bientôt s'intégrer aux thérapies multimodales.
Cependant, le chemin clinique est encore long ; la standardisation des tests, la démonstration de la causalité et la garantie de la sécurité seront des conditions préalables avant que ces interventions ne soient largement adoptées.
Source : https://suckhoedoisong.vn/lieu-co-the-chua-ung-thu-bang-cach-dieu-chinh-vi-sinh-trong-mo-u-169251028135655078.htm







































































































Comment (0)