Управление по контролю за оборотом лекарственных средств ( Министерство здравоохранения ) только что опубликовало список иностранных фармацевтических предприятий, выпускающих препараты, не соответствующие стандартам качества, которые обязаны продолжать отбор проб и тестирование 100% партий импортируемых лекарств. Все 46 компаний из разных стран имеют многократные нарушения.
В Постановлении Управления по контролю за оборотом лекарственных средств № 4318 от 2 декабря, направленном в департаменты здравоохранения провинций, городов и предприятиям-импортерам лекарственных средств, указано, что по результатам контроля качества лекарственных средств, находящихся в обращении, и проверки организаций, производящих лекарственные средства с нарушениями, а также предприятий-изготовителей иностранных лекарственных средств, подлежащих исключению из списка организаций, обязанных отбирать образцы для проведения испытаний качества 100% партий импортируемых лекарственных средств, Управление по контролю за оборотом лекарственных средств объявляет о публикации списка организаций, производящих лекарственные средства с нарушениями качества, которые обязаны отбирать образцы для проведения испытаний качества 100% партий импортируемых лекарственных средств (предварительная инспекция).
В этом списке индийские предприятия по-прежнему остаются страной с наибольшим числом нарушителей. Ряд компаний, появившихся в списке с 2013 по 2015 год, по сей день находятся под предварительным контролем.
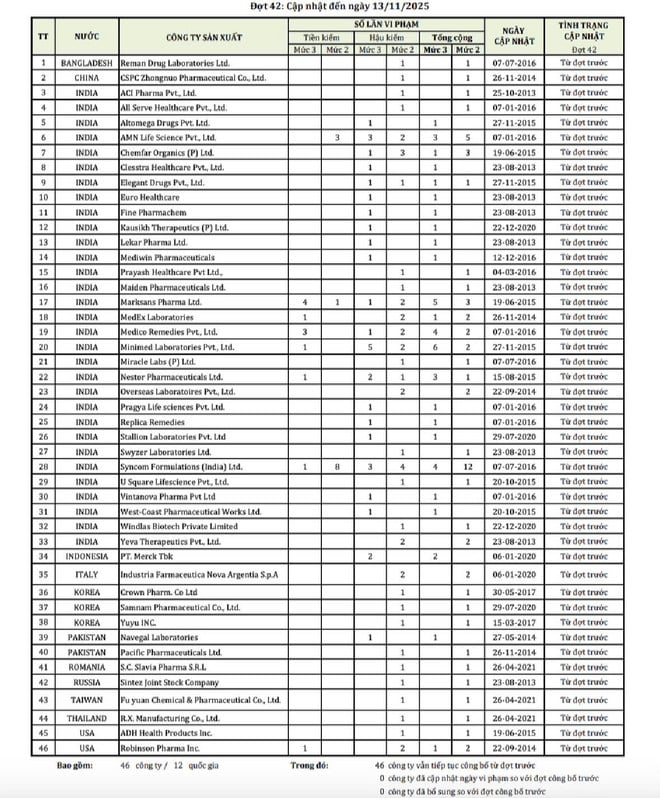
Список 46 иностранных фармацевтических компаний, чьи препараты нарушают требования к качеству. (Источник: Управление по контролю за лекарственными средствами)
Помимо большой группы компаний из Индии, под особым надзором продолжают находиться многие компании из Бангладеш, Китая, Индонезии, Южной Кореи, Пакистана, США, Италии и Румынии. Такие компании, как Reman Drug Laboratories (Бангладеш), CSPC Zhongnuo (Китай), PT. Merck Tbk (Индонезия), а также Crown Pharm и Yuyu Inc. (Южная Корея), были объявлены нарушителями в самом начале, но пока не выполнили требования для отмены предварительной проверки.
В этом списке есть две американские компании — ADH Health Products и Robinson Pharma, у которых были выявлены нарушения качества как до, так и после инспекции.
Общим для всех 46 компаний является то, что все они импортировали во Вьетнам лекарственные препараты, не соответствующие стандартам качества, требующим строгого контроля продукции перед ее выпуском в обращение.
В дополнение к списку нарушений Управление по контролю за лекарственными средствами также заявило, что 98 компаний из 16 стран были исключены из списка мониторинга после завершения периода предварительной проверки, и новых нарушений не было.
Управление по контролю за лекарственными средствами Вьетнама просит Департаменты здравоохранения провинций, городов и секторов здравоохранения поручить подразделениям по контролю, инспекции и тестированию лекарственных средств, находящимся в подчинении Департамента, проводить проверки и надзор за соблюдением правил проверки качества импортируемых лекарственных средств, находящихся в обращении в зоне управления, а также принимать меры в отношении организаций/лиц, нарушающих действующие правила.
(Вьетнам+)
Источник: https://www.vietnamplus.vn/cong-bo-danh-sach-46-cong-ty-duoc-nuoc-ngoai-co-thuoc-vi-pham-chat-luong-post1080823.vnp



![[Фото] Кат Ба — райский зеленый остров](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F12%2F04%2F1764821844074_ndo_br_1-dcbthienduongxanh638-jpg.webp&w=3840&q=75)













































![[VIMC 40 дней молниеносной скорости] Порт Хайфон полон решимости прорваться, достигнув цели в 2 миллиона TEU к 2025 году](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/12/04/1764816441820_chp_4-12-25.jpeg)






















































Комментарий (0)