Управление по контролю за продуктами и лекарствами США (FDA) одобрило революционную терапию генной инженерии для лечения серповидноклеточной анемии.
Решение FDA было принято 9 декабря. Два одобренных метода лечения называются Casgevy, основанный на удостоенной Нобелевской премии технологии редактирования генов CRISPR, и Lyfgenia, которая использует безвредный вирус для редактирования генов.
Препарат «Касгеви» производится двумя компаниями: Vertex Pharmaceuticals (США) и CRISPR Therapeutics (Швейцария). Препарат восстанавливает поврежденные гены в стволовых клетках пациентов в возрасте 12 лет и старше с серповидноклеточной анемией и талассемией.
Оба заболевания вызваны дефектами гена гемоглобина. Генная терапия обычно стоит миллионы долларов и недоступна для многих пациентов. Производитель, Vertex Pharmaceuticals, стремится поддерживать цены на максимально низком уровне.
Одобрение FDA поступило после того, как в ноябре терапию одобрило Агентство по регулированию оборота лекарственных средств и изделий медицинского назначения Великобритании (MHRA).
Lyfgenia, в свою очередь, использует перенос генов для редактирования генов. Препарат изменяет стволовые клетки крови пациента, чтобы они вырабатывали гемоглобин, полученный из гена. По данным FDA, добавление гемоглобина к эритроцитам снижает риск серповидноклеточной анемии.
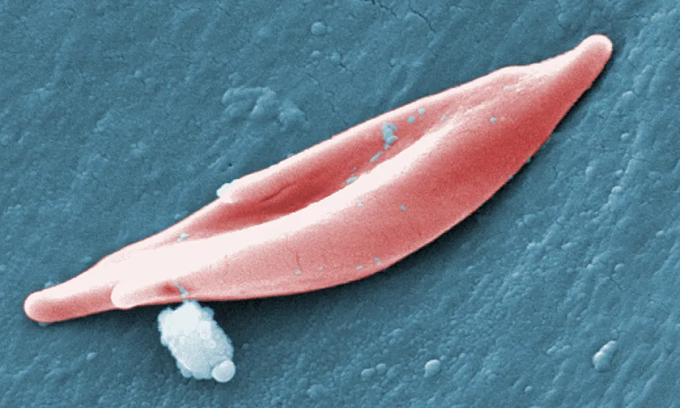
Серповидный эритроцит. Фото: CDC.
«Это значительный прогресс в области генной терапии для пациентов с серповидноклеточной анемией. Их потенциал изменить жизнь огромен», — заявил Питер Маркс, директор Центра оценки и исследований биологических препаратов FDA.
По словам доктора Николь Верден из FDA, генная терапия делает лечение более целенаправленным и эффективным, особенно для людей с редкими заболеваниями, у которых ограниченные возможности лечения.
Она добавила, что FDA «очень рада продвижению этой области», поскольку они помогают людям, чья жизнь серьезно нарушена этой болезнью.
Одобрение агентства означает, что около 16 000 человек с серповидноклеточной анемией получат потенциальный вариант лечения. Это заболевание поражает около 100 000 американцев и более 7,7 миллиона человек по всему миру, в основном африканского и карибского происхождения. Это редкое, изнурительное и опасное для жизни заболевание крови, и многие из них не имеют достаточного лечения.
У пациентов с серповидноклеточной анемией клетки крови имеют удлинённую серповидную форму вместо типичных вогнутых круглых. Деформированные клетки застревают в кровеносных сосудах, блокируя поступление кислорода, вызывая сильную боль, инсульты и повреждение органов.
Тхук Линь (по данным AFP, AP )
Ссылка на источник


![[Фото] 60-я годовщина основания Вьетнамской ассоциации фотохудожников](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F12%2F05%2F1764935864512_a1-bnd-0841-9740-jpg.webp&w=3840&q=75)

![[Фото] Кат Ба — райский зеленый остров](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F12%2F04%2F1764821844074_ndo_br_1-dcbthienduongxanh638-jpg.webp&w=3840&q=75)








































































































Комментарий (0)