Russlands Pembroria er ikke en ny indikasjon for kreftmedisiner.
Om kvelden 13. november utstedte K Hospital ( Hanoi ) en melding om sirkulasjon av kreftbehandlingsmedisinen Pembroria (aktiv ingrediens pembrolizumab) i Vietnam.
Ifølge K Hospital ble Keytruda oppfunnet i Vietnam av MSD i USA, med den aktive ingrediensen pembrolizumab, pakket i flasker på 100 mg/4 ml og lisensiert for sirkulasjon av Vietnams legemiddeltilsyn ( Helsedepartementet ) siden 2017.
Pembrolizumab er i hovedsak et monoklonalt anti-PD-1-antistoff og er et biologisk legemiddel indisert for visse typer kreft, som tilhører gruppen immunterapi. Legemidlet administreres ved intravenøs infusjon på et medisinsk anlegg.
Keytruda er godkjent av Helsedepartementet for 14 indikasjoner, inkludert malignt melanom, ikke-småcellet lungekreft, klassisk Hodgkins lymfom, urotelialt karsinom, plateepitelkreft i hode og nakke, magekreft, kreft med høyt nivå av mikrosatellittinstabilitet og livmorhalskreft.
Legemidlet er indisert for behandling av hepatocellulært karsinom, kolorektal kreft med høygradig mikrosatellittinstabilitet eller mismatch-reparasjonsdefekter, primært mediastinalt stort B-cellelymfom, spiserørskreft, trippelnegativ brystkreft og nyrecellekarsinom.
Den nåværende prisen på Keytruda er omtrent 62 millioner VND/flaske. Legemidlet har et delvis gratis støtteprogram for kvalifiserte kreftpasienter i henhold til Helsedepartementets beslutning nr. 2205/QD-BYT datert 2. juli 2025.
Støtteprogrammet ovenfor implementeres ved K Hospital og mange andre sykehus over hele landet. Med dette programmet er den maksimale kostnaden for en pasients behandlingssyklus omtrent 62 millioner VND med en dose på 200 mg (2 flasker), og noen sykluser kan være helt gratis, avhengig av hvilket støttenivå pasienten er godkjent for.
I mellomtiden fikk legemidlet Pembroria med virkestoffet pembrolizumab, 100 mg/4 ml hetteglass, produsert av aksjeselskapet «PK-137» i Russland, et registreringsbevis for sirkulasjon av Vietnams legemiddeltilsyn 31. oktober.
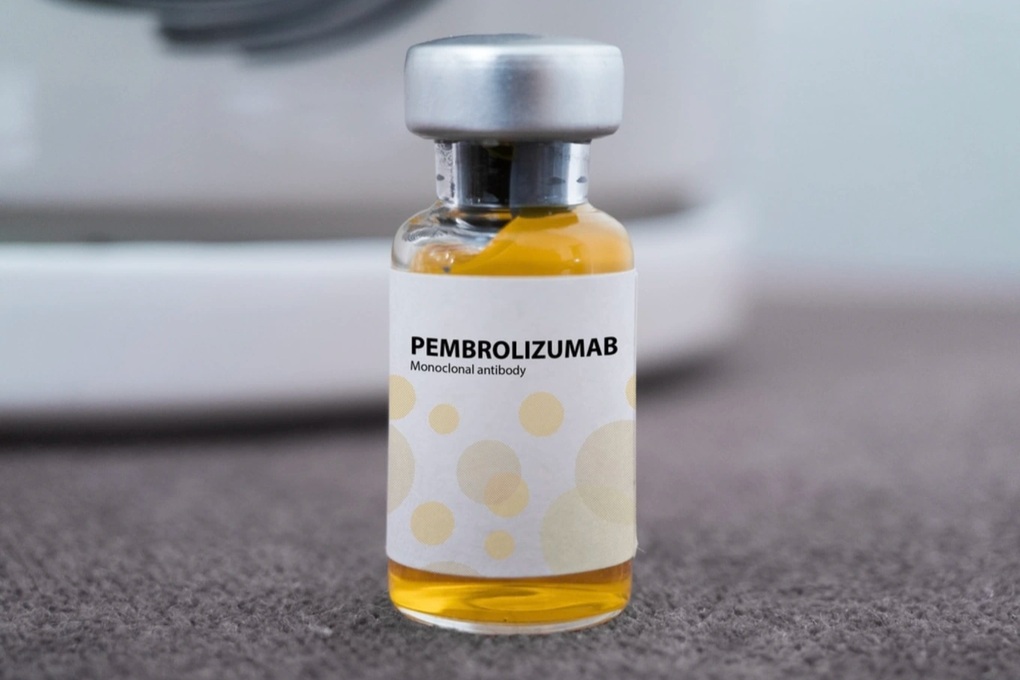
Et nytt russisk kreftlegemiddel har blitt godkjent for sirkulasjon i Vietnam, en behandling koster omtrent 36 millioner dong (Foto: incentra).
Pembroria er et biologisk legemiddel med samme aktive ingrediens som Keytruda, godkjent for følgende indikasjoner: melanom, ikke-småcellet lungekarsinom, plateepitelkarsinom i hode og nakke, klassisk Hodgkins lymfom, urotelialt karsinom.
Det russiske kreftmedisinet er indisert for behandling av øsofaguskreft, kreft med høygradig mikrosatellittinstabilitet (MSI-H) eller mismatch-reparasjonsdefekter, livmorhalskreft, nyrecellekarsinom, endometriekarsinom, trippelnegativ brystkreft, adenokarsinom i magesekken eller gastroøsofageal overgang, kolangiokarsinom.
Den estimerte prisen for Pembroria er omtrent 18 millioner VND/flaske, med en vanlig dose på 2 flasker for 1 behandlingssyklus. Dermed er kostnaden for en pasients behandlingssyklus omtrent 36 millioner VND med en dose på 200 mg (2 flasker).
For tiden planlegger K Hospital å kjøpe Pembroria-medisin til bruk for pasienter i nær fremtid.
Ikke alle kreftformer krever biologisk behandling.
K Hospital bemerker at ikke alle pasienter med kreftformene som er nevnt ovenfor, får forskrevet pembrolizumab.
Bruken av pembrolizumab avhenger også av mange faktorer, som for eksempel pasientens helsetilstand, type tumormutasjon, sykdomsstadium... vurdert av onkologer, individualisert for hver pasient, for å oppnå høyest mulig behandlingseffektivitet.
K Hospital bekreftet også at det russiske kreftbehandlingsmiddelet Pembroria ikke er et nytt kreftmedisin. Vietnam har for tiden nesten 100 typer monoklonale antistofflegemidler for kreftbehandling i omløp.
Tidligere bekreftet også Vietnams legemiddeltilsyn (helsedepartementet) at det russiske kreftbehandlingsmiddelet som nettopp har blitt godkjent for sirkulasjon, ikke er et kreftlegemiddel med en ny indikasjon.
I henhold til beslutning nr. 628/QD-QLD datert 31. oktober fra Vietnams legemiddeltilsyn, ble Pembroria innvilget et registreringsbevis for sirkulasjon i Vietnam med en gyldighet på 3 år. Legemidlet tilberedes i form av en konsentrert infusjonsløsning, med en holdbarhet på 24 måneder fra produksjonsdatoen.
Det forventes at dette legemidlet vil være tilgjengelig på det vietnamesiske markedet i 2026. Dette er et biologisk produkt som ligner på Keytruda, med komplette kliniske og forskningsmessige journaler. For tiden overvåkes legemidlet fortsatt for immunogenisitet.
Kilde: https://dantri.com.vn/suc-khoe/thuoc-tri-ung-thu-phien-ban-nga-se-co-tai-viet-nam-vao-nam-2026-20251113190818276.htm



![[Foto] Unik arkitektur på den dypeste metrostasjonen i Frankrike](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/14/1763107592365_ga-sau-nhat-nuoc-phap-duy-1-6403-jpg.webp)




























![[Foto] Spesialklasse i Tra Linh](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/14/1763078485441_ndo_br_lop-hoc-7-jpg.webp)
![[Foto] Unik kunst å male Tuong-masker](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/11/14/1763094089301_ndo_br_1-jpg.webp)







































































Kommentar (0)