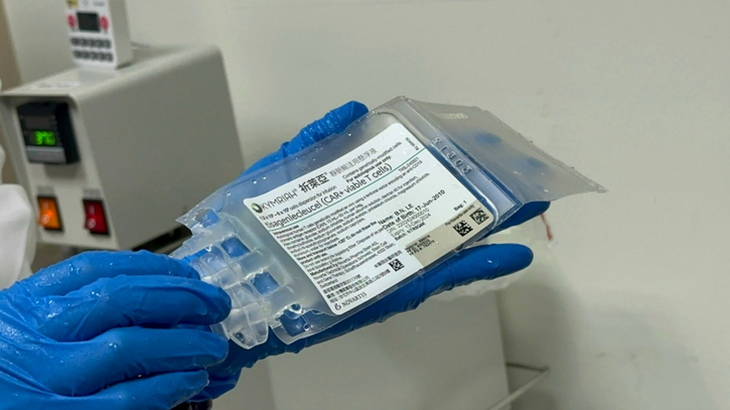
Poches de cellules de tisagenlecleucel avant leur perfusion chez les patients - Photo : BVCC
En conséquence, le Département des sciences, des technologies et de la formation du ministère de la Santé a reçu des informations des médias selon lesquelles l'hôpital de transfusion sanguine et d'hématologie de Hô Chi Minh-Ville a partagé des informations sur le premier cas au Vietnam d'application réussie de la thérapie par cellules CAR-T, ce qui donne de l'espoir à de nombreux enfants atteints de cancers du sang.
Le ministère a déclaré que l'utilisation de cellules et de produits cellulaires, y compris les cellules souches, dans la prévention et le traitement des maladies nécessite des preuves scientifiques de l'innocuité et de l'efficacité de la méthode.
Parallèlement, il est nécessaire de se conformer aux dispositions de la loi n° 15/2023/QH15 relative aux examens et traitements médicaux, du décret n° 96/2023/ND-CP du gouvernement détaillant et guidant la mise en œuvre de certains articles de la loi relative aux examens et traitements médicaux et de la circulaire n° 32/2023/TT-BYT du ministre de la Santé détaillant certains articles de la loi relative aux examens et traitements médicaux.
Afin de garantir les droits et la sécurité des patients au Vietnam et le respect de la réglementation légale en vigueur, le Département des sciences , des technologies et de la formation demande au Département de la santé de Hô Chi Minh-Ville d'examiner et de vérifier d'urgence les informations que l'hôpital de transfusion sanguine et d'hématologie de Hô Chi Minh-Ville a fournies aux médias concernant l'utilisation de la thérapie par cellules CAR-T par les patients au Vietnam.
Il précise la légalité de la thérapie par cellules CAR-T utilisée par le patient (que la thérapie ait été autorisée ou non pour une application dans le cadre d'examens et de traitements médicaux), ainsi que les protocoles et procédures en vigueur à l'hôpital pour les patients utilisant une thérapie par cellules CAR-T.
Parallèlement, il convient de revoir la réglementation relative au contrôle et à l'approbation du contenu des informations fournies aux médias concernant la thérapie cellulaire CAR-T de l'hôpital, afin de garantir des informations complètes et exactes.
Le département de la santé de Hô Chi Minh-Ville doit communiquer le contenu ci-dessus au ministère de la Santé (département des sciences, des technologies et de la formation, département des affaires juridiques, département de l'examen médical et de la gestion des traitements) avant le 25 septembre, afin de servir de base à un rapport aux dirigeants du ministère.
L'hôpital de transfusion sanguine et d'hématologie de Hô Chi Minh-Ville affirme être le premier à mettre en œuvre cette technique, en collaboration avec des partenaires étrangers. À ce jour, deux applications ont été réalisées, dont une couronnée de succès.
Le traitement réussi concernait une patiente de 12 ans atteinte d'une leucémie lymphoblastique aiguë à cellules B, appartenant au groupe à haut risque. Après une première rechute médullaire suite à une chimiothérapie, la patiente a reçu une greffe de moelle osseuse semi-compatible de son père, mais a rechuté une seconde fois.
La patiente a ensuite été traitée par thérapie cellulaire CAR-T avec le médicament Kymriah. À ce jour, après plus d'un an de traitement, elle est toujours en bonne santé, mène une vie normale et fait l'objet d'un suivi médical.
Concernant l'administration de cellules CAR-T par le médicament Kymriah aux enfants, elle a été réalisée à Taïwan (Chine) en raison d'un coût inférieur à celui des autres pays de la région et d'une collaboration professionnelle. Cependant, le coût du traitement restait très élevé, estimé à plusieurs dizaines de milliards de dongs.
« Il s'agit du premier cas d'un patient vietnamien utilisant le Tisagenlecleucel (un produit approuvé par la Food and Drug Administration américaine - FDA - pour le traitement des patients atteints de leucémie lymphoblastique aiguë en rechute en 2017) », a déclaré l'hôpital.
Qu’est-ce que la thérapie par cellules CAR-T ?
Les cellules CAR-T sont promues dans de nombreux pays développés, et le tisagenlecleucel est l'une des préparations approuvées par la FDA pour le traitement des patients atteints de leucémie lymphoblastique aiguë à cellules B récidivante/réfractaire.
Ce sont là les premiers pas vers l'accès des patients vietnamiens à des méthodes de traitement nouvelles et modernes, ouvrant de nombreuses perspectives de survie pour les patients ayant mal répondu aux traitements classiques antérieurs, et marquant en même temps un progrès dans la coopération internationale en matière de traitement des maladies malignes.
Source : https://tuoitre.vn/bo-y-te-yeu-cau-ra-soat-lieu-phap-car-t-cell-dieu-tri-benh-ac-tinh-ve-mau-20250919193013005.htm


![[Photo] Cat Ba - Île paradisiaque verte](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F12%2F04%2F1764821844074_ndo_br_1-dcbthienduongxanh638-jpg.webp&w=3840&q=75)






































































































Comment (0)