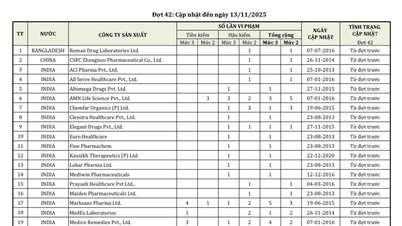
W związku z tym wśród prawie 600 produktów farmaceutycznych, składników farmaceutycznych i leków o udowodnionej bioekwiwalencji, którym tym razem Wietnamska Agencja Leków przyznała niedawno lub odnowiła ich rejestrację i certyfikaty dopuszczenia do obrotu, 404 krajowe produkty farmaceutyczne otrzymały niedawno certyfikaty rejestracji dopuszczenia do obrotu; 42 krajowe leki uzyskały odnowienie certyfikatów rejestracji dopuszczenia do obrotu, z czego 26 leków i składników farmaceutycznych odnowiono na 5 lat, a 14 leków i składników farmaceutycznych odnowiono na 3 lata.
Ogłoszono także 98 leków o udowodnionej bioekwiwalencji.
Wietnamska Agencja ds. Leków wymaga od firm produkujących leki stosowania się do zapisów i dokumentów zarejestrowanych w Ministerstwie Zdrowia , a także drukowania lub umieszczania na etykiecie leku numeru rejestracyjnego wydanego przez Wietnamskie Ministerstwo Zdrowia.
Przestrzegać w pełni wietnamskiego prawa i rozporządzeń Ministerstwa Zdrowia dotyczących produkcji i obrotu lekami w Wietnamie.

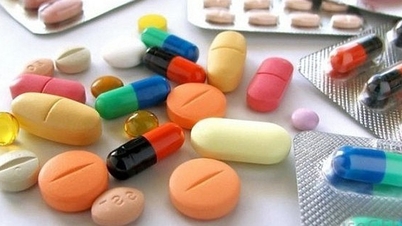
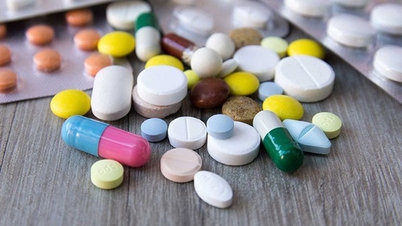
Ministerstwo Zdrowia wydało i odnowiło prawie 600 nowych leków, w tym dziesiątki leków bioekwiwalentnych...
Jednocześnie zakłady produkujące leki muszą zapewnić odpowiednie warunki funkcjonowania zakładu produkcyjnego przez cały okres ważności certyfikatu rejestracyjnego leku i składników leków.
Współpraca z placówkami leczniczymi w celu przestrzegania obowiązujących przepisów dotyczących leków na receptę, monitorowanie bezpieczeństwa, skuteczności i działań niepożądanych leków na obywateli Wietnamu oraz opracowywanie i raportowanie zgodnie z przepisami.
W szczególności w przypadku leków, których świadectwo rejestracji w obrocie zostało przedłużone, ale wniosek o aktualizację etykiety leku i instrukcji stosowania nie został złożony zgodnie z przepisami, Departament Administracji Leków wymaga dokonania aktualizacji zgodnie z przepisami punktu b, klauzuli 1, artykułu 37 Okólnika nr 01/2018/TTBYT w ciągu 12 miesięcy od daty przedłużenia świadectwa rejestracji w obrocie.
Ponadto placówki rejestrujące leki muszą zapewnić utrzymanie odpowiednich warunków operacyjnych przez cały okres ważności certyfikatu rejestrującego lek i składniki leku w obrocie.
Wiadomo, że produkty farmaceutyczne i składniki farmaceutyczne produkowane w kraju, którym niedawno przyznano rejestrację lub których rejestracja do obrotu została odnowiona, różnią się znacznie pod względem efektów farmakologicznych. Należą do nich leki stosowane w leczeniu infekcji dróg oddechowych; leki stosowane w leczeniu choroby zwyrodnieniowej stawów...; leki stosowane w leczeniu chorób układu krążenia, nadciśnienia, cukrzycy, nowotworów, leki przeciwwirusowe, antybiotyki, leki przeciwbólowe, leki przeciwzapalne... Ponadto leki o udowodnionej bioekwiwalencji różnią się także pod względem rodzajów.
Source: https://suckhoedoisong.vn/bo-y-te-cap-moi-gia-han-gan-600-thuoc-trong-do-co-hang-chuc-thuoc-tuong-duong-biological-nutrition-169251206123916227.htm


![[Zdjęcie] Przewodniczący Zgromadzenia Narodowego Tran Thanh Man uczestniczy w ceremonii wręczenia nagród VinFuture 2025](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F12%2F05%2F1764951162416_2628509768338816493-6995-jpg.webp&w=3840&q=75)



![[Zdjęcie] 60. rocznica powstania Wietnamskiego Stowarzyszenia Artystów Fotografików](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F12%2F05%2F1764935864512_a1-bnd-0841-9740-jpg.webp&w=3840&q=75)

































































































Komentarz (0)